
一、关于巨细胞病毒
巨细胞病毒(CMV,Cytomegalovirus)作为一种广泛存在的疱疹病毒,对造血干细胞移植患者的生命健康构成了严重威胁。
国家血液系统疾病临床医学研究中心主任、北京大学血液病研究所所长黄晓军教授指出,我国CMV的血清阳性率可高达92%,病毒复燃比例高达30%~60%。对于异基因造血干细胞移植患者,CMV感染会显著增加总死亡率、非复发死亡率以及相关住院时间和住院费用等。
多年来国内采用的CMV感染管理策略主要是基于PCR监测的抢先治疗,虽然抢先治疗是控制巨细胞病毒的有效方法,能够降低CMV疾病的发生,但仍有很多患者出现较高的CMV感染发生率、难治性巨细胞病毒感染及其带来的间接效应,且抢先治疗药物存在骨髓抑制、肾毒性等不良反应问题,增加了患者的死亡风险和医疗负担。
二、来特莫韦入中国
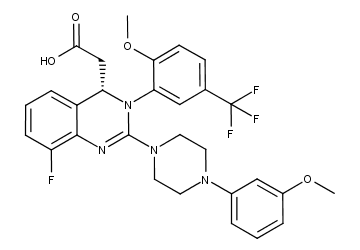
Letermovir结构式
药融云数据,vip.pharnexcloud.com/?zmt-mhwz显示:2022年1月,默沙东旗下新型非核苷类巨细胞病毒(CMV)抑制剂来特莫韦片(普瑞明®)获得中国国家药品监督管理局(NMPA)批准,用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒(CMV)血清学阳性的成人受者[R+]预防巨细胞病毒感染和巨细胞病毒病。
2022年5月,默沙东宣布,其新型非核苷类巨细胞病毒(CMV)抑制剂来特莫韦注射液(普瑞明®)获得国家药品监督管理局(NMPA)批准,用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒(CMV)血清学阳性的成人受者[R+]预防巨细胞病毒感染和巨细胞病毒病。
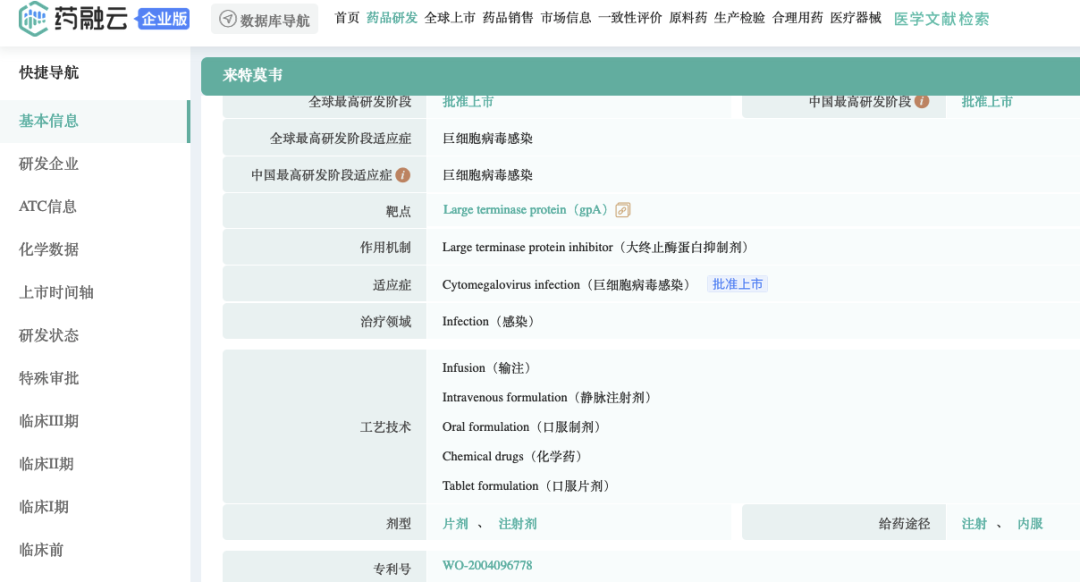
截图来源:药融云全球药物研发数据库
本品letermovir,化合物专利:WO-2004096778;最早开发企业为AiCuris,后被默沙东收购;2017年获得全球首次批准上市,后陆续进入加拿大、美国、欧盟、日本、中国等国家市场。据药融云统计,letermovir两款剂型,原研新药在2021财年全球销售业绩约3.7亿美元。
letermovir全球销售情况
截图来源:药融云全球药物研发数据库
三、仿制药递交上市
通用名称:来特莫韦片
商品名称:普瑞明®
规格:240mg*28片
适应症:本品用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒(CMV)血清学阳性的成人受者[R+]预防巨细胞病毒感染和巨细胞病毒病
药融圈监测,零售价格:35840元人民币
2022年12月13日,CDE承办受理公示了南京正大天晴制药有限公司的来特莫韦注射液仿制药上市申请。此前也受理了该公司来特莫韦片的仿制药上市申请。原研化合物专利将于2024年4月到期。
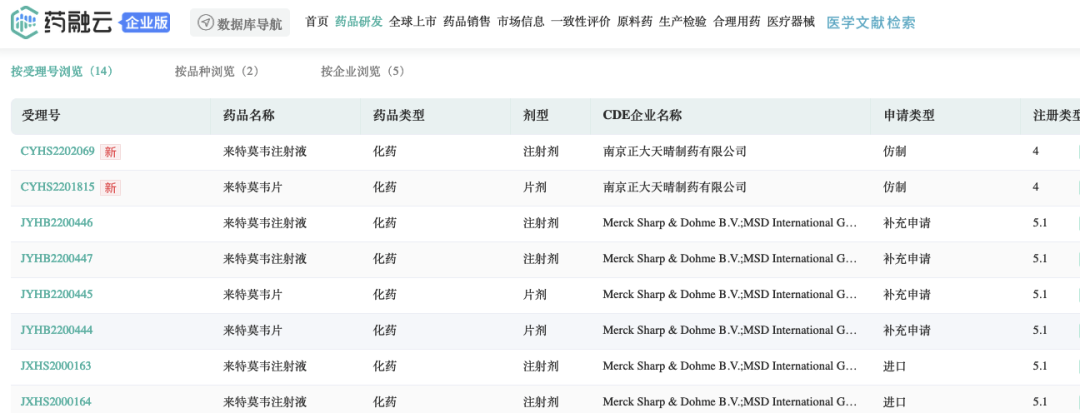
截图来源:药融云中国药品审评数据库
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据:vip.pharnexcloud.com/?zmt-mhwz;
FDA/EMA/PMDA;
相关公司公开披露;
https://www.msd.com/;
Liu J, et al. Patients with refractory cytomegalovirus (CMV) infection following allogeneic haematopoietic stem cell transplantation are at high risk for CMV disease and non-relapse mortality. Clin Microbiol Infect. 2015;21(12):1121.e9-15;
中国淋巴瘤治疗指南(2021年版)[J]. 中华肿瘤杂志, 2021, 43(7):29;
《专利法》第四十二条第三款规定,补偿新药上市审评审批占用的时间,专利期补偿制度;
药品专利纠纷早期解决机制实施办法(试行)公开征求意见;等等。
想要解锁更多疾病领域信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握疾病领域涉及药物信息、销售情况与各维度分析、市场竞争格局、创新药研发情况、仿制药布局情况、最新进展、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>
















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论