
据药融云中国药品审评数据库显示,近日CDE受理了罗氏「玛巴洛沙韦」干混悬剂的上市申请(受理号JXHS2200111)。
1.玛巴洛沙韦
玛巴洛沙韦(baloxavir marboxil)是一种First-in-Class的口服抗病毒药物,是近20年来首创的具有全新作用机制的抗流感病毒新药,被称为新一代抗流感“神药”;由日本盐野义制药公司对多替拉韦的母核进行结构改造得到,后授权给罗氏负责Xofluza美国、中国等市场的开发及销售。
药融云全球药物研发数据库显示,玛巴洛沙韦于2018年2月在日本获批上市,用于治疗既往健康(OwH) 患者的甲型或乙型流感病毒感染;同年10月在美国获批上市,这是近20年来在美国首个获批的抗流感药物;2021年4月玛巴洛沙韦在中国批准上市(商品名为速福达),用于12周岁及以上的流感患者,包括存在流感并发症高风险的患者。
玛巴洛沙韦上市时间轴
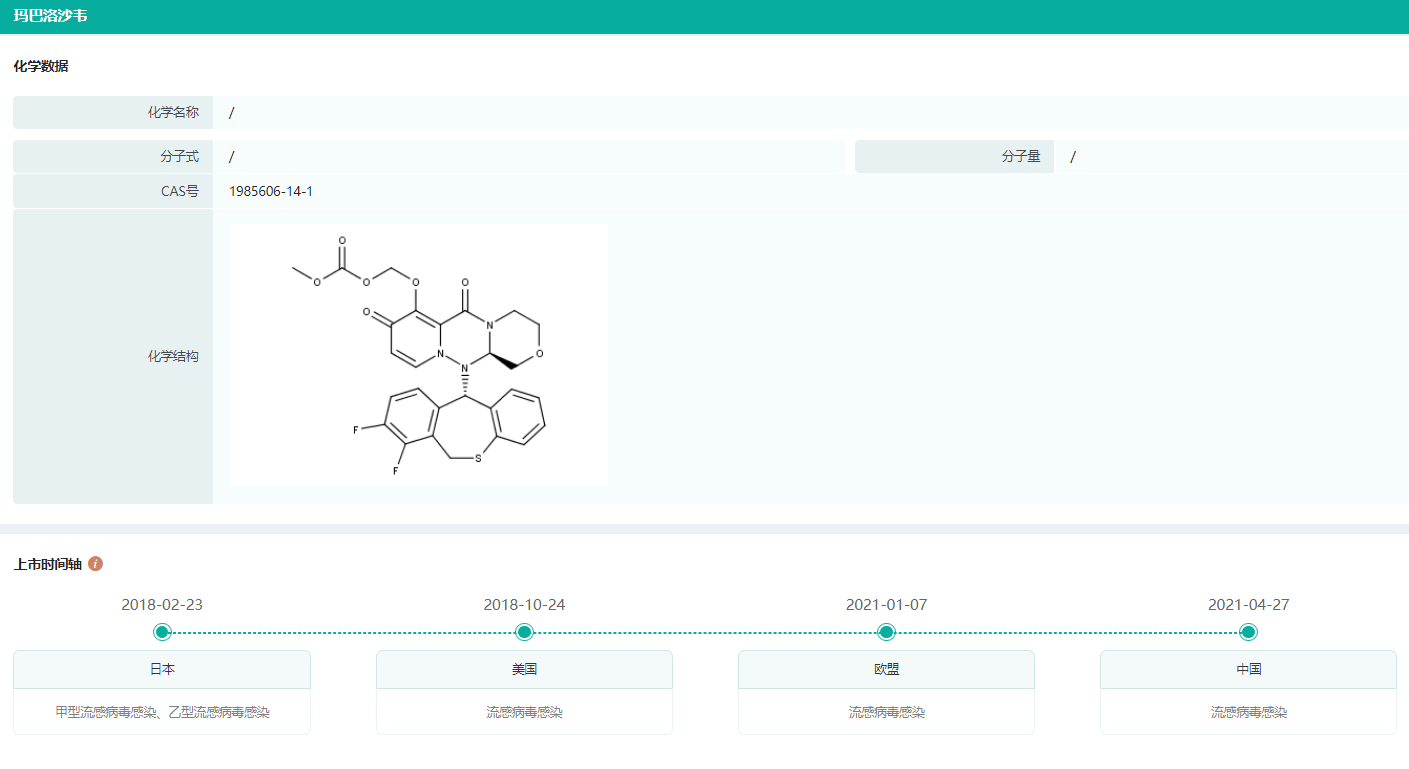
图片来源:药融云全球药物研发数据库
值得一提的是,玛巴洛沙韦(片剂)在获批8个月后就被获准纳入2021年版国家乙类医保目录,并被国内外流感治疗指南、共识列入推荐抗病毒治疗药物。此次,玛巴洛沙韦干混悬剂在国内申报上市,相比于片剂剂型,口服混悬剂可为儿童和吞咽困难的人提供更方便的治疗选择。
药融云药品招投标数据库显示,速福达(通用名:玛巴洛沙韦)最新医保价格为222.36元(20mgx2片/盒),每片约111元,在进入医保目录前,玛巴洛沙韦价格为498元,相比较以前,其降幅达55%。
玛巴洛沙韦片招投标信息(部分)
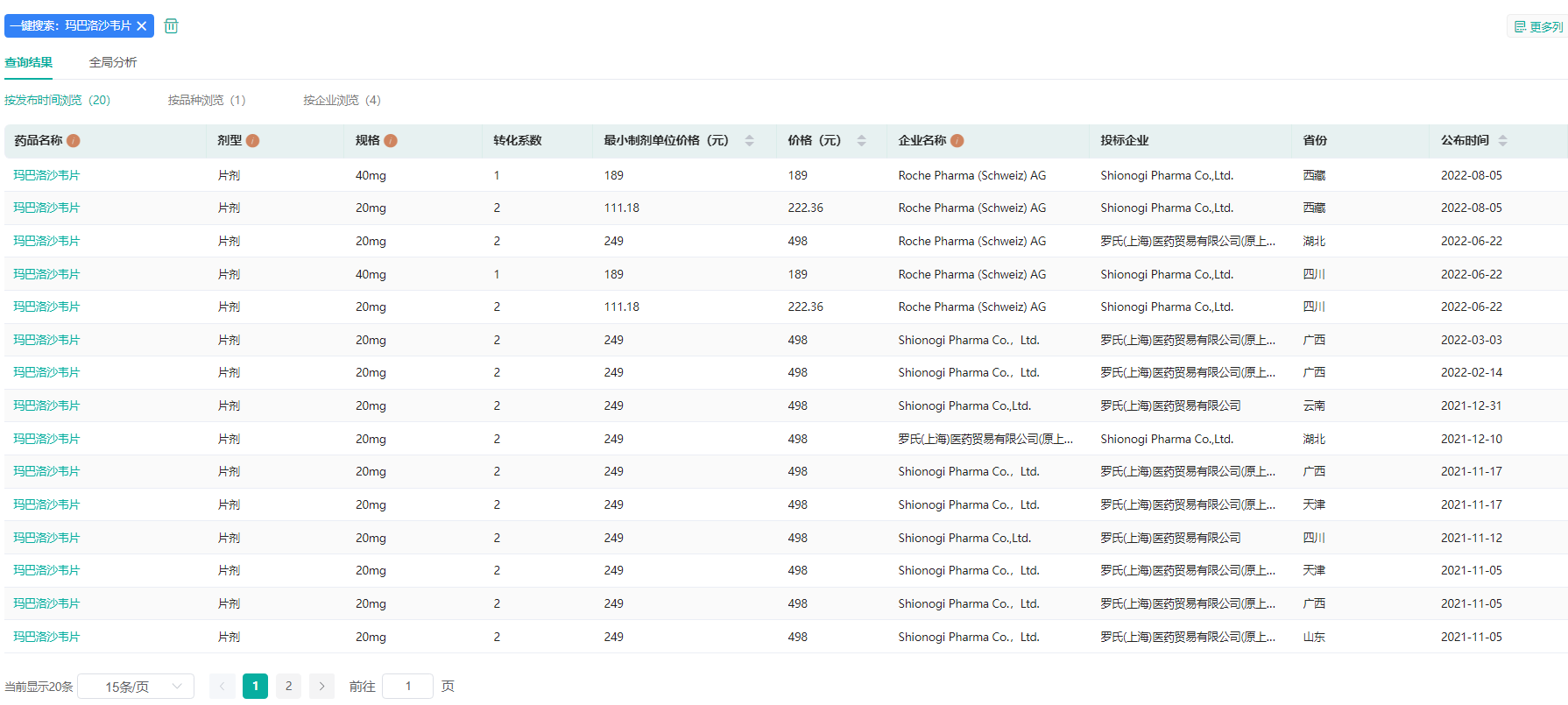
图片来源:药融云药品招投标数据库
玛巴洛沙韦不同于靶向神经氨酸酶的抗流感药(奥司他韦、laninamivir、帕拉米韦),它通过抑制流感病毒的cap-依赖型核酸内切酶来抑制病毒复制,在流感自我繁殖的早期发挥药效,快速降低体内病毒滴度,大幅减少流感的传播速度。
巴洛沙韦对A型和B型流感病毒、禽流感等均表现较强的抗病毒能力,还可显著降低高危患者的住院风险。目前关于玛巴洛沙韦对新型冠状病毒的治疗还在研究中。药融云全国医院销售数据库显示,玛巴洛沙韦2022年第二季度医院端销售额为623万元,增长率达到180.32%。
玛巴洛沙韦医院端销售额季度趋势(微信搜索"药融云小程序"查看更多维度数据分析)
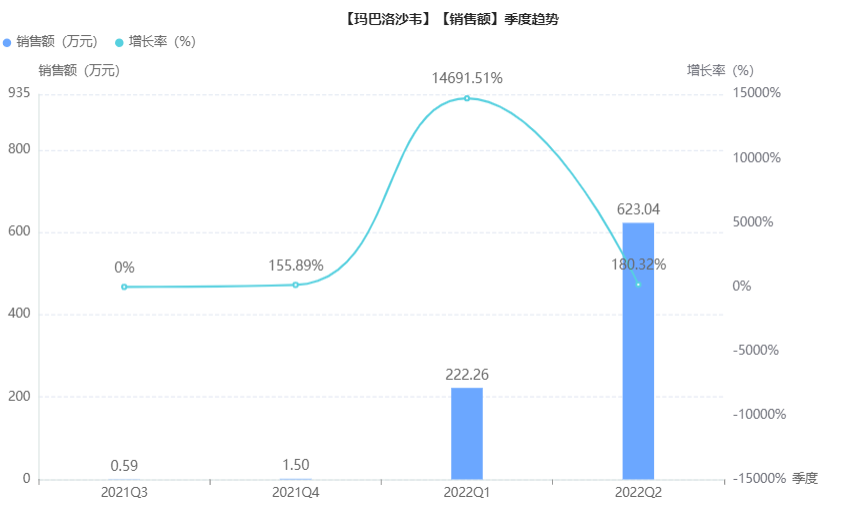
图片来源:药融云全国医院销售数据库
2.流行性感冒
流行性感冒简称流感,是一种季节性急性呼吸道病毒传染性疾病,每年在全世界范围内引起暴发和流行。流感病毒属于正黏病毒科,根据核蛋白和基质蛋白,分为甲、乙、丙、丁四型。目前感染人的主要是甲型和乙型流感病毒。
流感起病急,虽然大部分流感患者可以自愈,但部分患者可因出现肺炎、脑炎或心肌炎等并发症或基础疾病加重而发展成重症病例,少数病例病情进展快,可发生并发症而死亡。在全球范围内,流感每年可致约5%-10%的成人、20%-30%的儿童感染,造成多达500万例重症病例和65万例死亡。
目前国内市场上常见的抗流感病毒药物有奥司他韦、帕拉米韦、扎那米韦等神经氨酸酶抑制剂,以及血凝素抑制剂阿比多尔和聚合酶抑制剂法匹拉韦等,早期尤其是发病48小时之内应用抗流感病毒药物能显著降低流感重症和死亡的发生率。
据药融云全国医院销售数据库显示,2021年奥司他韦医院端的销售规模为11.24亿元,同比下降41.05%;其中宜昌东阳光长江药业占据92.69%的市场份额,其次是罗氏占据7.31%的市场份额。
奥司他韦年度销售趋势
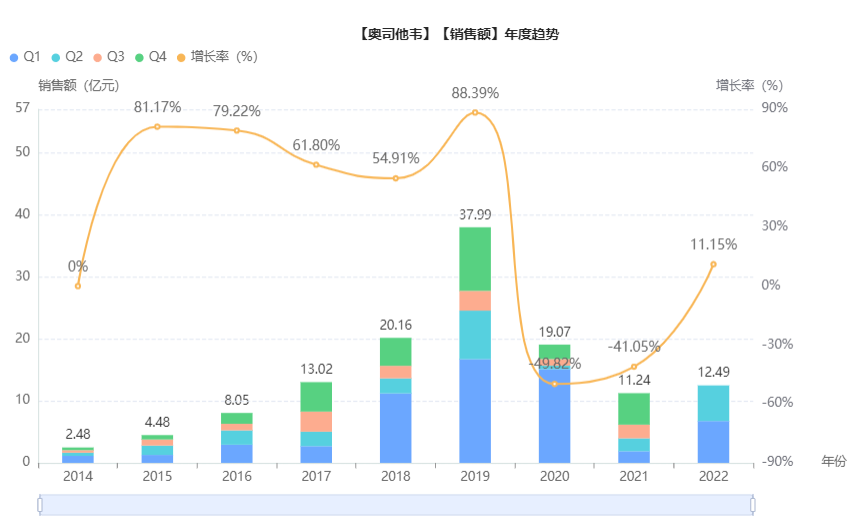
图片来源:药融云全国医院销售数据库
神经氨酸酶抑制剂类抗病毒药物可以选择性结合神经氨酸酶阻止病毒释放,对多种类型的流感病毒均有较强抑制作用,是目前临床上应用最广的一类抗流感病毒药物。此类药物需要每日服用两次,连续服用5天,而全新作用机制的玛巴洛沙韦(Xofluza)可以直接抑制病毒复制,患者在全病程只需服用一次,就能在24小时内停止病毒排毒。
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>













































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论