
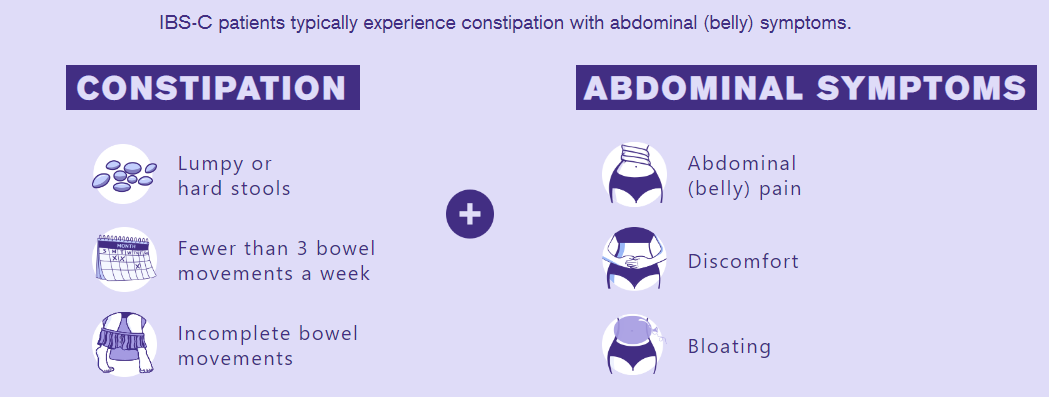
如果你便秘反复发作,并伴随与排便有关的腹痛、腹胀和腹部不适症状,那么你有可能就是肠易激综合征患者。肠易激综合征(IBS)是临床常见的一种功能性肠病,是便秘型肠易激综合征(IBS-C)的亚型之一。
依据肠易激综合征患者在根本症状基础上出现的不同排便习惯改变,现有分类标准将肠易激综合征分为腹泻型、便秘型、混合型和未定型四类,其中主要表现为便秘的就是IBS-C患者,流行病学数据显示,我国的肠易激综合征整体患病率约为6%,其中约15.1%为IBS-C型,对应着约1400万人的庞大患者群体。
在2019年利那洛肽(Linzess,Linaclotide)进入中国市场以前,IBS-C在我国还没有针对性的有效治疗药物,治疗主要是根据症状选择合适的药物,如解痉剂、渗透性泻药等。该药为胶囊剂,用于治疗便秘肠易激综合征(IBS-C) 和慢性特发性便秘(CIC),它是首个具有此种作用机制的治疗便秘的药物。
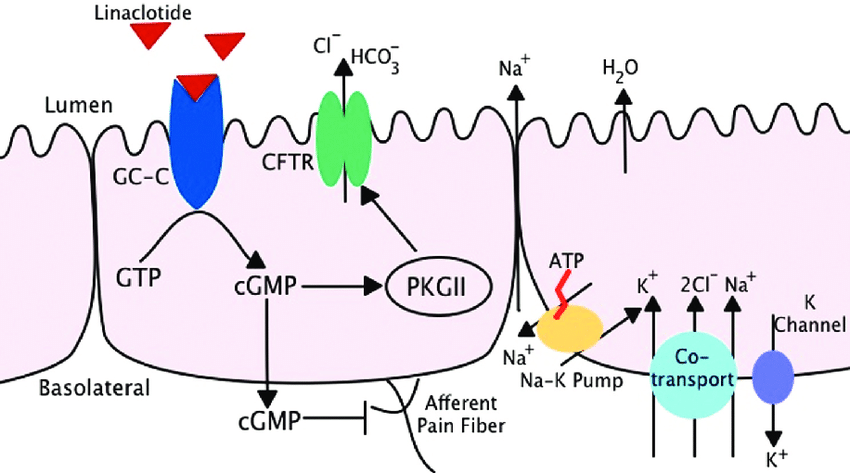
利那洛肽的作用机制
而开发利那洛肽的先驱,是专注于胃肠(GI)领域的Ironwood Pharmaceuticals。

Ironwood Pharmaceuticals Inc.(铁木制药公司)前身最早成立于1998年,总部位于美国马萨诸塞州波士顿。2008年4月7日,公司由Microbia公司更名为Ironwood Pharmaceuticals。2010年2月,Ironwood在纳斯达克上市,代码:IRWD。Ironwood是一家专注于GI的医疗保健公司,致力于推进胃肠道疾病的治疗并重新定义数百万胃肠道患者的护理标准。
Ironwood公司基本信息与投融资情况
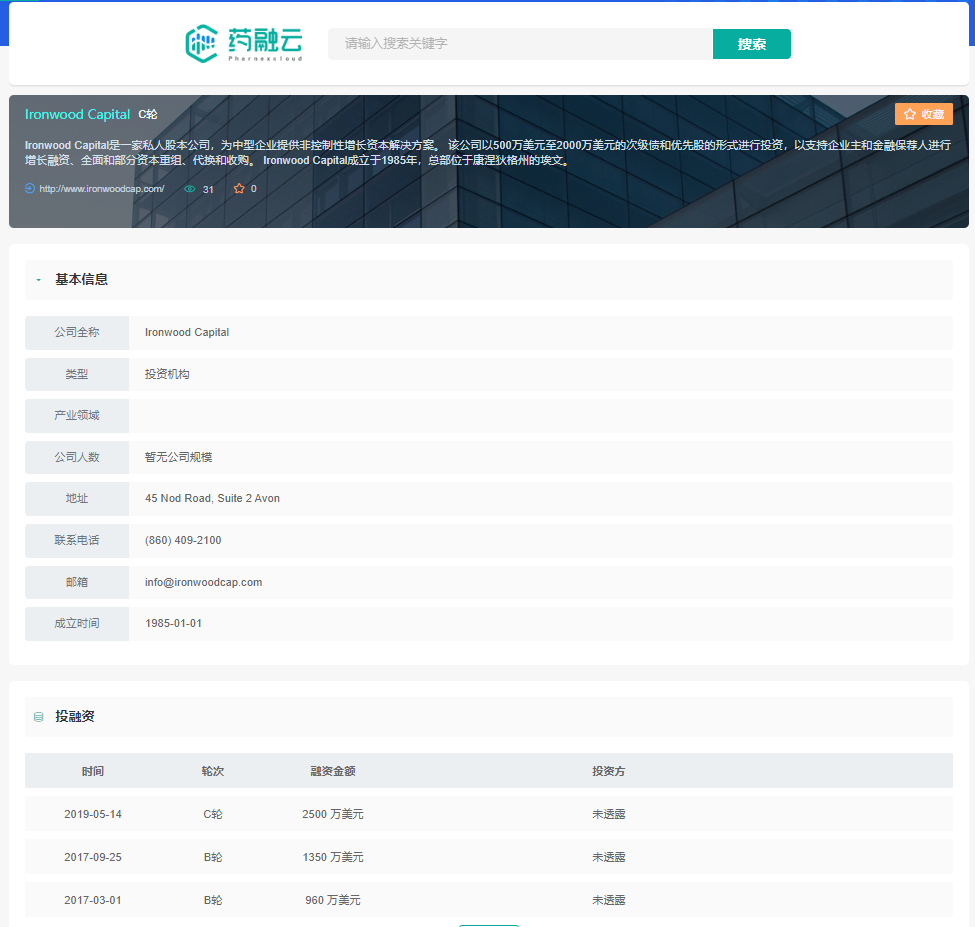
截图来源:药融云投融资数据库
自2021年起,ThomasA. McCourt任职Ironwood的CEO。他在2009年加入公司后,一直担任营销高级副总裁和首席商务官。在加入Ironwood之前,他曾于2008年4月至2009年8月期间,领导Amgen Inc.的地诺单抗的美国品牌团队。2001年至2008年,他任职于Novartis,指导用于治疗IBS-C和CIC患者的ZELNORM的推出和发展,并担任许多高级商务职务,包括战略营销和运营的副总裁。他还是Astra Merck Inc.创始团队的成员之一,领导医务和科学联络部门的发展,随后担任Prilosec and NEXIUM 的品牌经理。他拥有威斯康星大学的药学学位。

截至2021年12月31日,Ironwood公司员工人数共219名。其中药物开发团队有40人,销售和商业团队有126人,行政职能有53人。
便秘患者的福音——Ironwood王牌产品利那洛肽
在美国,利那洛肽是针对IBS-C/CIC成人的处方品牌Top1治疗药物,自推出以来约有400万患者。在品牌类IBS-C/CIC总处方药市场中,利那洛肽所占市场份额维持在60%~80%之间。
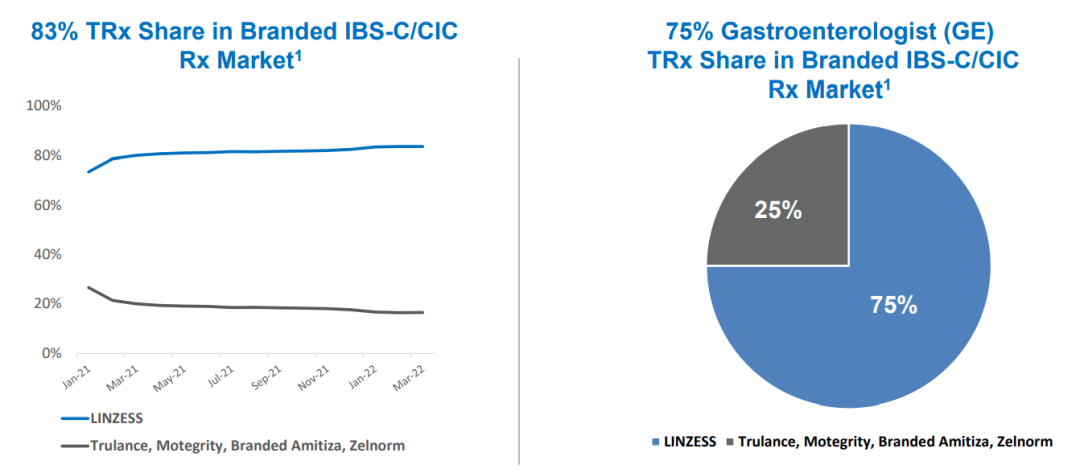
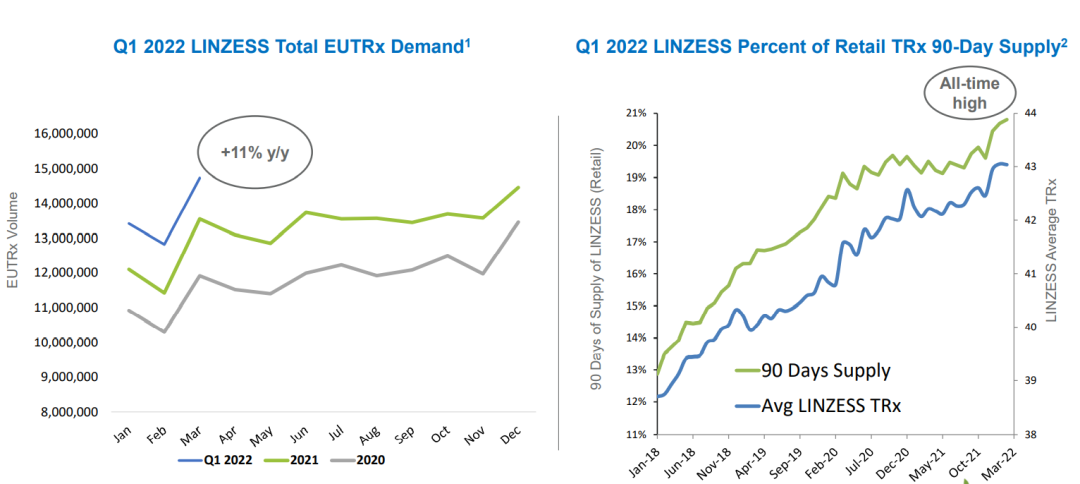
2022年一季度,利那洛肽需求继续保持两位数增长;90天的TRx将平均利那洛肽 TRx 推至历史新高:
2021年,利那洛肽成为同行中的一枚“重磅炸弹”,全球销售额约合10.99亿美元:

利那洛肽的相关历史
2017年1月25日,美国食品药品监督管理局(FDA)批准72微克剂量的令泽舒(Linzess)®利那洛肽(linaclotide),用于慢性特发性便秘(CIC)成人患者的治疗。此次批准是基于在1223例成人CIC患者中开展的一项III期临床研究的积极数据。数据显示,与安慰剂相比,利那洛肽72微克剂量在治疗的整个12周期间在完全自发排便方面实现了统计学意义的显著改善,达到了研究的主要终点。
截至目前,利那洛肽已获美国FDA批准3种剂量:290微克用于便秘型肠易激综合征(IBS-C)成人患者的治疗,145微克和72微克用于慢性特发性便秘(CIC)成人患者的治疗。
2019年1月15日,Ironwood合作伙伴阿斯利康(AZ)宣布,国家药品监督管理局(NMPA)已正式批准利那洛肽在中国上市。作为我国专门治疗成人便秘型肠易激综合征(IBS-C)的处方药物,利那洛肽的获批将填补我国成人便秘型肠易激综合征的治疗空白,为广大国内患者带来福音。
关于利那洛肽
利那洛肽分子的三维结构:
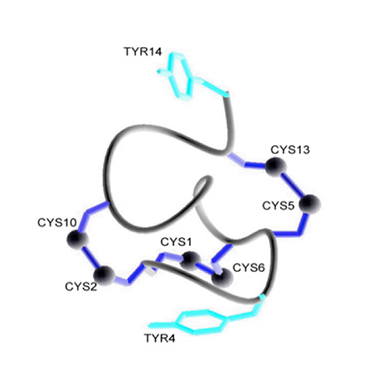
利那洛肽是一种鸟苷酸环化酶-C激动剂,是美国消化病学会(AGA)指南推荐的一种治疗便秘型肠易激综合征(IBS-C)的创新药物,也是治疗IBS-C的标准药物(推荐级别:强,证据级别:高)。中国Ⅲ期临床试验证实,与安慰剂组相比,利那洛肽可显著缓解IBS-C相关症状,其缓解程度反应者比例是安慰剂组的两倍以上(31.7%vs15.4%),疗效在治疗第一周就有体现,并在整个治疗期间症状都得到了改善。此外,由于利那洛肽作用于肠道局部,几乎不吸收入血,其安全性更为良好。研究显示,利那洛肽最常见的不良反应为轻度和中度腹泻,未见临床显著后遗症。
利那洛肽药物基本信息
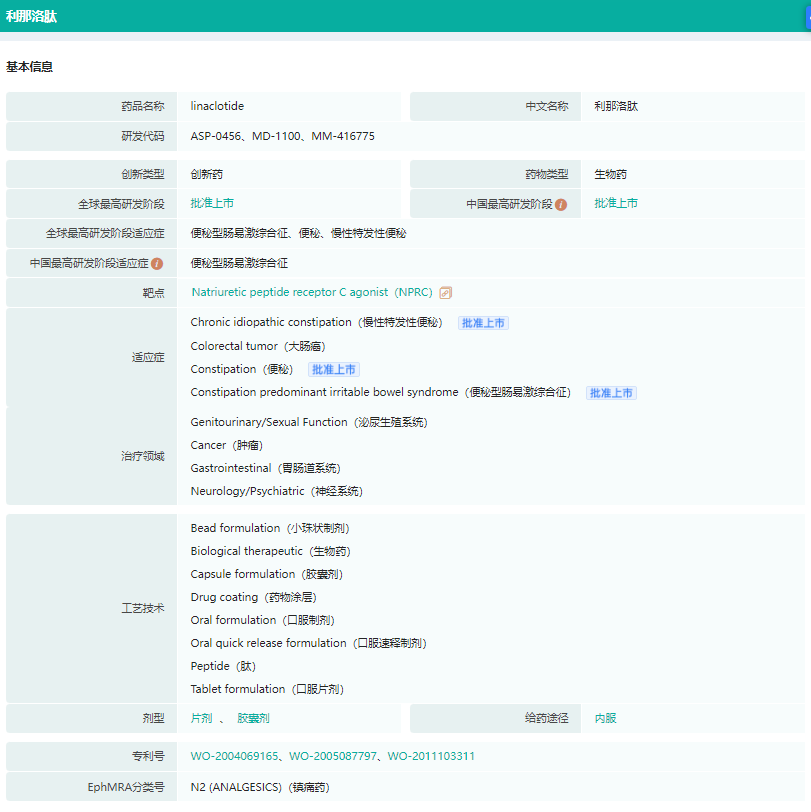
截图来源:药融云全球药物研发数据库
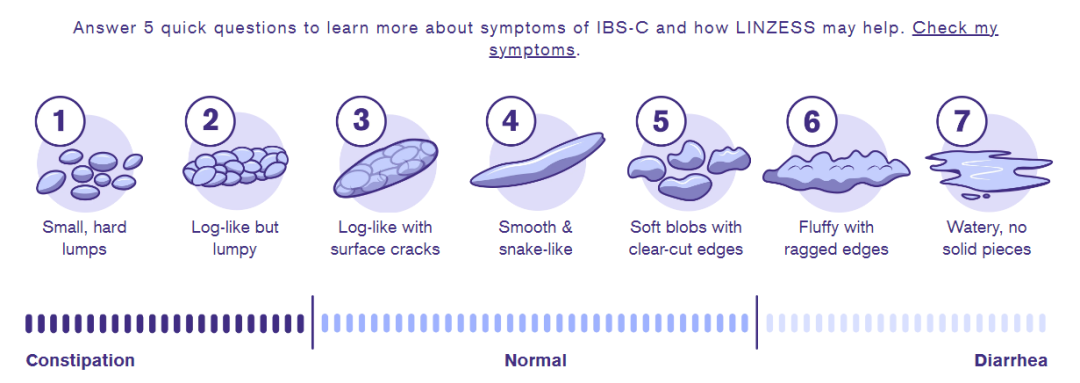
利那洛肽的创新机制是通过激活人体一种自有的鸟苷酸环化酶,促使肠液分泌,并通过降低内脏高敏感,达到同时缓解便秘型肠易激综合征患者腹痛、腹胀和便秘等症状的效果。与安慰剂比较,六成以上的患者在使用一天后就能够实现自主排便;一周内,患者的严重腹痛症状及完全自主排便频次均获得显著改善6;近九成的患者在整个治疗周期内,自主排便次数显著增加,近八成的患者腹痛、腹胀显著改善。

利那洛肽是每日服用一次的药丸,可以帮助缓解IBS-C和CIC的症状,包括与IBS-C相关的腹部疼痛和整体腹部症状(疼痛,不适和腹胀)。

利那洛肽的活性药物成分是linaclotide,这是一种鸟苷酸环化酶‐C(GC-C)激动剂,能够结合并局部作用于小肠上皮管腔表面的GC-C受体。GC-C的激活导致细胞内和细胞外环磷酸鸟苷(cGMP)浓度均升高。细胞内cGMP升高刺激氯离子和碳酸氢根离子分泌进入肠腔,导致小肠分泌液增加和加速通过。动物模型中,linaclotide还表现出减轻小肠疼痛的作用,而这被认为是细胞外cGMP增加所介导,降低了肠道疼痛感应神经的活动,从而诱导内脏疼痛减轻。
Ironwood产品与业务
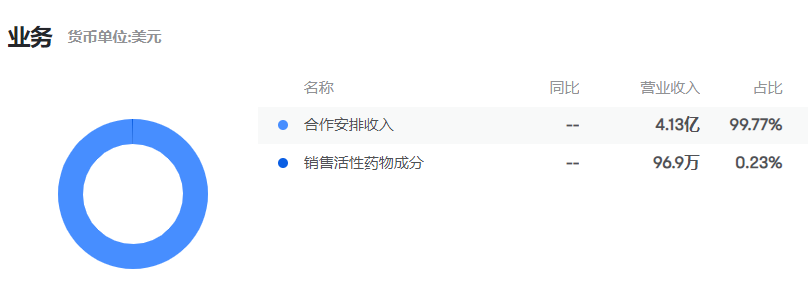
从业务类型来看,Ironwood营业收入主要来自两大业务类型:合作权益收入,直接销售活性药物成分(API)收入。2021年,合作权益收入$4.13亿,占比99.77%;销售活性药物成分实现营收$96.9万,占比0.23%。
从市场地区分布来看,其大部分收入来自利那洛肽在美国的销售。2021年,Ironwood与利那洛肽有关的销售收入为$4.004亿,同比增长9%,这一增长主要是由于2021年美国利那洛肽处方需求增加。下图是Ironwood与合作公司在美国和日本两地的营收占比情况:
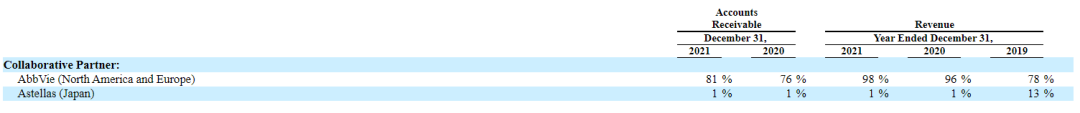
在北美和欧洲地区,AbbVie与Ironwood合作销售利那洛肽。2021年,Ironwood与AbbVie合作,营收$4.05亿,占总营收比重为98%,收款额度占比81%;在日本的合作公司是Astellas,2021年的营收占比和收款额度占比都为1%。
在中国(包括中国香港和澳门),Ironwood的销售合作方是阿斯利康(AstraZeneca),2021年利那洛肽中国营收$74.3万。阿斯利康是全球领先的制药公司,由前瑞典阿斯特拉公司和前英国捷利康公司于1999年合并而成,总部位于英国伦敦,于1993年进入中国。
2019-2021合作权益收入和API销售收入的具体金额如图所示:

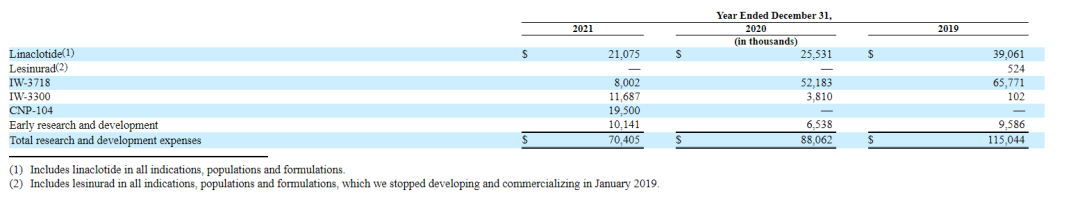
近3年Ironwood研发费用(R&D)相关数据如下,2021年总研发投入金额为$7040万:
- MD-7246:是Ironwood与AbbVie曾开发的一种利那洛肽的缓释制剂。2020年5月,该公司和艾伯维(AbbVie)公布了一项II期试验的一线数据,该试验评估了MD-7246在与IBS-D相关的腹痛成人患者中的疗效。II期试验未达到其主要或关键次要终点。基于这些发现,MD-7246的开发停止。
- IW-3718:是一种胆汁酸螯合剂的胃滞留制剂,用于治疗难治性胃食管反流病或难治性GERD。2020年9月,Ironwood在难治性GERD中评估IW-3718的两项相同的III期试验中有一项不符合与计划的早期疗效评估相关的预先指定的标准,并停止了IW-3718的开发。
- IW-3300:一种GC-C激动剂,用于内脏疼痛疾病的潜在治疗,包括间质性膀胱炎/膀胱疼痛综合征和子宫内膜异位症。2021年12月,美国FDA接受了我们的研究性新药申请,IC/BPS的I期临床计划于2022年第一季度开始。
- CNP-104:通过COUR合作协议,Ironwood和COUR正在开发用于治疗PBC的CNP-104,这是一种针对肝脏的罕见自身免疫性疾病。2021年12月,COUR获得了CNP104的美国快速通道指定,并启动了CNP-104的临床研究,以评估CNP104在PBC患者中的安全性、耐受性、药效学作用和疗效。
Ironwood产品管线(部分)
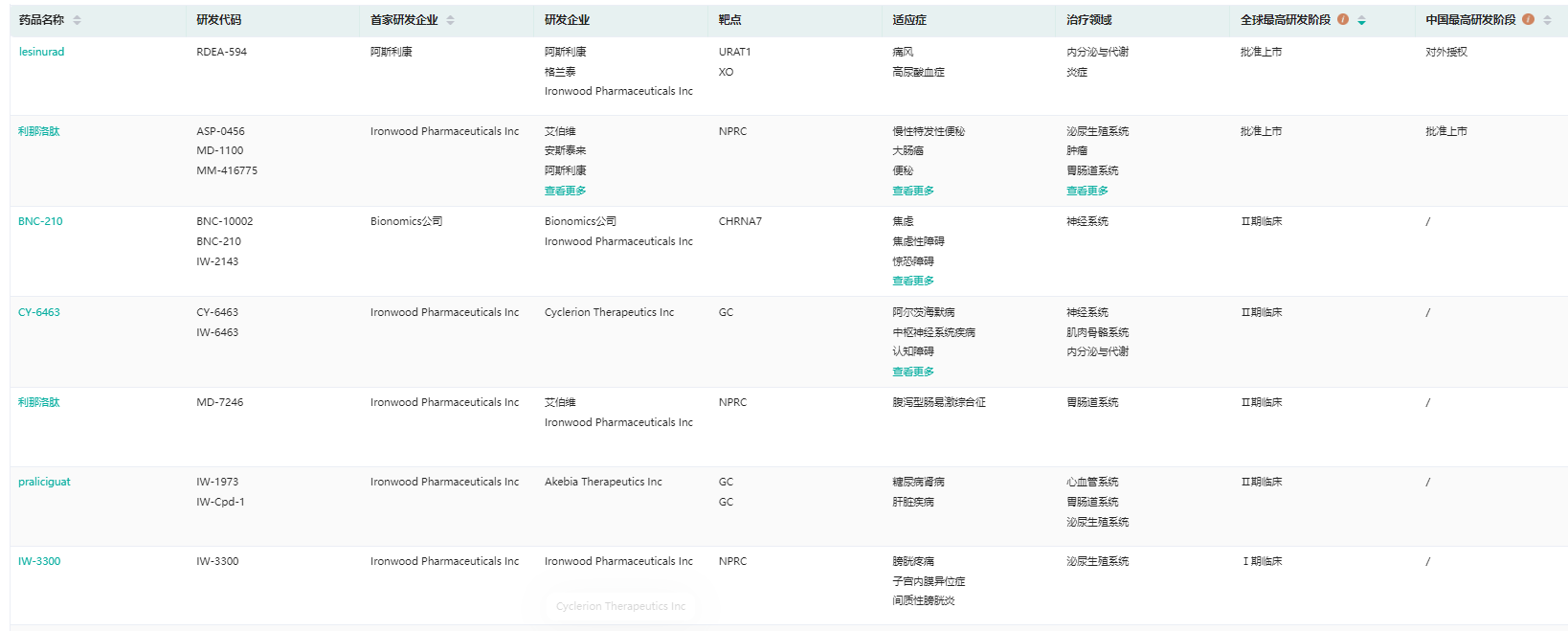
截图来源:药融云全球药物研发数据库
主打产品
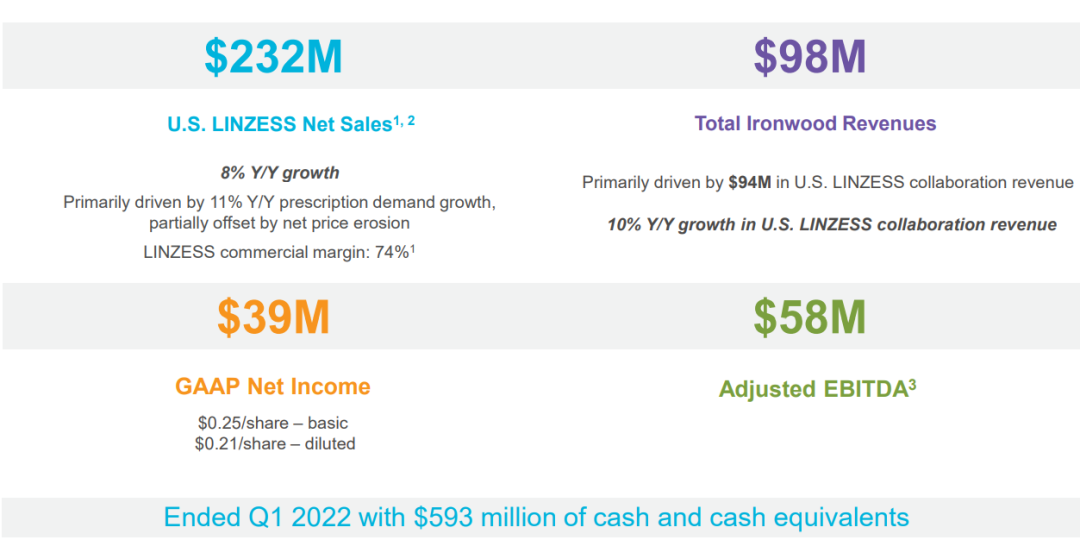
Ironwood在2021财年净利润为$5.28亿,现金和现金等价物为6.201亿美元。

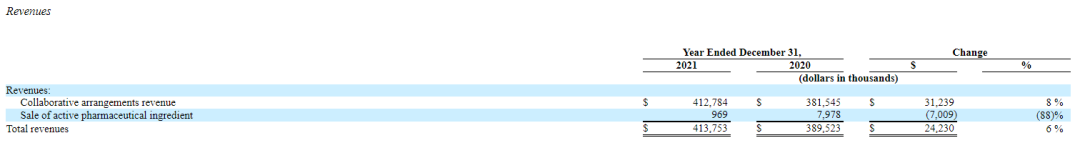
2022年5月6日,Ironwood发布2022年一季报,2022年一季度实现营收$9800万,主要受美国利那洛肽合作收入$9400万的推动。利那洛肽在美国净销售额达到$2.32亿。
战略与目标
三大战略抓手:
▶最大化利那洛肽;
▶加强GI管线创新能力;
▶持续创造收益产生现金流。

Ironwood计划2022年实现利那洛肽在美国净销售额个位数增长,全年总营收预计在$4.2亿~4.3亿:
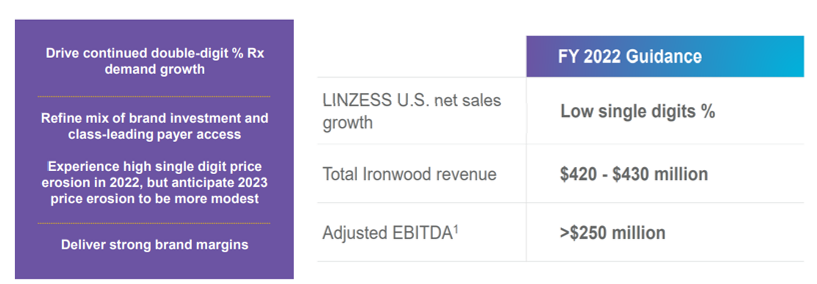
2022年Ironwood战略规划:
▶持续推动两位数百分比的Rx需求增长;
▶完善品牌投资和领先的支付方准入组合,在2022年价格以高个位数比例下降,但预计2023年的价格能实现轻微下降;
▶提供强劲的品牌利润率。
产品管线

- 1.利那洛肽
Ironwood与AbbVie合作开展IBS-C和功能性便秘(FC)的儿科计划。美国患有功能性便秘(FC)的6~17岁的儿童现有4~600万。Ironwood称FC研究结果将在2022年下半年公布,该研究使用72微克剂量的自发肠道运动作为主要终点。目前,还没有FDA批准用于IBS-C和FC的处方儿科治疗。
- 2.IW-3300
间质性膀胱炎/膀胱疼痛综合征(IC/BPS)在美国影响着4~1200万人,Ironwood已完成单次递增剂量临床研究,并有望在2022年第二季度启动多次递增剂量研究。预计将在2022财年末开始第2阶段概念验证研究,重点关注IW-3300的内脏疼痛益处。
- 3.CNP-104
美国大约有13.3万人患有原发性胆汁性胆管炎(PBC),COUR预计在2023年公布该公司在2022年第一季度发起的临床研究。终点包括安全性、耐受性、药效学和疗效结果,例如碱性磷酸酶的变化,旨在为急需新治疗方案的PBC患者引入一种可能改变游戏规则的新疗法。
近 况
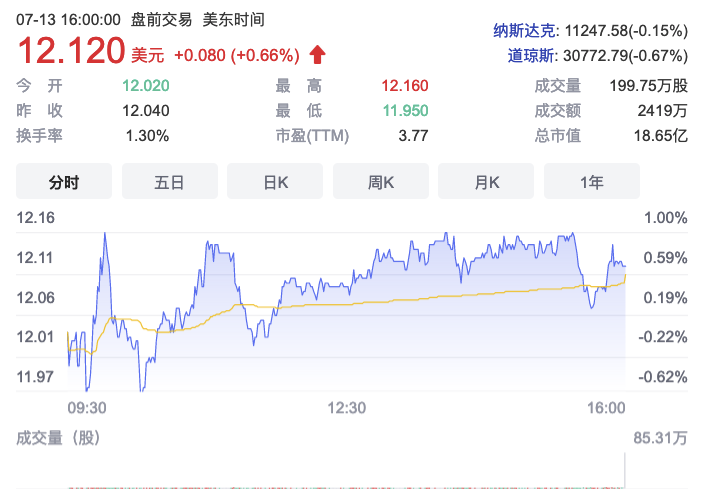
截至美国当地时间2022年7月13日收盘,Ironwood公司股价$12.12,总市值约$18.65亿。
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据库,www.pharnexcloud.com;
FDA/EMA/PMDA;
相关公司公开披露;
https://ironwoodpharma.com;
https://Ironwoodpharma.com/wp-content/uploads/2022/04/iw-ESG-2021-1.pdf;
从百年多肽发展史看多肽药物发展机会;
口服多肽药物开发情况及其前沿技术简介;
https://s2.q4cdn.com/924599680/files/doc_financials/2021/ar/c5d341c2-503c-4176-a56f-af98e56aa1d4.pdf;
https://d18rn0p25nwr6d.cloudfront.net/CIK-0001446847/c64e9491-253a-4d67-8755-4a6435abcaae.pdf;
https://d18rn0p25nwr6d.cloudfront.net/CIK-0001446847/c5d341c2-503c-4176-a56f-af98e56aa1d4.pdf;
邹多武.利那洛肽:慢性便秘和便秘型肠易激综合征的新选择.中华消化杂志 2019 Apr,39(4):286-288.;
中华医学会消化病学分会胃肠功能性疾病协作组;中华医学会消化病学分会胃肠动力学组.中国肠易激综合征专家共识意见(2015年,上海)[J].中华消化杂志,2016,36(5):299-312.;等等。
想要解锁更多药企信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息;投融资情况;最新动态;产品管线布局、药物基本信息、研进展、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论