
甲苯磺酸艾多沙班片是日本第一三共研发的一种选择性Xa因子抑制剂,于2011年4月率先在日本上市,用于静脉血栓栓塞症(VTE)。2015年1月在美国获批用于降低非心脏瓣膜病引起的房颤患者卒中和危险血栓 (系统性栓塞) 风险。2018年12月,甲苯磺酸艾多沙班正式进入中国,用于伴有一个或多个风险因素(如充血性心力衰竭、高血压、年龄≥75 岁、糖尿病、既往卒中或短暂性脑缺血发作(TIA)病史)的非瓣膜性房颤(NVAF)成人患者,预防卒中和体循环栓塞。用于治疗成人深静脉血栓(DVT)和肺栓塞(PE),以及预防成人深静脉血栓和肺栓塞复发。目前仅有原研产品在售,尚无仿制药获批。
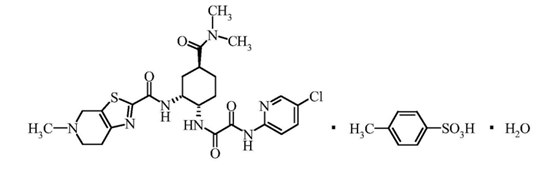
图1. 甲苯磺酸艾多沙班结构
据药融云统计,艾多沙班的销售额自上市后一路攀升,2021年达16亿美元,但是,随着仿制药企业的杀入,仿制药的陆续上市将会对其造成致命打击,尤其是国内集采情况下。
艾多沙班全球销售情况
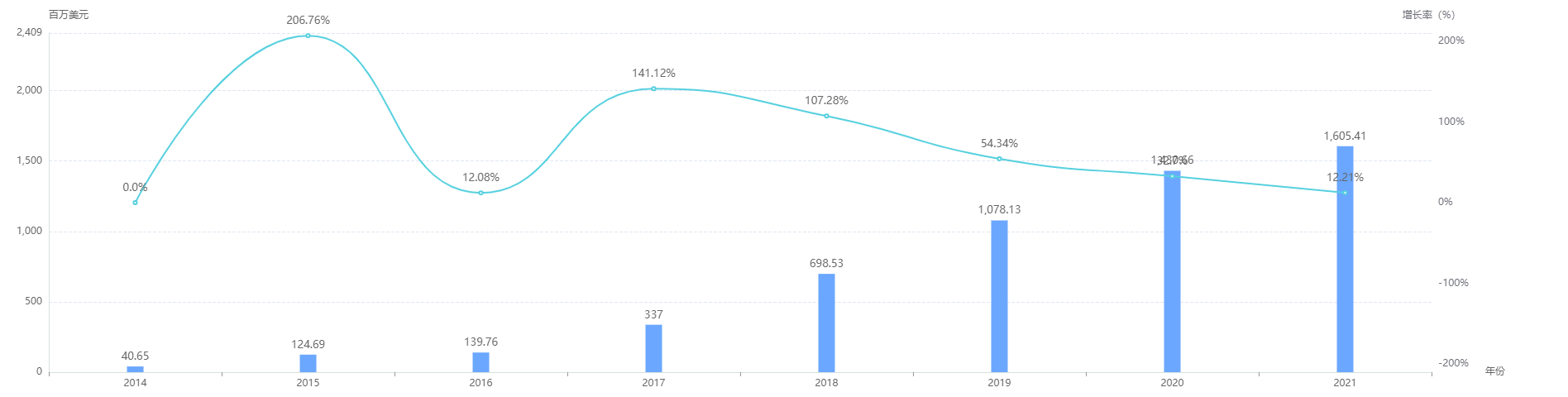
图片来源:药融云全球药物研发数据库
随着山东新时代药业于今年5月份提交了甲苯磺酸艾多沙班片仿制药的上市申请,该产品先后已有海南先声药业、南京正大天晴和扬子江药业集团南京海陵药业等四家企业以仿制4类提交上市申请。
甲苯磺酸艾多沙班片仿制药申报情况
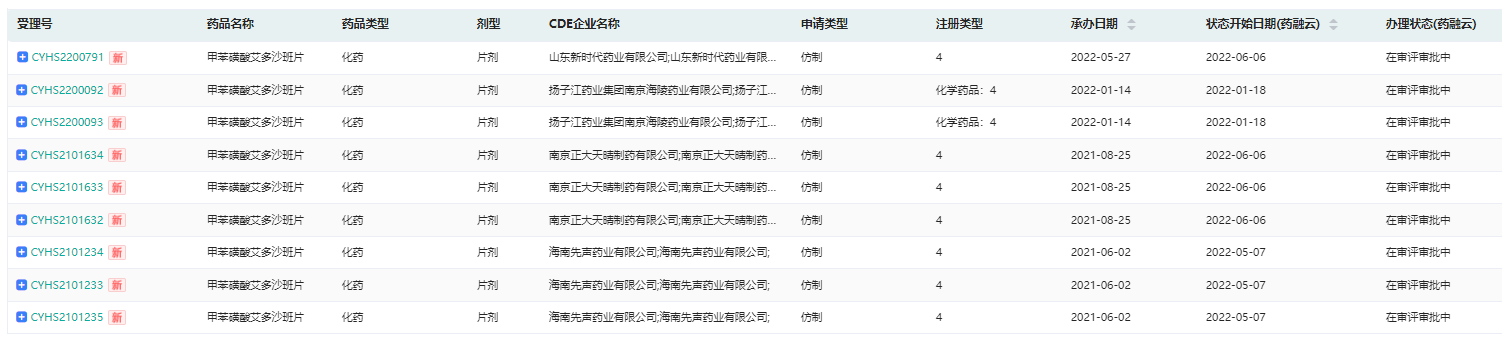
截图来源:药融云中国药品审评数据库
下图是甲苯磺酸艾多沙班片原研国内专利布局,从专利类型看,原研主要保护了化合物、药物组合物及用途,但相应的外围专利布局较少,缺少对核心产品的立体、多层次的保护,随着核心专利于今年6月19日的到期,仅剩制剂组合物专利尚在保护期内,其专利有效期至2028年3月27日。如果能规避或者无效掉原研制剂组合物专利,仿制药企业就可以提前六年上市,这对仿制药企业的诱惑无疑是巨大的。
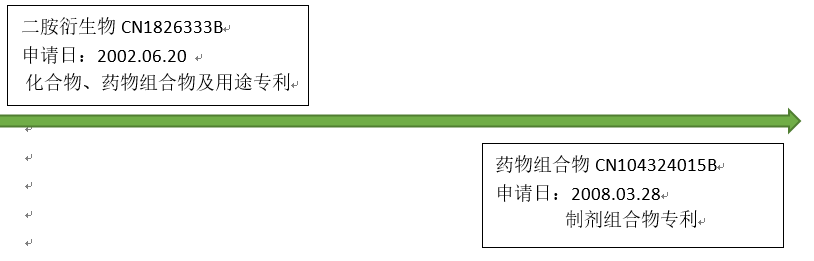
图2.原研国内专利布局
从中国上市药品专利信息登记平台已公开的三家仿制药企业的专利声明信息可知,三家药企都采取了规避或者挑战制剂组合专利的申报策略。其中两家企业选择专利挑战,一家选择进行专利规避。对比仿制药上市申请信息,可知海南先声药业没有选择专利声明。
表1.仿制药企业专利声明
南京正大天晴公司于去年10月29日对原研药物组合物专利CN104324015B提出了无效宣告请求,今年5月18日国家知识产权局做出了无效审查决定。从公布的无效审查决定看,原研部分权利要求因为概况范围过大,超过了说明书公开范围,从而得不得说明书支持而被判定无效。具体的看主要是原研专利权利要求对组合物中活性成分及包衣材料保护范围过宽,活性成分不仅包括艾多沙班,还包括其药理上可接受的盐或它们的水合物,而说明书中能支持其达到发明技术效果的仅为对甲苯磺酸盐一水合物。包衣材料同样是限定的材料范围过宽,得不得说明书的支持。权利要求中与发明改进点密切关联的技术特征可概括程度取决于说明书对该特征变化与技术效果之间对应关系和规律的阐释和证明程度。如果说明书实验数据显示该特征的变化会带来对技术效果的较大影响,使得本领域技术人员无法预期权利要求涵盖的所有技术方案均能够解决所要解决的技术问题,则该权利要求得不得说明书支持。
但是原研组合物专利没有被全部无效,仅部分被无效,且该无效审查决定也不是最终判决,专利权人和请求人还可以选择上诉,因此暂时还难以确定是否可以成功挑战原研专利。
根据《药品专利纠纷早期解决机制实施办法(试行)》,如果仿制药企业选择四类声明,而专利权人或者利害关系人对四类专利声明有异议的,可以自国家药品审评机构公开药品上市许可申请之日起45日内,就申请上市药品的相关技术方案是否落入相关专利权保护范围向人民法院提起诉讼或者向国务院专利行政部门请求行政裁决。收到人民法院立案或者国务院专利行政部门受理通知书副本后,国务院药品监督管理部门对化学仿制药注册申请设置9个月的等待期。猜测不管是4.1或4.2类声明,为了保护既有市场,原研肯定会让仿制药企业“享受”等待期。根据《药品专利纠纷早期解决机制实施办法(试行)》政策解读,未在中国上市药品专利信息登记平台登记相关专利信息的,不适用本办法,也即南京先声药业不会遭遇审评等待期,也不影响后续的行政审批。对此类未能早期解决专利纠纷的,相关药品获批上市后,如专利权人认为相关药品侵犯其相应专利权,引起纠纷的,依据《中华人民共和国专利法》等法律法规的规定解决。
等待期内不会停止技术审评。从仿制药的技术审评周期看,即使遭遇等待期,对后续技术审评影响也不大,主要是后续的行政审批。理论上如果选择不进行专利声明,不会遭遇等待期也不影响行政审批,当然也不能享受市场独占期,其批准时间将会加快。
但获得批准是一回事,能够正常上市销售又是另外一回事,究竟谁将占得先机尚未可知!
参考文献:
1.《药品专利纠纷早期解决机制实施办法(试行)》
2. 《药品专利纠纷早期解决机制实施办法(试行)》政策解读
3. 无效宣告请求审查决定书(第56057号)
想要解锁更多药物销售情况吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药物全国医院和药店年度及季度销售情况、销售药物排行、生产企业排行、ATC分类销售额占比等全局分析,可否投入仿制与研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论