
血友病是一组遗传性出血性疾病,因患者体内基因突变引起血液中凝血因子缺乏或失活,导致凝血功能障碍,即使是轻微的磕碰也会导致流血不止,因此这类患者被形象地称为“玻璃人”。患者通常被长期限制活动,甚至需要卧床,生活质量极差,往往终身具有创伤性出血倾向,重症患者即便没有明显外伤也可“自发性”出血。该病主要分为血友病A(凝血因子VIII缺乏)和血友病B(因子IX缺乏),血友病C(因子XI缺乏)最为罕见。2018年,血友病被收录进我国国家卫健委《第一批罕见病目录》。
当前,血友病主要通过输注重组或血源性凝血因子制剂来进行替代治疗,但终身治疗给患者带来极大负担,且可能会引起患者体内中和抗体(抑制剂)的产生,阻碍治疗的有效性,可见该领域存在极大的未满足需求。作为一种由基因突变导致的遗传性疾病,患者和业界都十分期待血友病能有“简便”或“一针治愈”的基因疗法,该病也成为了基因疗法开发最热门的赛道之一。
2022年6月24日,罕见病制药公司BioMarin(拜玛林制药公司)的血友病基因疗法Roctavian(Valoctocogene Roxaparvovec)获欧洲人用医药产品委员会(CHMP)积极意见,建议授予有条件上市许可(CMA),用于严重血友病A成人患者,欧盟委员会预计将于2022年第三季度做出通常与CHMP建议一致的最终批准决定。Valoctocogene Roxaparvovec可能是第一款在欧洲被推荐用于治疗血友病A的基因疗法,同时也意味着该疗法或将成为全球首款获批的血友病基因疗法,具有里程碑意义。
该疗法以腺相关病毒5型(AAV5)为载体,递送凝血因子VIII基因的功能性拷贝,从而使肝脏细胞可以持续表达因子VIII,以减少患者出血现象。药融圈旗下,药融云数据(https://www.pharnexcloud.com/?zmt-mhwz)显示,该项目最初源自伦敦大学学院(UCL)和StJude儿童研究医院,BioMarin于2013年获得研发权益。
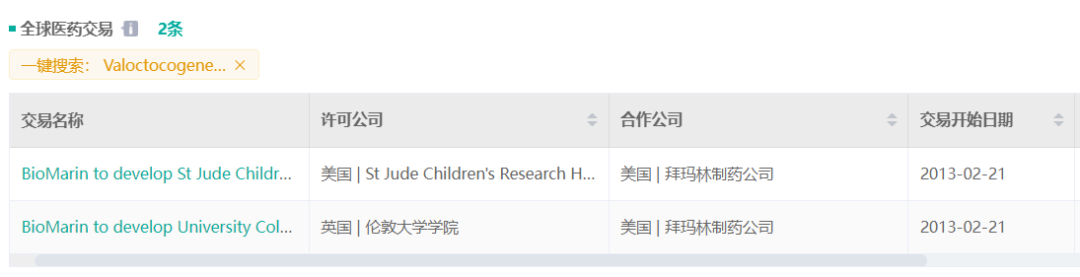
截图来源:药融云数据全球医药交易数据库
Valoctocogene Roxaparvovec在2016年被FDA授予孤儿药资格认定,2017年底被授予突破性治疗药物资格。虽然该药曾是全球首个进入监管审查的血友病基因疗法,但其审批之路并不顺利。BioMarin最初分别于2019年11月和12月向EMA和FDA提交了该疗法的上市申请,但在2020年8月遭FDA驳回,虽然当时的临床试验结果达到了预先指定的监管审评标准,但FDA出于耐久性问题的考虑,要求公司提供完整的2年随访数据以评估长期疗效,这也间接导致了BioMarin撤回了该疗法在欧洲的上市申请;2021年1月,BioMarin公布了积极的3期随访1年的数据,基于此,FDA在2021年3月授予其再生医学高级疗法(RMAT)认定;2022年1月,BioMarin公布了全球3期临床试验的2年随访安全性和有效性数据,主要和次要终点均已达到。
由于FDA的申报要求3期研究2年随访数据而EMA只要求1年,2021年6月,BioMarin率先向EMA重新提交了Valoctocogene Roxaparvovec的上市许可申请(MAA),CHMP此次积极意见基于Valoctocogene Roxaparvovec临床研究的全部数据,这是迄今为止血友病A基因疗法范围最广泛的研究,包括全球3期GENEr8-1试验的2年治疗结果,以及1/2期剂量爬坡研究中部分队列的5年和4年随访数据。然而,FDA方面在2022年5月要求BioMarin提供更多关于该疗法的数据和分析,因此该疗法在美国的监管意见最早也要等到明年,公司预计在2022年6月~9月之间重新向FDA提交BLA申请。

BioMarin Pharmaceutical 是一家针对慢性基因性疾病研发以酵素为基材的治疗药物的生物制药公司,专注于为那些严重、危及生命的罕见疾病患者开发变革性疗法,其开发工作主要针对重大未满足医疗需求,并有机会带来首个上市或比现有疗法显著更优的创新产品。BioMarin在1997年3月从Glyko Biomedical获得150万美元投资并开始运营,当时罕见病药物跟罕见病本身一样稀少,而现在其产品组合中已有7款商业化产品(大部分为酶替代疗法)以及多款处于临床或临床前开发阶段的候选产品。
BioMarin Pharmaceutical 公司基本信息
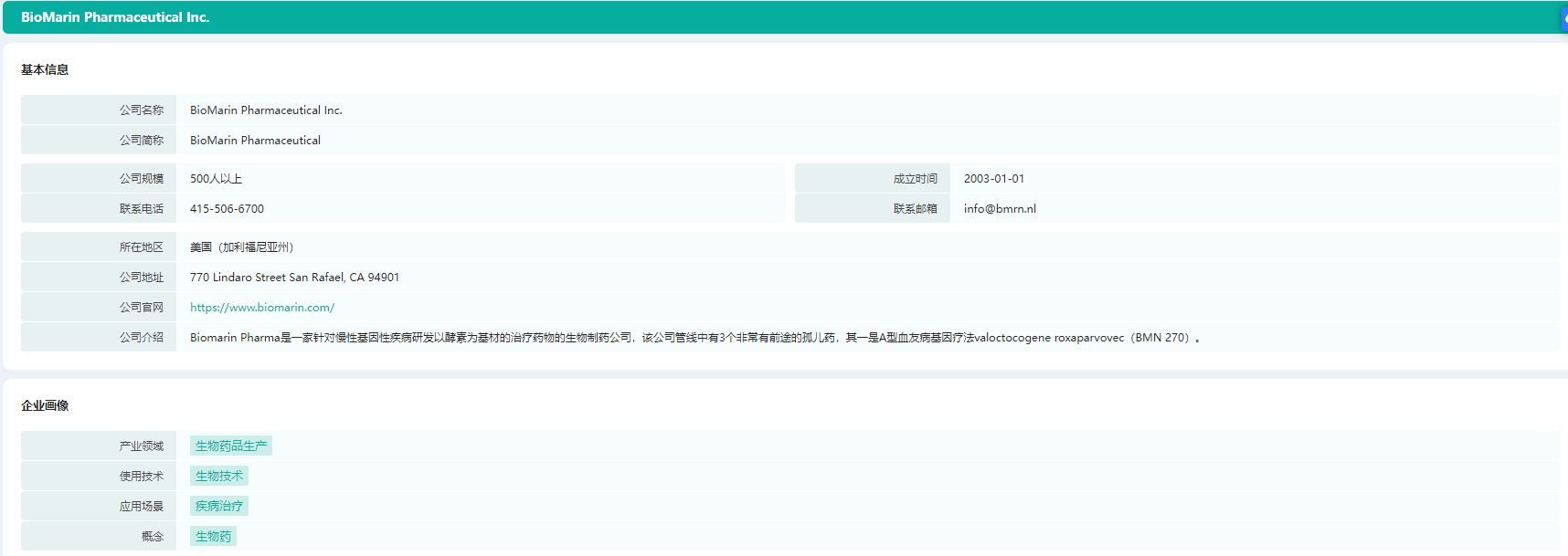
截图来源:药融云投融资数据库(新版)
商业化产品组合
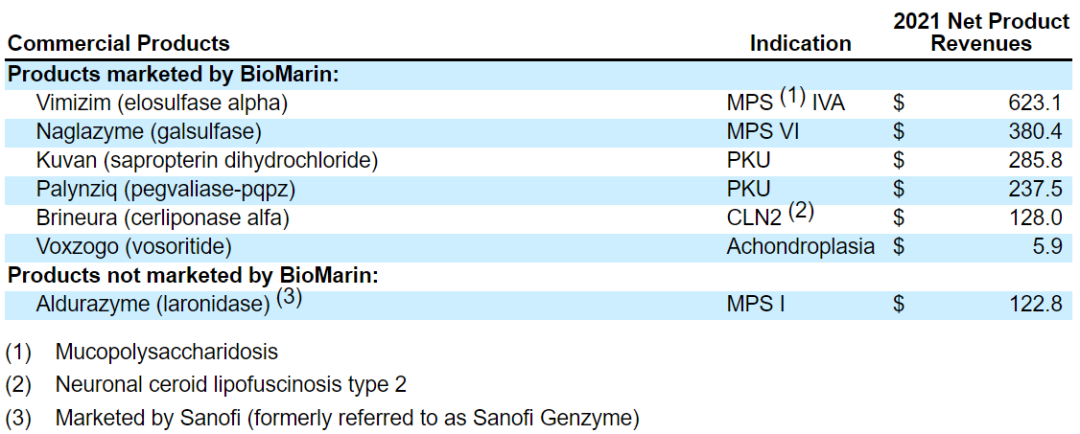
BioMarin Pharmaceutical已上市产品基本信息
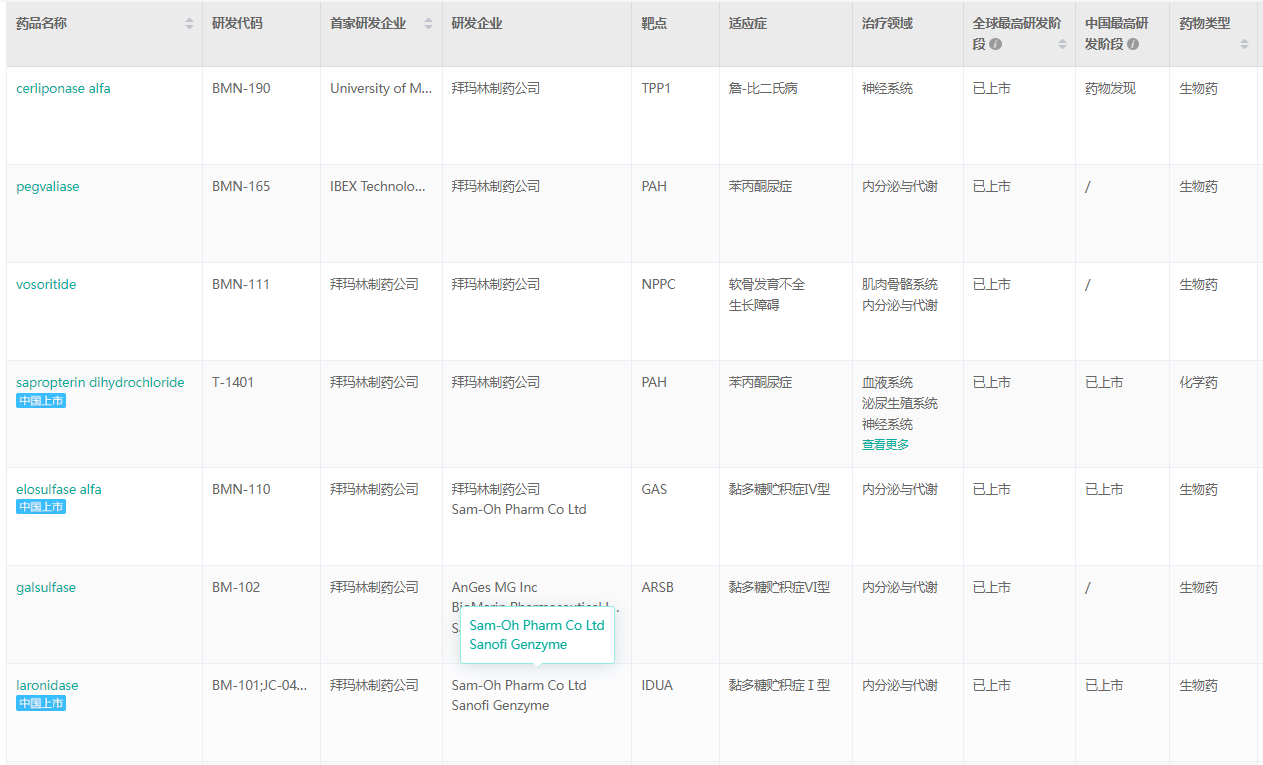
截图来源:药融云全球药物研发数据库
黏多糖贮积症(MPS)是一组罕见的遗传性溶酶体贮积症,由降解糖胺聚糖(GAG,或黏多糖)所需的溶酶体酶缺乏引起,导致一系列代谢紊乱。GAG是全身细胞外基质、关节液和结缔组织的重要组成部分,随着时间的推移,患者体内GAG大量堆积,造成永久性、进行性的细胞损伤,影响外观、身体器官和系统功能。所缺酶类型的不同导致该病有多种分型,且临床症状不同,疗法也不同。对于这组疾病,BioMarin目前有三款药物:
·Vimizim(elosulfase alpha,重组N-乙酰半乳糖胺-6-硫酸酯酶[rhGALNS])是一种酶替代疗法,用于治疗黏多糖贮积症IVA型(MPSIVA)。MPSIVA的特征是GALNS酶活性不足,引起糖胺聚糖(GAG)在溶酶体中大量堆积,会导致全身性骨骼发育不良、身材矮小和关节异常。Vimizim是FDA批准的首款治疗MPSIVA的疗法,已在美国、欧盟和其他国际市场上市。在国内,该药于2019年获批。
·Naglazyme(galsulfase)是一款重组N-乙酰半乳糖胺-4-硫酸酯酶(芳基硫酸酯酶B),用于治疗黏多糖贮积症VI型(MPSVI),已在美国、欧盟和其他国际市场获批上市。
·Aldurazyme(laronidase)是BioMarin第一个获批上市的药物,用于治疗黏多糖贮积症I型(MPSI),其本质是一款高度纯化的α-L-艾杜糖醛酸酶,已在美国、欧盟和其他国际市场获批上市。该药源于1998年BioMarin与健赞(现为赛诺菲的一部分)成立的合资公司,BioMarin与赛诺菲拥有50/50的权益。目前该药由BioMarin负责制造,并由赛诺菲进行销售,BioMarin将获得全球净销售额39.5%至50%不等的付款。
苯丙酮尿症(PKU)是一种遗传性氨基酸代谢疾病,由苯丙氨酸(Phe)代谢所需的苯丙氨酸羟化酶(PAH)缺乏而引起,使得苯丙氨酸在体内大量蓄积,并从尿中排出,导致严重的神经系统并发症,包括智力障碍和脑损伤、精神疾病、癫痫等。针对该病,公司目前有2款药物:
·Kuvan(sapropterin dihydrochloride,盐酸沙丙蝶呤)为天然6R-BH4(四氢生物喋呤)的合成口服制剂,6R-BH4是苯丙氨酸羟化酶(PAH)的天然辅助因子。该药最早于2007年12月被FDA批准用于苯丙酮尿症(PKU)或四氢生物蝶呤缺乏症(BH4D)引发的高苯丙氨酸血症(HPA)。该药是首个与饮食调整相结合的药物,用于降低PKU患者血液和大脑中的苯丙氨酸浓度,以防止PKU的破坏性影响。在国内,该药于2011年上市用于治疗四氢生物喋呤缺乏症引发的高苯丙氨酸血症,中文商品名科望。
·Palynziq(pegvaliase-pqpz)是一种聚乙二醇化重组苯丙氨酸解氨酶(PAL),通过皮下注射给药以降低血液中的苯丙氨酸浓度。该药是公司获批的第二款PKU治疗药物,在美国获批用于现有治疗效果不佳,血液Phe浓度超过600μmol/L的PKU成人患者,在欧盟和澳大利亚获批用于16岁及以上PKU患者。
·Brineura(cerliponase alfa)是一款重组人三肽基肽酶1(TPP1),用于治疗儿童2型神经元蜡样脂褐质沉积症(CLN2),一种超罕见疾病。该病由TPP1缺乏而引起,导致小儿神经退行性病变,无法治愈且快速进展,患者通常在10-12岁时死亡,据估计全球约有1200~1600例患者。Brineura是全球首款获批治疗此病的TPP1酶替代疗法,通过脑内注射给药,每两周注射一次,每次注射历时约4.5个小时。
·Voxzogo(vosoritide,伏索利肽)是一款C型利钠肽(CNP)类似物,每日注射一次用于治疗软骨发育不全症。该病是一种常染色体显性遗传疾病,是最常见的侏儒症,由成纤维细胞生长因子受体3(FGFR3)基因突变引起,导致参与调节骨骼生长的FGFR3和CNP信号通路之间不平衡。Voxzogo可作为FGFR3下游信号通路的正调节剂,促进软骨内骨生长。该药是全球首款靶向该病根本病因的药物,于2021年8月在欧盟率先获批,2021年11月在巴西获批,用于2岁及以上生长板开放的软骨发育不全症患者;2021年11月获FDA加速批准用于5岁及以上生长板开放的患者。同时FDA还授予BioMarin一张罕见儿科疾病优先审评券(PRV),以奖励该公司在罕见病新药研发方面做出的突出贡献,2022年2月,公司宣布已将该PRV以1.1亿美元出售,未披露购买方。2022年6月21日,BioMarin宣布日本厚生劳动省(MHLW)已批准Voxzogo用于治疗所有年龄段生长板未闭合的儿童软骨发育不全患者。
管线开发计划
BioMarin致力于围绕中心法则各个层面开发突破性药物,在公司创立之时,其核心科学模式在于酶替代疗法。现在BioMarin正关注分子医学的前沿,如研究腺相关病毒(AAV)基因疗法将短链DNA递送给细胞,利用其天然机制创建所需蛋白质,以解决遗传性疾病的根本原因。该公司主要关注具有明显遗传缺陷的罕见病或超罕见疾病,开发first--in-class或best-in-class疗法。
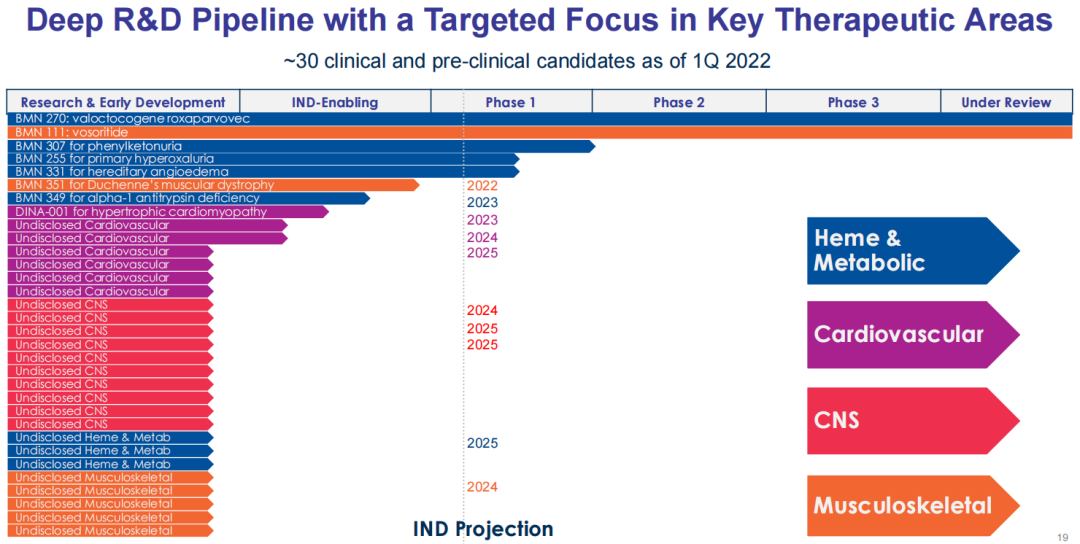
截至2022年第一季度,其管线中约有30款处于临床或临床前研究阶段的候选疗法,治疗领域包括血液与代谢疾病、心血管疾病、中枢神经系统疾病以及肌肉骨骼疾病,在研疗法类型包括基因治疗、多肽/生物制品、寡核苷酸疗法以及小分子药物。

针对Valoctocogene Roxaparvovec,除了正在进行的全球3期GENEr8-1试验以及1/2期剂量爬坡试验,BioMarin正在开展一项3b期单臂、开放标签试验以评估该疗法与预防性糖皮质激素联用治疗血友病A患者的疗效及安全性。另外,该公司对于体内预先存在AAV5抗体以及体内具有FVIII抑制剂的血友病A患者分别开展了一项1/2期研究。
针对已获批产品,BioMarin计划拓展Voxzogo(vosoritide,伏索利肽)的适应症,以获得更多市场机会。目前,公司正与美国国家儿童医院合作开展Voxzogo用于遗传性身材矮小患者的研究。此外,BioMarin还在探索该药用于婴幼儿枕骨大孔压迫,这类患者通常需要采取颈髓减压手术,目前正在一项2期临床试验中招募患者。
据药融云数据库显示,BMN307是一款在研的AAV5基因疗法,用于治疗苯丙酮尿症(PKU)的PAH靶向药物,旨在使PKU患者血液的苯丙氨酸(Phe)浓度水平正常化。该疗法已获FDA的孤儿药认定和FDA的EMA和快速通道资格。BioMarin在2020年9月开启了BMN307的1/2期PHEarless研究,但该试验在2021年9月被FDA叫停,原因是在临床前试验中观察到致癌性(肝肿瘤)。2022年2月,FDA要求公司提供更多非临床研究数据以评估该疗法的人体致癌风险,这可能需要几个季度的时间。
BMN307药物基本信息
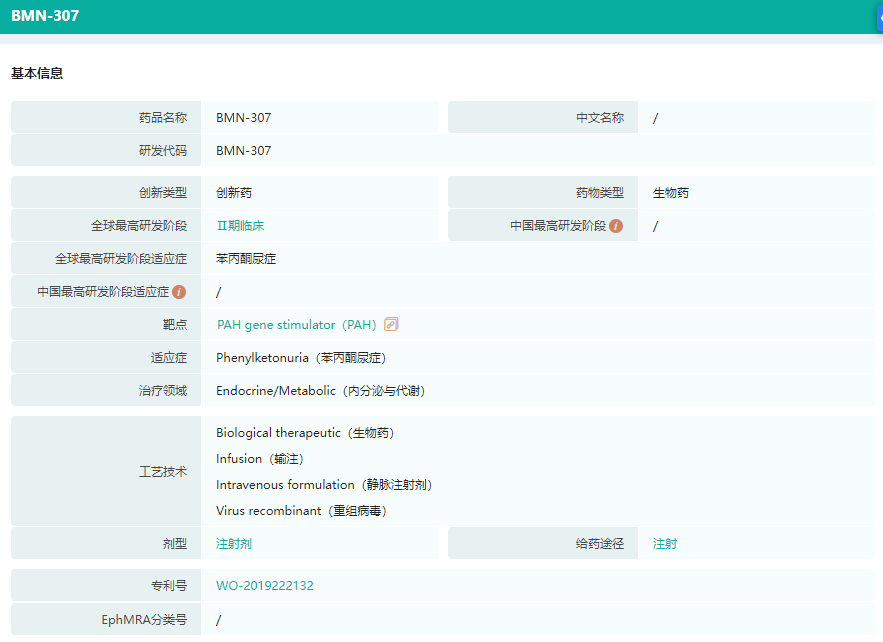
截图来源:药融云全球药物研发数据库(新版)
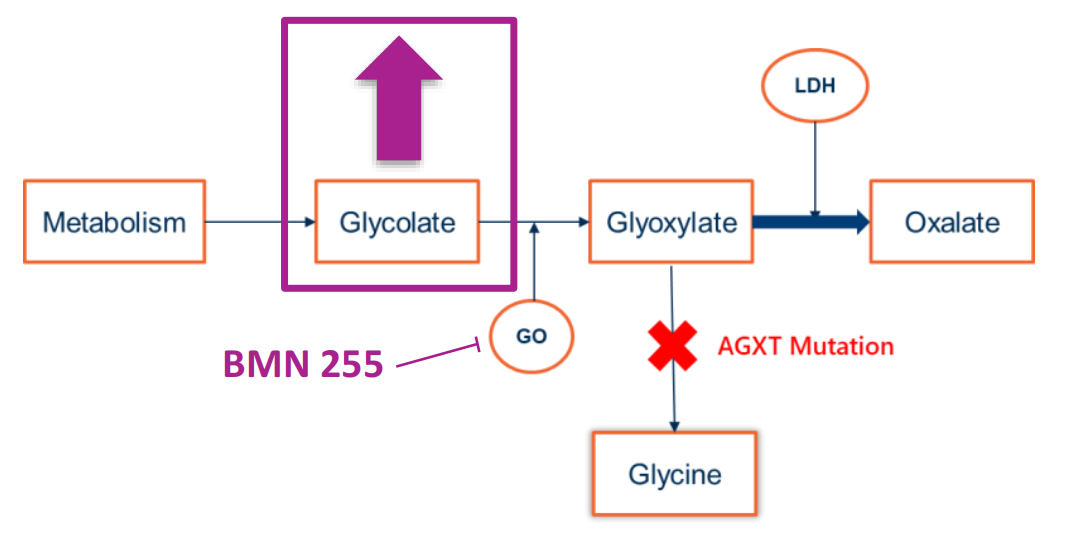
BMN255是一款小分子疗法,旨在治疗原发性高草酸尿症1型(PH1),该病是一种由AGXT致病突变导致的严重儿科罕见疾病,患者肾脏内草酸盐大量蓄积,引起肾脏损伤,并可导致多器官衰竭。BMN255的本质是一种口服生物可利用的乙醇酸氧化酶(GO)小分子抑制剂,旨在下调草酸的代谢合成,目前正在1/2临床研究中接受检验。
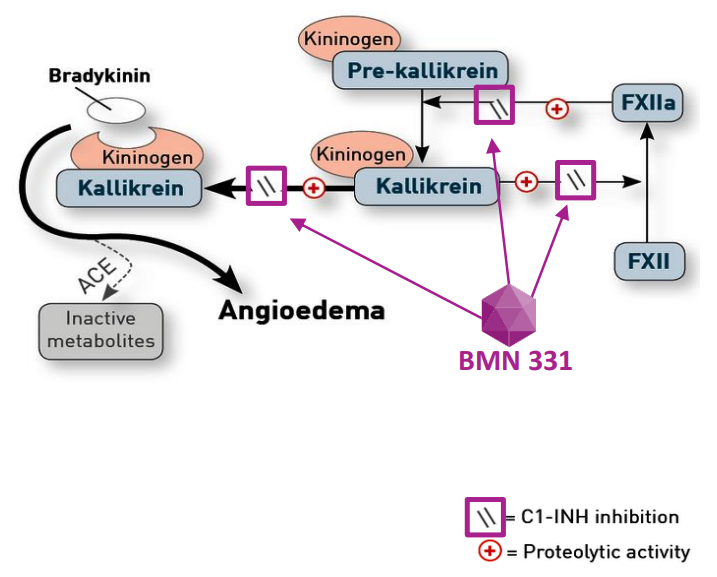
BMN331是一款治疗遗传性血管性水肿(HAE)的在研AAV5基因疗法。该病是一种常染色体显性遗传的罕见病,由SERPING1突变引起C1酯酶抑制因子(C1-INH)缺乏或功能障碍所致,患者血管性水肿反复发作,最常累及皮肤、肠道或上呼吸道。BMN331旨在启动C1-INH的天然表达,重建人体内C1-INH途径。临床前研究表明,BMN331引起C1-INH蛋白的结构性表达可降低疾病发作的频率和严重程度,并有望取代慢性治疗。该疗法在2021年获得FDA授予的孤儿药资格认定,并于2022年第一季度启动1/2期HAERMONY试验。
BMN349是一款在研的口服小分子药物,用于治疗α1-抗胰蛋白酶缺乏症,该病是由α1-抗胰蛋白酶(A1AT)缺乏引起的一种先天性代谢病,患者肝脏中A1AT蛋白累积,常导致新生儿肝炎,婴幼儿和成人的肝硬化、肝癌和肺气肿等。BMN349旨在下调A1AT蛋白在肝脏中的累积,小鼠模型显示,该疗法可减少肝脏中A1AT的累积,具有逆转肝脏损伤的潜力。公司预计将在2023年第三季度提交该疗法的IND申请。

BMN351是一款在研的反义寡核苷酸(ASO)药物,用于治疗杜氏肌营养不良(DMD),公司预计在2022年第二季度递交该疗法的IND申请。

DiNA-001是一款在研的基因治疗产品,用于MYBPC3相关肥厚性心肌病(HCM),这是一种罕见的遗传性心肌病变。该候选疗法来自2020年5月,BioMarin与基因疗法公司DiNAQOR达成的一项临床前合作和许可协议。公司预计2023年递交该疗法的IND申请。
除此之外,BioMarin还在2020年11月与AI制药新贵Deep Genomics建立了临床前合作关系,以使用Deep Genomics的人工智能药物发现平台(AI Workbench)来发现四种具有高度未满足需求的罕见病寡核苷酸候选疗法。
在中国,2021年12月,BioMarin与九天生物医药有限公司(Skyline Therapeutics)宣布达成一项为期数年的全球战略合作,共同研究和开发基于腺相关病毒(AAV)的新型基因疗法用于治疗遗传性心血管疾病。
财务状况
2021全年BioMarin总收入为18.463亿美元,同比减少1%,主要由于Kuvan(sapropterin dihydrochloride,盐酸沙丙蝶呤)在2020年10月专利到期,受仿制药竞争,该药2021年业绩同比减少38%,不过公司2021年总体收入稳定。随着Voxzogo(vosoritide,伏索利肽)分别在2021年第三季度和第四季度获EMA和FDA批准,商业销售工作也同时启动,这导致公司的销售、一般和行政费用增加,为7.594亿美元;公司全年研发支出6.288亿美元,与2020年持平;全年净亏损6408万美元。以下为BioMarin全年产品业绩分布:

2022年第一季度,BioMarin总收入达到创纪录的5.194亿美元,同比增长7%,主要得益于Voxzogo(vosoritide,伏索利肽)近2000万美元的业绩贡献。第一季度净收入达1.208亿美元。
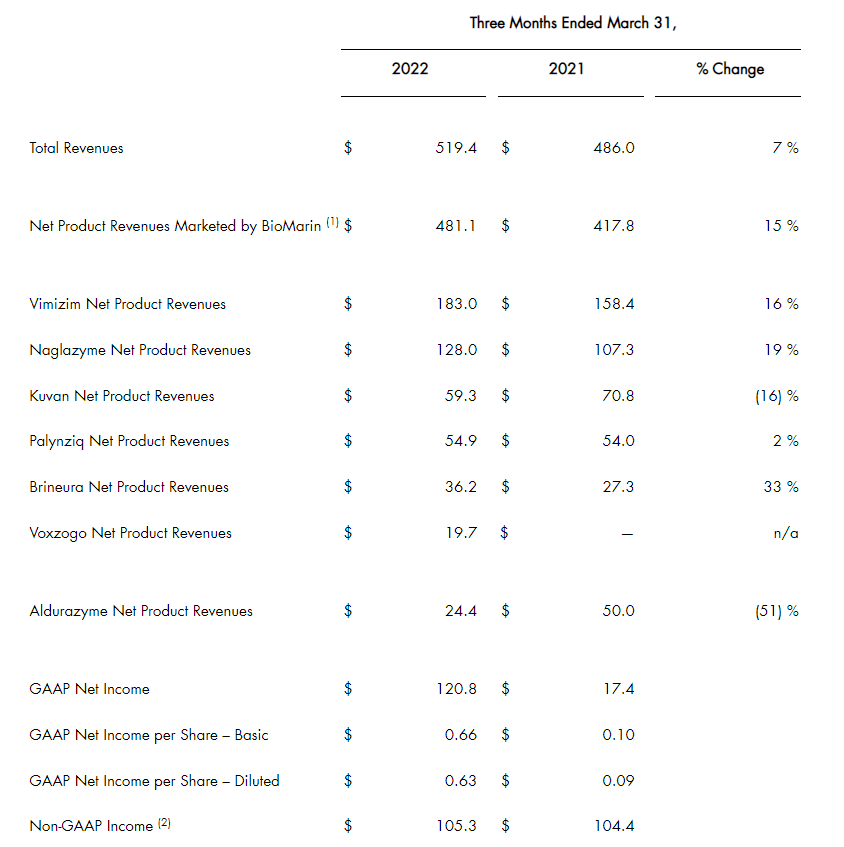
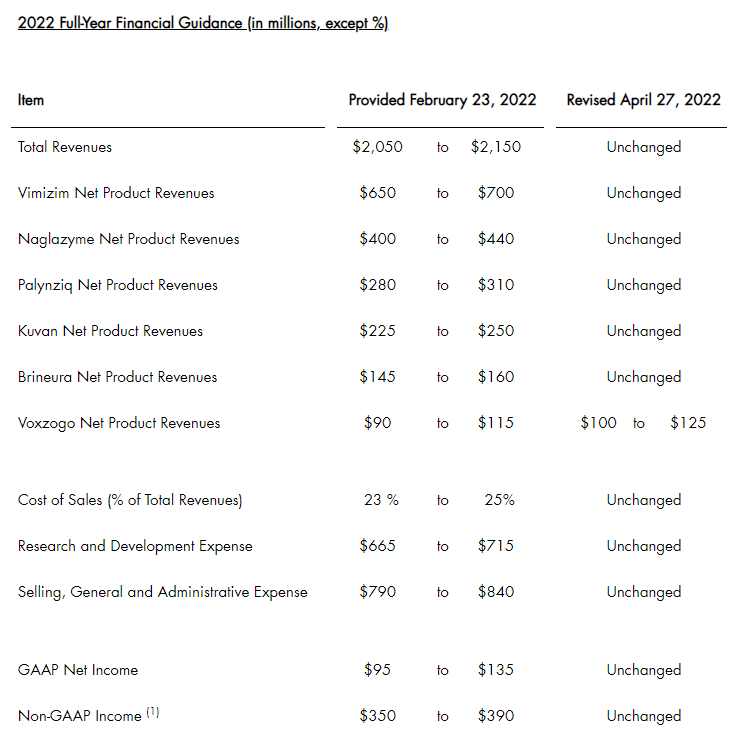
截至2022年3月31日,BioMarin的现金、现金等价物和投资总额为15.19亿美元。公司预计2022年将恢复两位数的收入增长和盈利能力,预测2022年总收入将达20.5~21.5亿美元,Voxzogo净产品收入预计将达到1~1.25亿美元。
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据库,https://www.pharnexcloud.com/?zmt-mhwz;
FDA/EMA/PMDA;
相关公司公开披露(正文图片除标注外,均来自企业官方);
https://www.biomarin.com/;
中华血液学杂志,《血友病治疗中国指南(2020年版)》;
https://investors.biomarin.com/2022-06-24-BioMarin-Receives-Positive-CHMP-Opinion-in-Europe-for-Valoctocogene-Roxaparvovec-Gene-Therapy-to-Treat-Adults-with-Severe-Hemophilia-A;
https://www.globenewswire.com/news-release/2016/03/01/816024/18475/en/BioMarin-Receives-Orphan-Drug-Designation-From-FDA-for-First-AAV-Factor-VIII-Gene-Therapy-BMN-270-for-Patients-With-Hemophilia-A.html;
https://www.fiercebiotech.com/biotech/fda-gets-out-its-red-pen-again-rejecting-biomarin-s-gene-therapy-valrox-amid-durability;
https://endpts.com/once-again-the-fda-is-putting-BioMarins-hemophilia-a-quest-on-hold-as-gene-therapy-frets-simmer/;等等。
想要解锁更多药企信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息;投融资情况;最新动态;产品管线布局、药物基本信息、研进展、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论