
5月份,关于阿尔茨海默病的重要资讯有:(1)美国FDA宣布允许用于早期发现与阿尔茨海默病相关的淀粉样蛋白斑块的首款体外诊断检测上市(2)卫材完成向FDA滚动提交阿尔茨海默新药lecanemab上市申请(3)绿谷制药原创治疗阿尔茨海默病新药九期一®(甘露特钠胶囊,代号:GV-971)的国际3期临床试验被传已经停止。
一场起始于暮年的战争
阿尔茨海默病(Alzheimer Disease,AD)作为目前最常见的老年期痴呆之一,是一种由于自身中枢神经系统变性所致的慢性神经退行性疾病。阿尔茨海默病(俗称“老年痴呆”)是一场起始于暮年的战争,临床上表现为记忆障碍、失语、失认、视空间技能损害、执行功能障碍以及人格和行为的改变,在这场战争中,人们几无胜算。
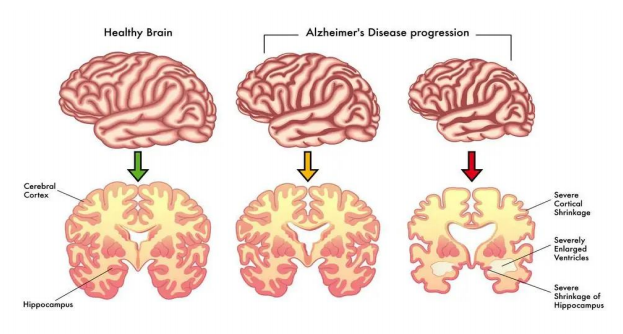
目前AD患者约占全部痴呆患者的60%-80%,已成为严重的社会问题。据统计,全球AD患者已超过5000万人,预计2050年将突破1.52亿人,其中65岁以上患者将达到1380万人。当前中国AD患者已超过1000万人,是新发病例全球增速最快的国家之一。
而治疗AD的成本负担与流行程度与日俱增,仅2020年美国AD患者的家人和朋友就提供了约153亿小时的无偿护理,相当于贡献了2570亿美元。到2050年预计总费用将达到 1.1兆亿美元(不包括上述无偿护理费用),患者、家庭、社会和医疗机构都面临着巨大压力。
致病机理仍未明确
阿尔茨海默病到底是如何发生的?科学家提出多种广为认可的AD发病机制假说,如Aβ级联假说、胆碱能假说、Tau蛋白异常磷酸化假说、神经炎症假说、金属离子紊乱假说等,但是其致病机理仍无法明确,目前该疾病仍无法治愈,成为医学界一大难题。
淀粉样蛋白假说图解
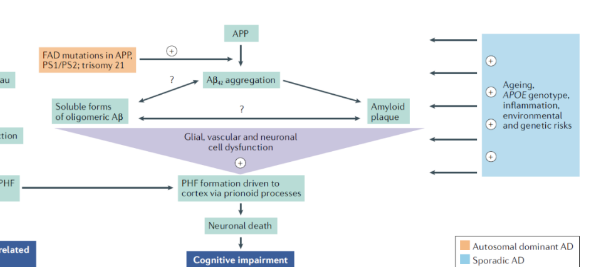
目前上市的抗AD药物包括4种,胆碱酯酶抑制剂、NMDA受体拮抗剂、Aβ抑制剂以及肠道菌群调节剂,这些药物可以通过抑制乙酰胆碱活性促进或恢复胆碱功能,对于初期和中期 AD患者起治疗作用,维持患者认知状态。
然而,在治疗效果上,这些药物也仅仅能延缓疾病进展以及改善症状,并不能够根治疾病,而且部分药物具有较为严重的副作用,如他克林具有肝毒性,卡巴拉汀有恶心、呕吐等胃肠道不良反应等,因此,该领域更有效的药物亟需开发。
极具争议的抗AD药物GV-971
近20年来,国内外药企在AD新药领域的研究几乎全军覆没,上市的药物基本只能延缓而无法有效治愈。直到2019年和2021年,才有新的药物获批,分别为Aducanumab和GV-971。
2019年11月2日我国上市了由中国海洋大学研发的抗AD药物GV-971(甘露特钠胶囊,商品名“九期一”),它是从海藻中获得的甘露寡糖二酸,是中国原创、全球首个靶向脑–肠轴的AD治疗新药,通过重塑肠道菌群平衡,从而改善认知功能障碍,应用于轻度至中度AD治疗。
GV-971基本信息

图片来源:药融云全球药物研发数据库
2020年4月,该药获批在美国进入临床试验。这款药物也一定程度上填补了市场的空白。GV-971的出现揭示了肠道菌群失调促进神经炎症在AD进展中的作用,提出了通过重塑肠道菌群平衡,抑制肠道菌群特定代谢产物的异常增多,减少外周及中枢炎症,降低Aβ沉积和 Tau蛋白过度磷酸化,为抗AD药物的研发提供新思路。
而事实上,过去一段时间里,GV-971这款新药一直伴随着学术界和业界的争议。鉴于AD疗法的紧缺性和病患的需求,国家药监局批准了GV-971的上市申请,但在这款药物上市后,仍然被要求继续进行药理机制方面的研究,继续进行长期安全性有效性研究,并完善寡糖的分析方法。如果后续数据不理想,可能意味着这款药物会被撤回。
而5月初GV-971的国际3期临床试验被传已经停止,此次被停止的3期国际多中心临床试验,旨在评估GV-971治疗轻中度阿尔茨海默病的疗效和安全性。业内有消息称,临床试验搁置可能存在新冠疫情的影响,或者是由于公司资金紧缺。但无论争议如何,GV-971上市并纳入医保已经成为事实,我们还是静观后续临床动态发展。
近二十年唯一批准上市的AD新药
2021年6月7日,渤健与卫材联合开发的Aducanumab(阿杜那单抗)获FDA批准上市,这是自2003年以来第一个获得美国FDA批准上市的新型阿尔茨海默病药物。它是一款基于β-淀粉样蛋白靶点研发的人类单克隆抗体,理论上能够有选择性地与AD患者大脑中的β-淀粉样蛋白沉积结合,然后通过激活免疫系统,将沉积蛋白清理出大脑。
阿杜那单抗作用机制
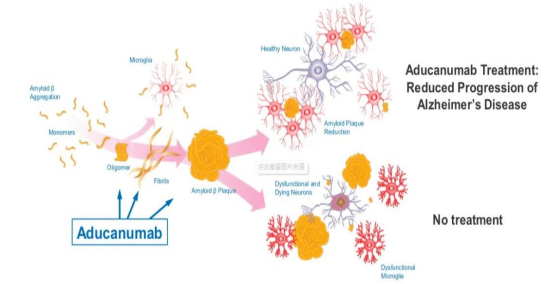
事实上,Aducanumab在临床试验中历经坎坷,FDA内部对于这一药物的审评意见也并不一致,2020年11月,专家委员会投票拒绝了Aducanumab的过批并对审批流程提出了批评。但考虑到疾病的严重性,病人的迫切需要等种种其他因素,最终FDA在不经过专家委员会讨论的情况下,使用快速审批通道过批了Aducanumab。
Aducanumab基本信息
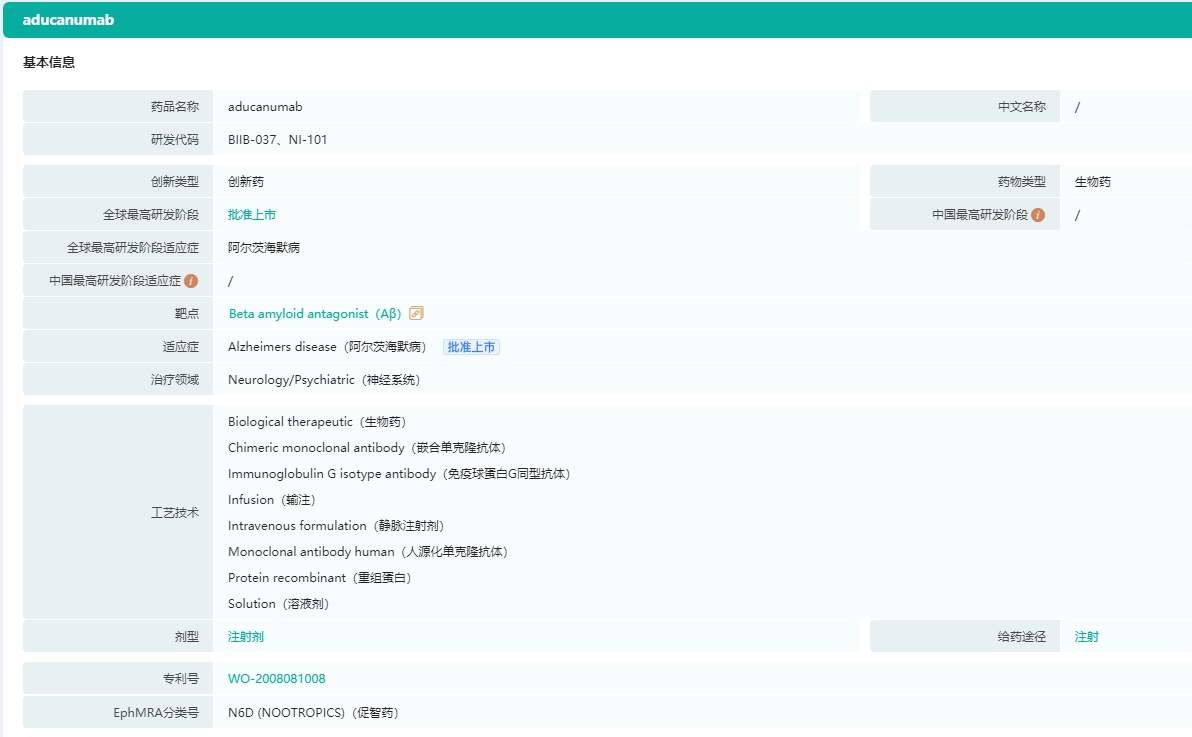
图片来源:药融云全球药物研发数据库
Biogen曾预测Aduhelm在获得FDA快速批准后将实现数十亿美元的销售额,但结果是这款曾被称作“将改变阿尔茨海默病的治疗方式”的药物在上市一年后仅仅被极少数患者使用,美国医疗保险和医疗补助服务中心(CMS)也不愿意为Aduhelm提供医保覆盖。
Biogen曾经试图为Aduhelm辩护以及采取降价至28,000 美元/年的措施,但到今年4月,持续恶化的局面让Biogen不得不下定决心抛弃Aduhelm。4月22日,Biogen宣布撤回 Aduhelm在欧洲的上市申请。
在与EMA人用药品委员会(CHMP)进行交流时,该机构指出迄今为止提供的数据不足以支持 EMA对aducanumab的上市许可给予积极意见。随后,主导Aduhelm项目的Biogen公司 CEO Michel Vounatsos离职,Aduhelm的营销团队也被解散。
全球AD药物研发现状
根据“创新药周期理论”,未来癌症如果得到控制,AD药物将是下一个医药大市场。
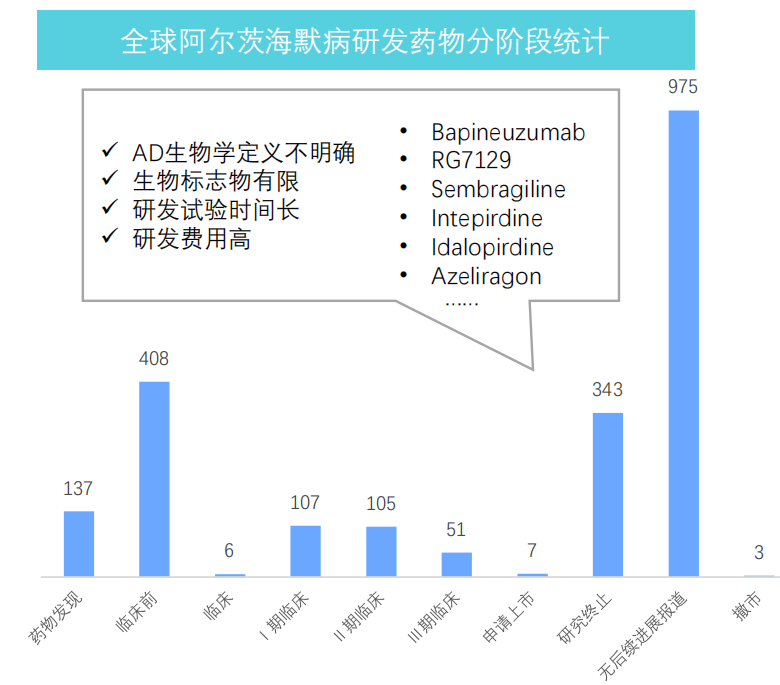
根据药融云数据统计,截至2022.05.25,全球共有2145个阿尔茨海默病研发药物(包括 active 和 inactive),其中IND以上研发阶段的药物占比仅为13%,包括临床Ⅰ期107个,临床Ⅱ期105个,临床Ⅲ期51个。
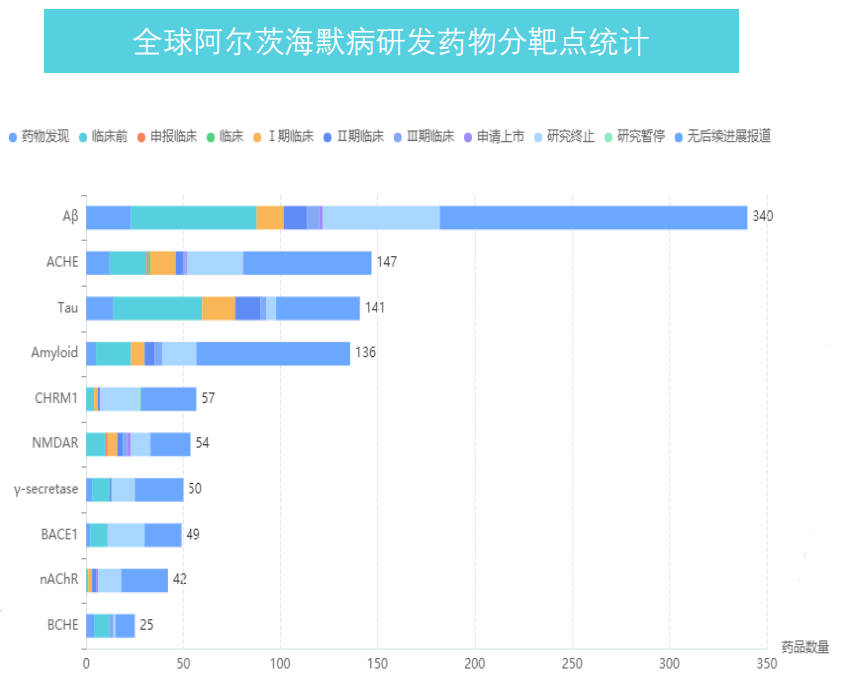
图片来源:药融云全球药物研发数据库
但值得一提的是,以上研发药物中,处于研究终止状态的药物共有343个,无后续进展报道的有975个,二者占比达到61.45%。
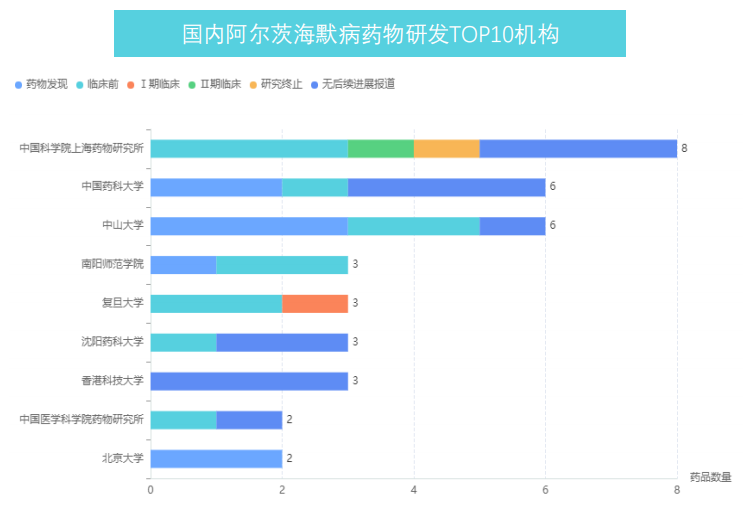
图片来源:药融云全球药物研发数据库
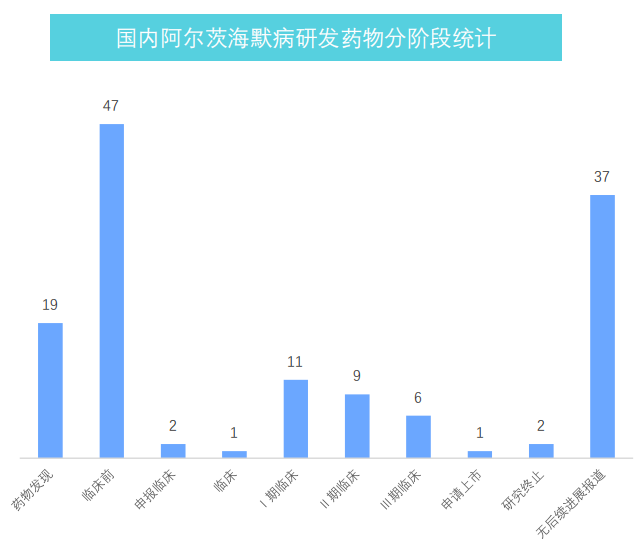
而目前国内阿尔茨海默病研发药物情况,处于临床前阶段的有66个,I期临床阶段的有11个,II、III期临床阶段的15个,申请上市的1个,研究终止以及无后续进展报道的有39个。
国内上市AD药物市场情况
目前全球批准用于AD治疗的药物包括:美金刚,卡巴拉汀,多奈哌齐,加兰他敏,及美金刚-多奈哌齐复方制剂五种,品种不多但占据了全球AD治疗药市场的八成以上。中国已批准用于治疗AD的药物主要有AChEI和NMDA受体拮抗剂、促智类辅助治疗药物、GV-971。
据药融云数据库显示,2019年国内公立医院抗痴呆药物市场规模为86.58亿元,市场规模呈逐年下降趋势。2019年,促智类药物在抗痴呆药物中市场规模占比82%,胆碱酯酶抑制剂占比12%,NMDA受体拮抗剂占比6%。
在国内抗AD一线治疗产品中,销售势头最猛的是多奈哌齐,在近年来经历了高速增长,2015-2019年间的平均复合销售增速超12%,且在2019年达到峰值,医院端销售额达到了7.62亿元;其次为盐酸美金刚和卡巴拉汀,近年也保持增长趋势,2020年医院端销售额盐酸美金刚达到41793.42万元,卡巴拉汀达到5993.64万元,市场优势比较明显。
多奈哌齐医院端市场销售趋势
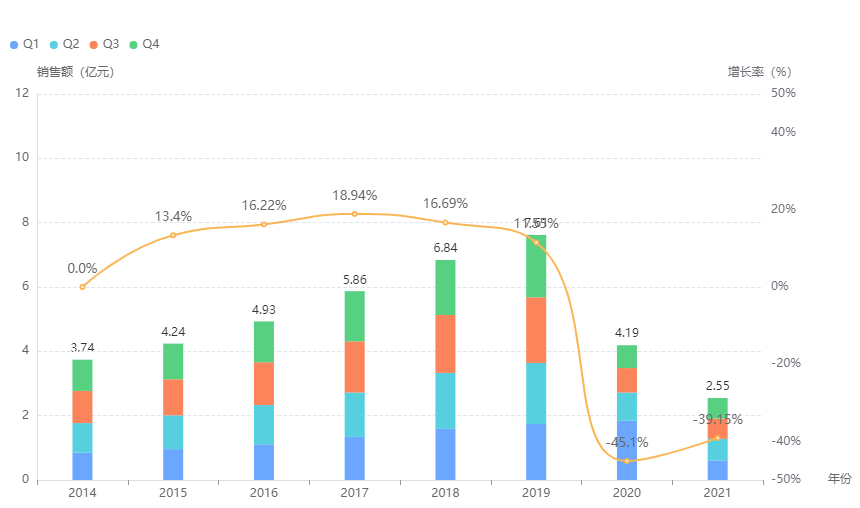
图片来源:药融云全国医院销售数据库
盐酸美金刚医院端市场销售趋势
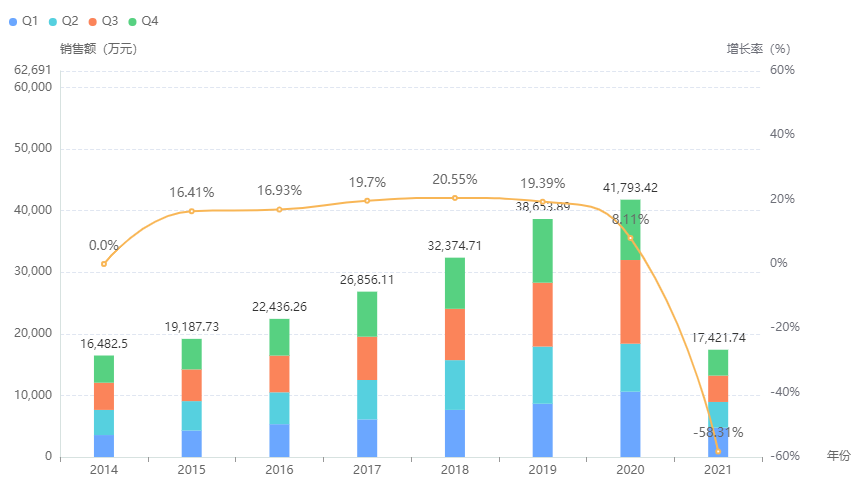
图片来源:药融云全国医院销售数据库
卡巴拉汀医院端市场销售趋势
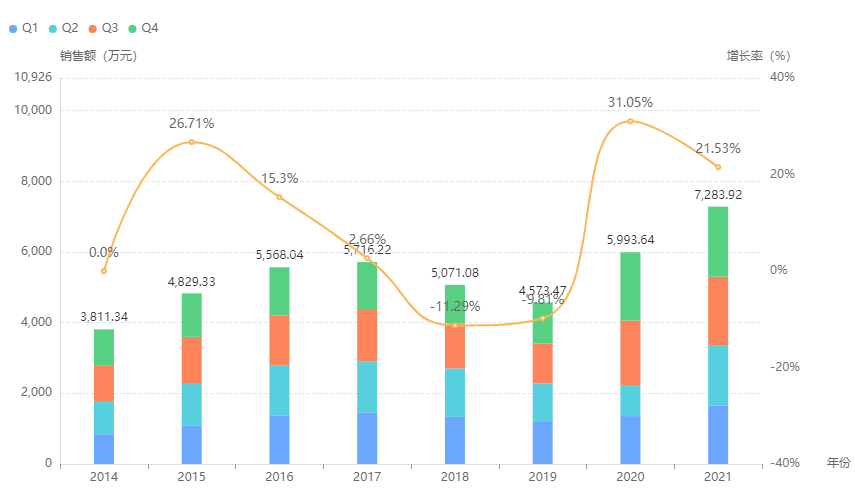
图片来源:药融云全国医院销售数据库
失败率高达99.6%,制药巨头纷纷“折戟”
针对治疗AD药物的研发领域,由于AD的生物学定义不明确、生物标志物有限,并且研发试验时间长、费用高等原因,大型药企频频受挫,对其打击重大。
世界上几家制药巨头公司已纷纷中止几项大型AD症Ⅲ期临床试验,例如美国辉瑞公司在 2018 年就宣布退出AD研发领域。
在全球医药界,AD药物的研发始终是一大难题。根据相关文献报道,肿瘤药物的失败率为 92%,而AD临床试验的失败率高达99.6%。本世纪以来,各大制药企业为AD市场投入了约2000多亿美元,但仅2018年至2019年初,就有8种药物因为疗效差或毒性高,Ⅲ期临床试验均宣布失败。
结语:
尽管道路曲折,但相信随着医学、生物学等基础研究的不断发展,随着研究者对高效生物标志物的发现、新发病机制的探究、新研发思路的探究,AD药物研发终将迎来胜利的曙光。(想要了解更多5月全球在研新药详细内容,关注“药融云”公众号(gh_d20f87bd52d9),后台回复关键词“报告”即可获取)
<END>
















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论