一、肝癌流行病学数据
全球肝癌新发病例数和死亡病例数分别排名第7和3位,男性比例高于女性。
2022年全球新增癌症病例数达到2,000万例,其中肝癌86.53万例,占比4.3%,排名第7位,男女肝癌患者例数分别为60.02万例和26.5万例。
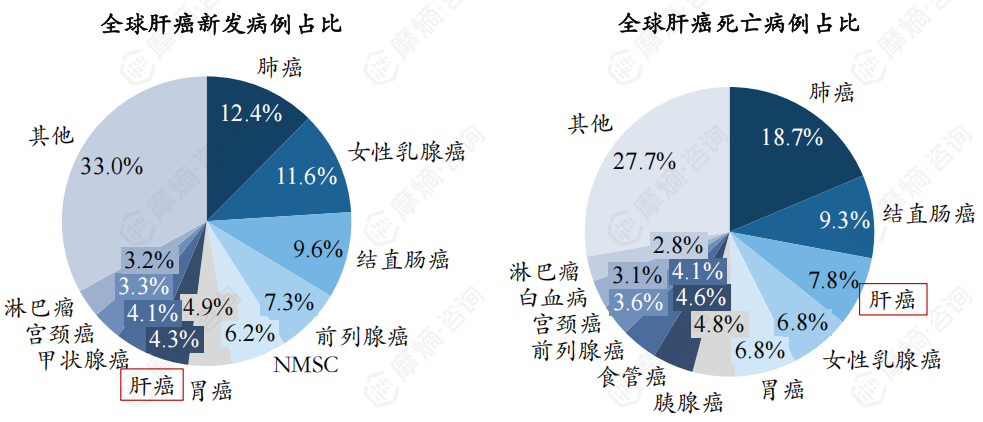
2022年全球癌症死亡病例共970万例,其中肝癌75.79万例,占比为7.8%,排名第3位。男女肝癌患者例数分别为52.14万例和23.65万例。
肝癌预后极差,发病率与死亡率之比达到 1:0.9。
中国肝癌新发病例数和死亡人数分别排名第4和2位,男性远高于女性。
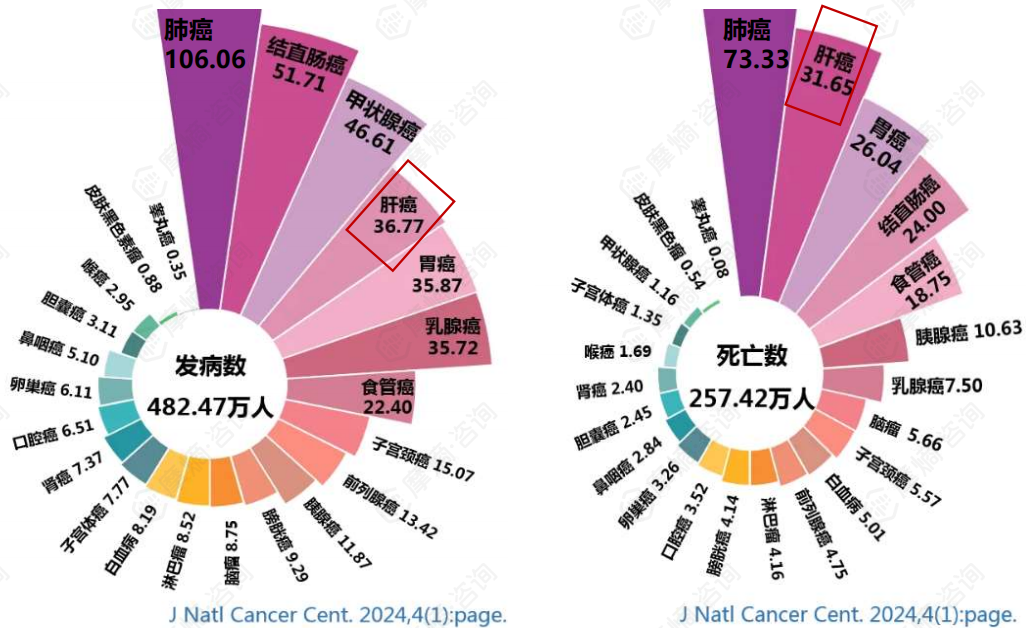
2022年我国癌症新发病例数情况:新发病例数482.47万,其中肝癌36.77万人,排名第4位;其中男女的发病人数分别为:26.79万人和9.98万人。
2022年我国癌症死亡情况:死亡总人数257.42万人,其中肝癌31.65万人,排名第2位。其中男女的死亡人数分别为:22.98万人和8.68万人。
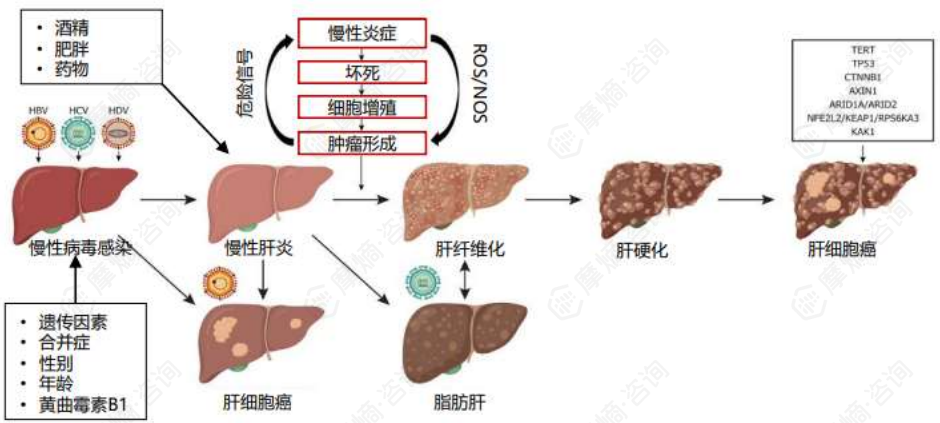
乙肝丙肝病毒感染是肝癌的主要诱因,持续服用抗病毒药物可显著降低肝癌发病率。
我国约90%的肝细胞癌患者中有HBV感染病史。肝炎病毒感染导致慢性肝炎,肝细胞表型发生变化逐步发展为肝硬化,此过程大概经历10-30年的时间,最后可能再发展至肝癌(患者也可能由慢性病毒感染直接发展至肝细胞癌)。其余诱因还包括酒精、肥胖、药物。
使用抗病毒药物(DAA)后,具有持续病毒学应答(SVR)的慢性丙型肝炎患者的肝癌发病率会显著降低。
二、肝癌诊疗指南及药物市场竞争格局分析
1. 晚期肝癌主要治疗药物为TKI靶向治疗和PD-1为主的免疫疗法
乙型肝炎病毒(HBV)和丙型肝炎病毒(HCV)感染是我国肝癌的常见危险因素,我国肝癌5年生存率仅为12.1%。前期主要以抗病毒治疗为主,符合要求的患者可进行肝切除术并加以术后辅助治疗。2024年版CSCO推荐晚期肝癌治疗药物以TKI靶向治疗和PD-1为主的免疫疗法。对于肝功能较好的患者一线治疗药物推荐多纳非尼、仑伐替尼和索拉非尼以及多个PD-1产品。
晚期肝癌的诊疗指南

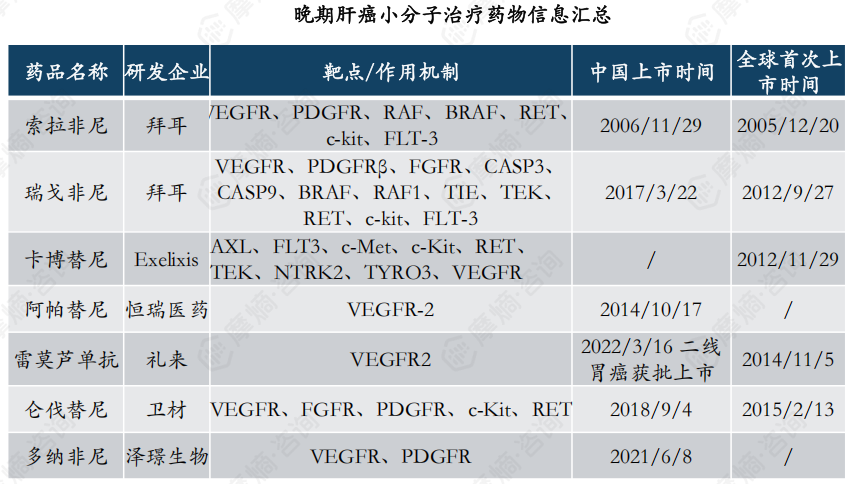
2. 肝癌小分子靶向药上市多年,尚无突破性药物补充
全球已获批上市的肝癌小分子靶向药中,索拉非尼最早2005年就在美国获批上市,为全球首款肝癌一线靶向药,但随着专利过期,新上市药物竞争加剧,2024上半年的市占率仅3.7%。
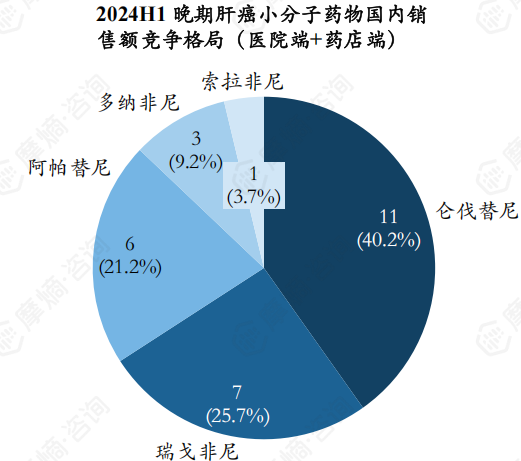
瑞戈非尼作为全球首款获批上市的肝癌二线用药,2024年12月在国内已纳入第10批国采,最高降幅91.86%,预计2025年销售总额将下滑。阿帕替尼凭借和卡瑞丽珠单抗联用,销售额虽下滑,但全年仍有望维持10亿元。多纳非尼为泽璟制药原研的氘代化合物,仍处于上市放量期。
3. 全球首个肝癌一线靶向疗法,专利悬崖2024上半年国内销售额仅1亿元
全球首个批准用于无法手术或远处转移的肝细胞癌的一线治疗,由拜耳研发,2005年获FDA批准上市,2006年获得中国药监局批准进入中国市场。还批准用于晚期肾癌和分化型甲状腺癌。
索拉非尼通过抑制RAF/MEK/ERK信号传导通路,直接抑制肿瘤生长;通过抑制VEGFR和PDGFR而阻断肿瘤新生血管的形成,间接抑制肿瘤细胞的生长。
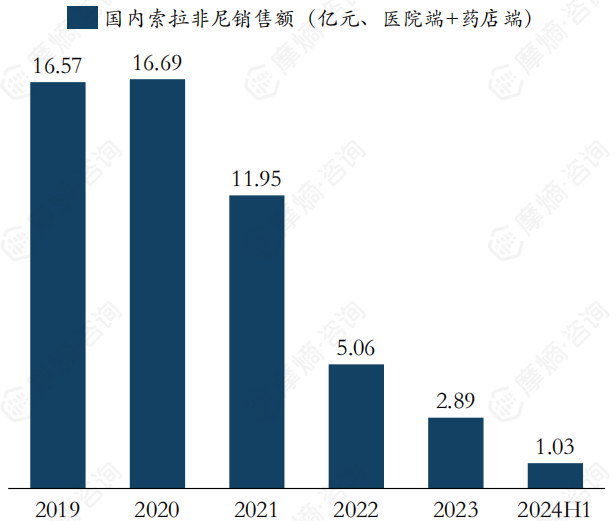
索拉非尼被纳入2017版国家医保目录,随后快速放量,并于2020年达到销售额峰值16.69亿元,后随着专利到期,竞品增加,销售额逐年下滑,2024年上半年仅剩1亿元的销售额。
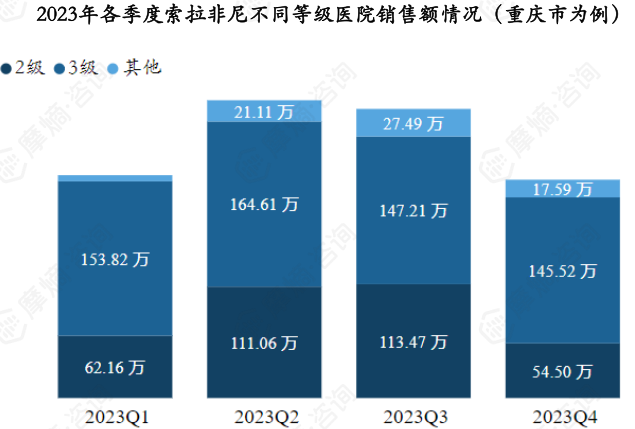
4. 索拉非尼各级医院市场分析(以重庆市为例)
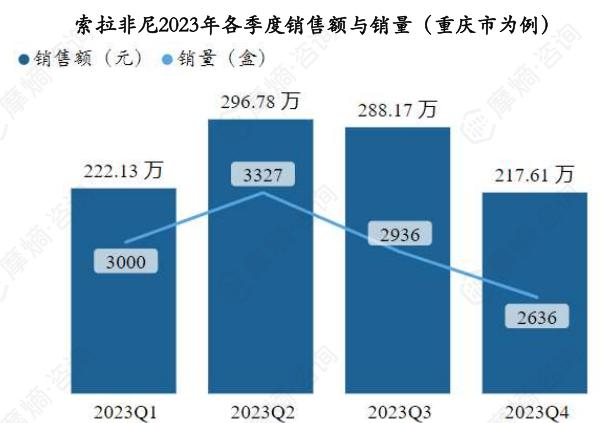
据摩熵医药药物流向数据显示,以重庆市为例,索拉非尼2023年各季度销售量和销售额如下图:
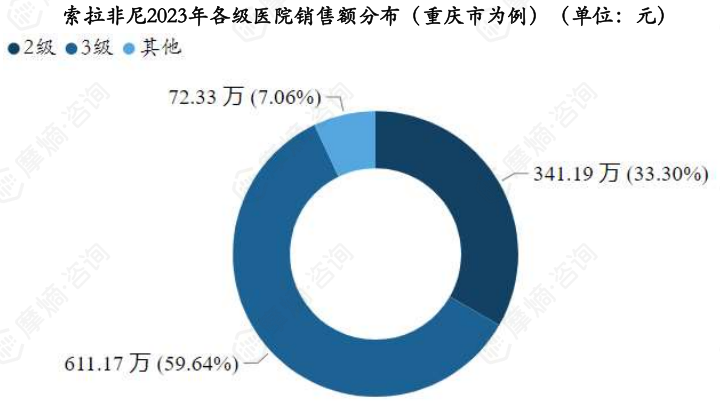
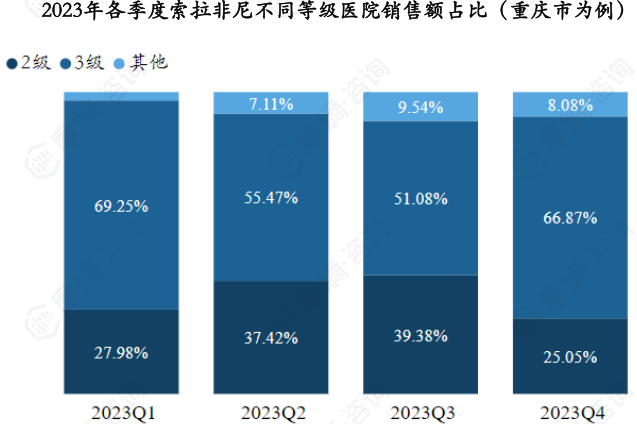
索拉非尼2023年各级医院(重庆市为例)销售额分布如下图,其中三级医院销售额占比接近总销售额的60%。
据摩熵医药药物流向数据显示,以重庆市为例,索拉非尼2023年销售市场主要分布在二、三级医院,各季度三级医院销售额占比达到50%-70%,其他医院销售额占比不足10%。
5. 瑞戈非尼超10亿品种,第10批集采后竞争格局生变
瑞戈非尼片是新一代口服多靶点磷酸激酶抑制剂,由拜耳研发,最早2012年9月获得美国FDA批准上市,用于治疗接受过多种化疗方案的转移性结直肠癌患者。2013年2月,FDA批准其用于二线胃肠道间质瘤,2017年4月, FDA批准用于二线肝癌。
2017年3月,瑞戈非尼首次在中国上市,并于同年12月获批用于既往接受过索拉非尼治疗的肝癌患者,这也是中国首个获批用于肝癌二线治疗的新药。2018年瑞戈非尼降价45.56%进入医保,降价后价格为196元(40mg/片),肝癌、结直肠癌、胃肠道间质瘤3个适应症均纳入国家医保。2019年国内销售额突破5亿元,随后也快速放量,2021年突破10亿元,2023年和2024年也都维持在14亿元左右。
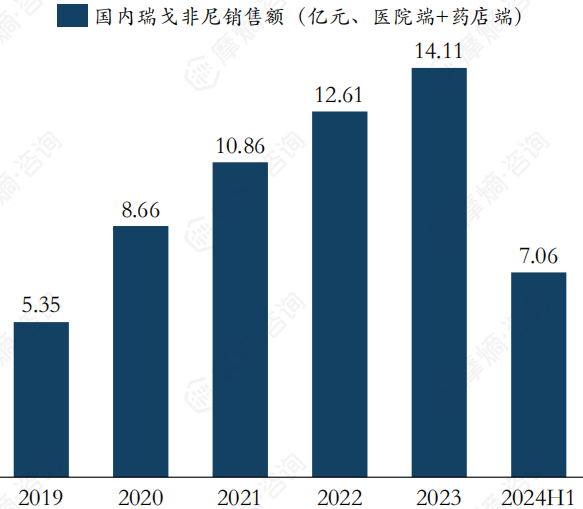
瑞戈非尼在中国的化合物专利于2024年7月到期,已经有9家企业过评,2024年12月第十批国采,共有6家企业中标(创诺制药、正大天晴、扬子江、科睿药业、齐鲁制药、科伦制药),最低价为创诺制药的118元/瓶(40mg*28片),单片价格仅4.21元,降幅91.86%。
第10批集采预计2025年4月开始执行,原研企业拜耳并未纳入集采,随着集采落地及众多仿制药的上市,竞争会愈加剧烈,拜耳的份额将被蚕食。
6. 阿帕替尼+卡瑞丽珠单抗作为一线肝癌疗法,美国上市可期
阿帕替尼是一种新型小分子TKI(酪氨酸激酶抑制剂),能够高度选择性竞争细胞内VEGFR-2的ATP结合位点,阻断下游信号转导,抑制肿瘤血管生成,由恒瑞医药研发。
2014年首次在国内获批上市,用于既往至少接受过两种系统化疗后进展或复发的晚期胃腺癌或胃-食管结合部腺癌。2020年批准用于晚期HCC的二线治疗,单药用于既往接受过至少一线系统性抗肿瘤治疗后失败或不可耐受的晚期肝癌患者。2024版CSCO指南推荐卡瑞利珠单抗联合阿帕替尼可作为一线疗法。
2019年达到销售额峰值27.63亿元,随着竞争愈发激烈,销售额逐年下滑,2024年上半年销售额为5.84亿元。
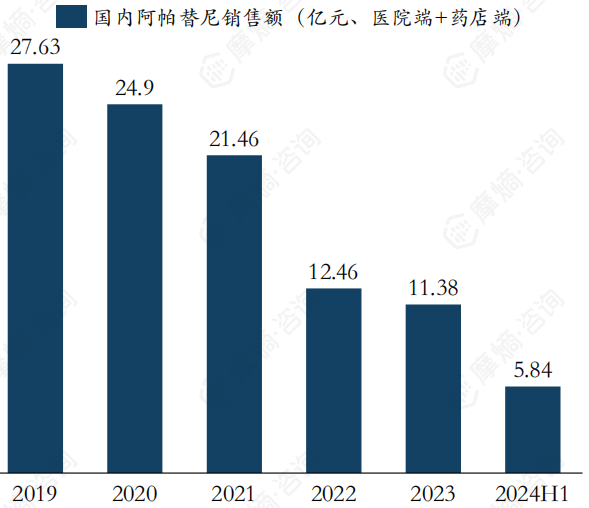
2024年10月,注射用卡瑞利珠单抗联合甲磺酸阿帕替尼片用于不可切除或转移性肝细胞癌患者的一线治疗的生物制品许可申请(BLA)获得美国FDA受理。FDA对注射用卡瑞利珠单抗的PDUFA日期为2025年3月23日。
7. 仑伐替尼全球第二款肝癌一线疗法,销售额峰值曾达28亿元
仑伐替尼(lenvatinib)是一种口服多种激酶抑制剂,可以选择性抑制多种激酶的活性,包括血管内皮生长因子受体(VEGFR1、VEGFR2和VEGFR3),以及成纤维细胞生长因子受体(FGFR1、FGFR2、FGFR3和FGFR4),此外还有致病性血管生成、肿瘤生长和癌症进展相关受体酪氨酸激酶,如血小板衍生生长因子受体α(PDGFRα)、KIT和RET。
该药由卫材药业研发,2018年获FDA批准用于晚期HCC系统治疗,是继索拉非尼之后十多年来首次获批用于晚期HCC一线治疗的新药,同年也在中国获批上市。
仑伐替尼作为单药,已经在日本、美国、欧洲、中国等国家和地区获批用于一线治疗甲状腺癌和肝细胞癌,在日本也被批准用于治疗胸腺癌。仑伐替尼与依维莫司联合疗法已经在美国、欧洲和亚洲等地被批准用于二线治疗肾细胞癌;与抗PD-1单抗帕博利珠单抗组成的联合疗法已经在多地获批用于一线治疗肾细胞癌、既往经过全身治疗的子宫内膜癌等。
仑伐替尼在2020年首次纳入医保,2021年放量明显,全年销售额达16.56亿元,并在2022年达到销售额峰值近28亿元,2023年和2024上半年由于竞争加剧,销售额有下降趋势。
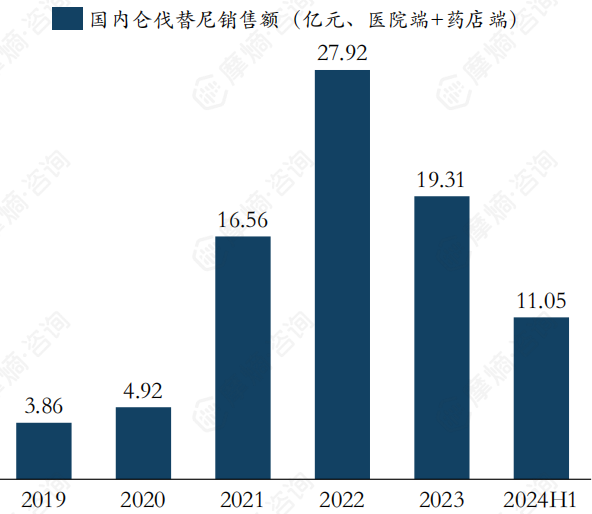
8. 国产创新药多纳非尼放量正当时
多纳非尼是一种新型口服多激酶抑制剂,既可通过抑制VEGFR和血小板源性生长因子受体(PDGFR)等多种酪氨酸激酶受体的活性,阻断肿瘤血管生成,又可通过阻断丝氨酸-苏氨酸激酶(RAS/RAF/MEK/ERK)信号传导通路直接抑制肿瘤细胞增殖,从而发挥双重抑制、多靶点阻断的抗肿瘤作用。
多纳非尼是索拉菲尼的一种氘代化合物,理论上其作用机制与索拉非尼相同,为多激酶抑制剂,临床试验结果显示多纳非尼和索拉非尼两组的中位 PFS 相似,但多纳非尼组具有良好的安全性和耐受性。
该药由泽璟制药原研,2021年被我国药监局获批用于没接受过全身治疗的不可切除肝癌的一线治疗。还批准用于放射性碘难治性分化型甲状腺癌。在2022年底纳入医保后,2023年快速放量,全年销售额达到4.26亿元,2024年上半年已突破2.52亿元。
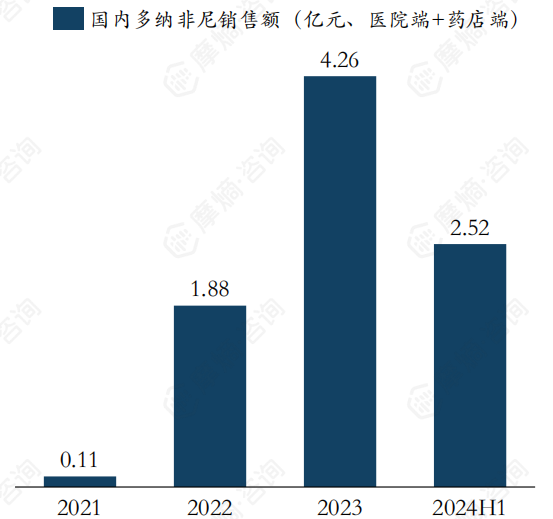
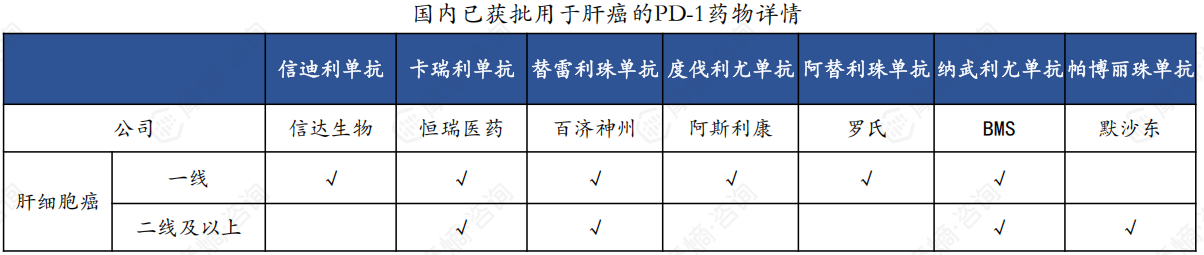
9. 多个PD-(L)1联用方案成为CSCO一线推荐用药
国内多个PD-(L)1获批上市用于肝癌一二线疗法,且CSCO指南中多推荐PD-(L)1联用方案作为一线推荐用药:
阿替利珠单抗(Tecentriq,PD-L1)+贝伐珠单抗(Avastin,VEGF):2020年5月,FDA批准“T+A”方案用于肝癌一线治疗,同年10月获得NMPA批准,临床研究结果显示,T+A方案组的mOS达到了19.2个月,大幅优于索拉非尼组为13.4个月。贝伐珠单抗被纳入2022医保目录但阿替利珠单抗尚未进入医保。
度伐利尤单抗(PD-L1)+替西木单抗(CTLA-4)双免疫联合疗法,临床试验结果显示mOS达到了16.4个月,优于索拉非尼组的13.8个月。
卡瑞利珠单抗( PD-1 )+阿帕替尼( VEGFR-2 小分子)是恒瑞医药的“双艾组合”,其对比索拉非尼用于治疗晚期不可切除肝细胞癌的全球多中心III期临床研究结果显示mOS达到了22.1个月,优于索拉非尼15.2个月。
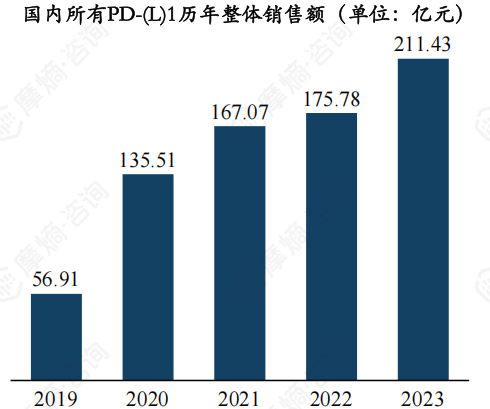
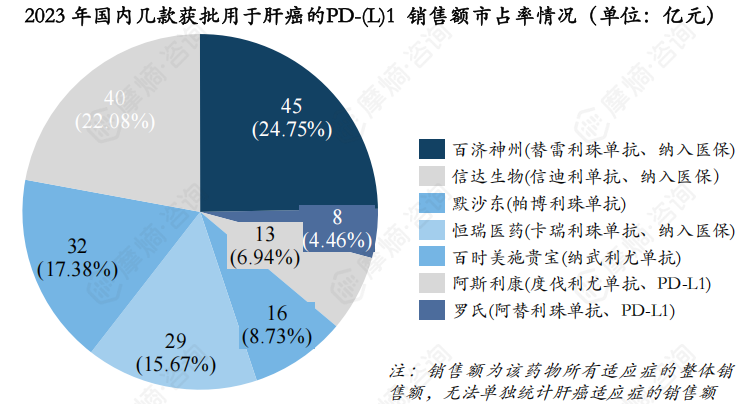
10. PD-(L)1国内整体销售额突破210亿元,百济神州和信达生物名列前茅
自2018年首款PD-(L)1在国内上市以来,截止目前已有15款PD-(L)1相继获批上市,销售额一路高歌猛进,从2019年57亿元增长至2023年211亿元。主要原因在于:
(1)显著的临床疗效;
(2)广泛的适应症范围,肺癌、肝癌、胃癌、黑色素瘤等多种肿瘤适应症都已获批上市。
从2023年国内销售额竞争格局来看(仅统计获批用于肝癌的几款PD-(L)1),百济神州的替雷利珠单抗以45亿元的销售成绩市占率第一(24.75%),信达生物的信迪利单抗以40亿元的销售额排名第二,市占率为22%,排名第三的为默沙东的帕博利珠单抗,32亿元(17%),未纳入医保能有这么好的成绩在于帕博利珠单抗先发优势,广泛获批的适应症和默沙东超强的销售能力。
三、肝癌药物市场趋势分析
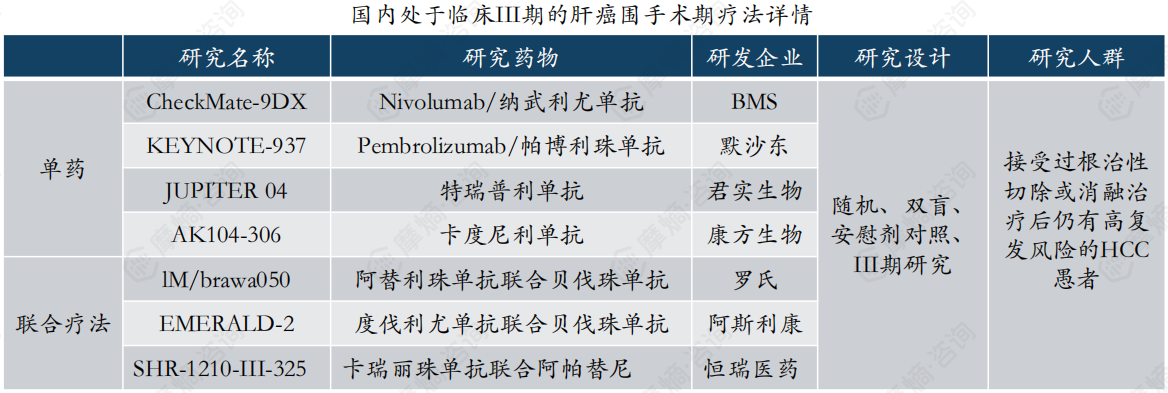
肝癌术后复发率高,多个药物围手术期疗法均处于临床III期。
肝癌手术切除率偏低和术后极高的复发率是当前早期肝癌临床治疗中面对的重大难题,亟需有效的围手术期方案。
目前多个药物围手术期III期研究正在进行中,包括君实生物特瑞普利单抗,其联合贝伐珠单抗用于不可切除或转移性肝细胞癌(HCC)患者一线治疗的上市申请已于2024年7月获CDE受理。
康方生物的卡度尼利单抗,为PD-1/CTLA4双抗,其用于二线宫颈癌、一线胃癌适应症均已获批上市,用于一线肝癌和肝癌围手术期疗法均在临床III期阶段。
以上内容均来自摩熵咨询{肝癌药物市场研究专题报告},如需查看或下载完整版报告,可点击!
想要解锁更多药品信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论