一、全球生物制药蓬勃发展
全球医药制药的蓬勃发展,中国创新药企不断出现,全球疫情持续紧张形势下;由于小型创新药企研发投入和pipeline(研发管线)占比提升,以及药企对于提升研发回报的需要,外包服务率也在不断上涨。
据悉,目前全球范围内生物药相关的产能,尤其是无菌制剂产能面临短缺。各类生物药CDMO迅速提升自身原液和无菌制剂产能,以满足激增的不同申报/临床阶段以及商业化生产阶段的客户需求。
BioProcess International 近期发表文章数据显示,自2018年以来,全球生物制药原液总产能从1650万L增长到了目前的1740万L。

▲2018至2021全球产能(按服务功能区分)趋势
在目前的1740万L的总产能中,有550万L (31.7%)位于美国和加拿大,546万L (31.4%)位于西欧,220万L (12.5%) 位于日本以及其它亚太地区,180万L位于中国 (2018年统计数据为87万升),110万L位于印度 (2018年为94.1万L)。(注:该数据中产能覆盖范围包括生产治疗性蛋白、单克隆抗体、ADC、疫苗、酶、培养的细胞产品和其它生物药品 (人和动物) 以及血液来源的细胞和血浆蛋白产品的工厂。)由于外需转移和内需强劲,中国的产能布局还在逐年扩大。

▲全球生物制药产能区域分布
成品(Drug Product,DP)灌装产能方面,作为制药行业外包最多的服务之一,一方面初创公司缺乏设备产能以及“轻资产”运营模式,会选择将这一部分生产外包出去;另一方面一些制药企业,为了保障市场供应的稳定、更好的匹配规模与需求,往往会选择将部分的DP工作外包,同时,当一家企业有新剂型的产品后,会选择将DP外包给拥有多种(如冻干、预充针、卡式瓶等)灌装产线的企业以加速推进开发进程;当新型疗法需要专门的生产线持续供应时,公司往往会选择外包这种极具成本效益的形式。因此随着药物剂型的增多,使得更多的服务外包企业在增加产能的同时,也不断的扩充着针对不同药物剂型的设备以增加对这一细分领域的布局。
同时,新冠疫情仍在全球蔓延,部分国家和地区出现新冠疫情局部反弹现象,且变异新冠病毒带来更多的不确定性,全球疫苗接种工作进入“加速期”。新冠疫情爆发后,国内疫苗厂企业积极扩产能,目前预计国产新冠疫苗年产能达88亿剂,其中部分为原有产能,预计新建产能需求在64亿剂。制剂灌装生产需求量激增,海外创新药企则通过外包/合作努力提高产能(如BioNTech与辉瑞/ Siegfried、强生与默沙东/ Emergent BioSolutions、阿斯利康/牛津与印度血清研究所/ Anagni、俄罗斯Sputnik V 新冠疫苗与韩国的GL Rapha/ 印度的Hetero、Novavax与Fujifilm Diosynth)。
二、中国生物制药CDMO崛起代表
作为国内产能扩增的代表,药明生物是非常典型的一家生物药CDMO。面对疫情之下的生物药需求激增,药明生物全球战略凸显,加大国内外产能布局。其中,药明生物在中国本土分别收购了辉瑞中国位于杭州的生产基地与位于苏州的苏桥生物超过90%的股份,这两次动作将迅速提升药明生物原液和制剂产能以及人才储备。药明生物将新增生物药制剂九厂(DP9,西林瓶)、制剂十厂(DP10,预充针)、制剂十一厂(DP11,液体和冻干)。

同样近年来发展增速迅猛的CDMO中,康日百奥生物科技(苏州)有限公司(Bioworkshops (Suzhou) Limited)(以下简称“康日百奥”),这家CDMO 公司在其生物药原液生产不断蓬勃发展的同时,作为国内屈指可数的DP已通过欧盟质量受权人(Qualified Person)审计(简称"QP审计")的CDMO服务供应商,康日百奥完善的高质量无菌制剂灌装的布局也使得其可以为更多的生物制药企业提供更广维度的服务。(药融云数据www.pharnexcloud.com显示,国内大分子CDMO中既有DS和DP布局的企业,同时DP通过欧盟QP认证的企业极少。)
据悉,康日百奥目前拥有约2000m2的制剂灌装生产区,已有一条无菌灌装线在2020年8月正式投产,从设备安装到验证、正式投产仅用短短4个月的时间,基于团队多个商业化产品的灌装经验,目前已经交付50余批次的合作伙伴的无菌制剂灌装项目,成功率达到100%。康日百奥专业的制剂灌装团队拥有10年以上无菌生产经验,主要致力于液体,冻干,预充针,卡式瓶的灌装生产。
无菌制剂灌装作为整个生物药GMP生产的最后环节,同时也是需要进行严格监控的环节,高标准的无菌保证体系贯穿着这一非常复杂的连续式生产过程。整个过程涉及到原液(Drug Substance,DS)化冻和混匀、除菌过滤、洗瓶、灌装加塞、冻干、轧盖、灯检、包装等多重工序,每一个工序都会直接影响最终的产品质量。
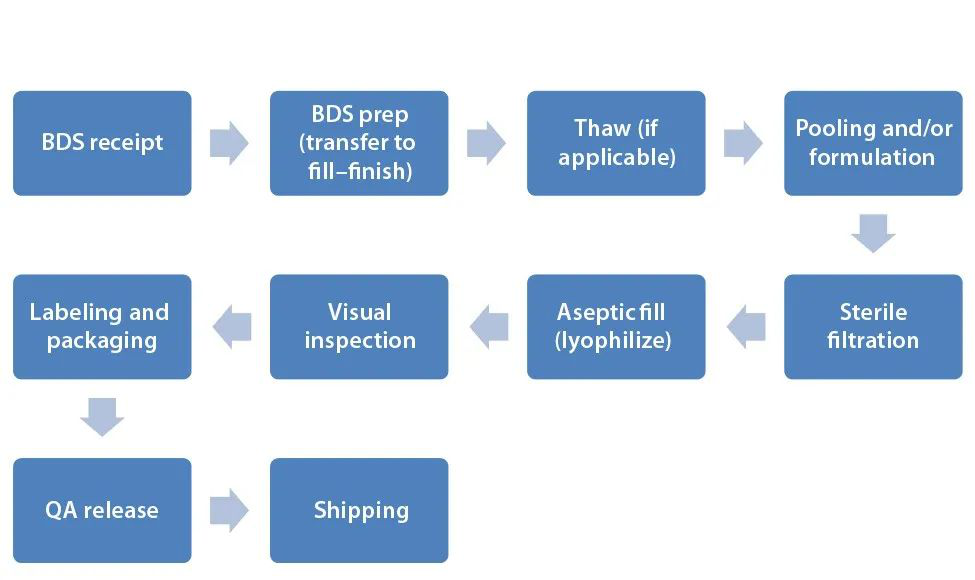
▲生物药制剂灌装流程示意图,具体品种有差异
康日百奥灌装生产车间主要包括:CNC区、D级区、C级区和B级区,以及B+A环境下的无菌灌装区域。生产过程中所有与产品接触的物料均采用一次性物料以防止交叉污染。DP已经通过欧盟QP审计,质量体系符合EMA要求,同时也通过了国内GMP审核。所有会影响产品生产的过程,文件,人员,环境,物料都会进行严格监控。
灌装生产线装量覆盖范围(0.2mL – 50.0mL),同时在连续生产时,可进行在线称重控制,进而保证灌装精度。康日百奥目前可灌装品种包括抗体,融合蛋白,疫苗等多种生物制剂,商业化灌装生产线也会在年底投产, 届时,将涵盖包含冻干、预充针等市场上主要药物剂型的灌装生产线,可灌装产能将达到1500w瓶/年,基于强有力的法规支持,针对无菌灌装完备的QC检测放行体系,将会更加高效高质灵活的提供无菌制剂灌装服务。
持续的全自动智能设备的投入以及对于技术的精进,进一步推动了康日百奥在CDMO领域增速的可延续性,形成了以质量和技术为核心的竞争优势,“高质量的产能“,真正的一站式服务,增加了合作伙伴整体药物开发的灵活性。
在药融圈看来,在未来:依靠国际一流的质量体系,符合不同国家和地区的法规要求的CDMO企业,持续提高技术平台竞争壁垒,不断提高交付效率和质量;康日百奥的未来值得期待。





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论