近日,聚焦于基因和细胞治疗的上海邦耀生物科技有限公司(以下简称“邦耀生物”)与华东师范大学、上海长征医院合作的新一代异体通用型CAR-T疗法(管线代号:BRL-303)治疗自身免疫疾病的研究成果被《Nature》子刊《Nature Reviews Rheumatology》(《自然评论风湿病学》)研究亮点(Research Highlights)专栏以“Off-the-shelf CAR T cells for refractory autoimmunity”为题目进行了报道。杂志评论认为,通过该研究的临床数据表明,靶向CD19抗原的异体通用型CAR-T细胞在自免疾病治疗中显示了出色的临床安全性和有效性。值得一提的是,2024年7月15日该项研究已正式在国际顶级学术期刊Cell上发表[1],这是国际上首次报道异体通用型CAR-T细胞成功治疗自身免疫疾病,也是顶尖学术期刊Cell首次发表CAR-T细胞治疗自身免疫疾病的研究。

Nat Rev Rheumatol (2024). https://doi.org/10.1038/s41584-024-01148-y
近年来,尽管自体CAR-T在血液肿瘤的治疗中已经取得了良好的治疗效果,但由于其个性化定制的固有属性,给商业化推广带来了极大挑战。因此,现货可供、具有完美商业化属性的异体CAR-T成为免疫细胞治疗产业最重要的发展方向。BRL-303是邦耀生物基于自主研发的通用型细胞平台(TyUCell®)开发的全新一代UCAR-T产品,主要利用基因编辑技术改造异体免疫细胞,有效避免了异体细胞移植中可能存在的GVHD和HVG风险,在保障细胞产品安全性和有效性的基础上,真正实现了免疫细胞治疗产品的通用化,该产品布局的适应症领域为——“自身免疫疾病”。
据杂志文章报道,在该研究中上海长征医院徐沪济教授团队使用邦耀生物BRL-303 UCAR-T产品成功治疗了3例难治性自身免疫性疾病患者,其中1例为免疫介导的坏死性肌炎(IMNM)、2例为系统性硬化症(SSc)。临床结果显示,接受BRL-303细胞治疗后,所有患者的CRISS评分在几个月内得到显著提高;且在皮肤纤维化方面,2名患者修改后的Rodnan皮肤评分(mRSS)均显著下降。另外经细胞治疗后,所有患者的B细胞均被完全清除,IMNM患者的自身抗体被彻底消除;2名SSc患者的重要器官纤维化损伤均得到了逆转,并在6个月的监测期内持续改善。整个治疗过程耐受性良好,未观察到细胞因子释放综合征(CRS)、移植物抗宿主病(GvHD)、免疫效应细胞相关神经毒性综合征(ICANS),体现了显著的疗效和安全性。
此外,文章系统描述了BRL-303 UCAR-T独特的制备工艺及卓越的临床疗效,并对其相比于传统自体CAR-T所具有的巨大临床价值进行了高度评价。最后,该项临床试验研究者(PI)、Cell论文第一通讯作者徐沪济教授在文章中介绍:“未来,我们还将继续对这些治愈患者进行长期随访以评估临床治疗效果,并计划进一步增加研究患者的例数来验证同种异体CAR-T细胞的临床安全性和有效性。”此外徐教授还强调,根据已有的临床结果,通用型CAR-T疗法具有巨大的治疗潜力和市场价值,有望改写改变难治性自身免疫疾病的治疗格局。
对此,邦耀生物董事长、论文共同通讯作者刘明耀教授表示:“目前已上市或正在研的CAR-T产品大多属于自体来源的产品,此次邦耀生物BRL-303 UCAR-T产品则属于典型的跨代产品,最突出的优势在于其源自健康供者细胞、可规模化制备成现货型产品,具有即需即用,方便、安全、成本低、效果好等特点,能够全面克服自体CAR-T产品高度个性化、制备周期长、失败风险高且成本极其高昂的诸多痛点。通过临床研究显示,BRL-303产品在使用比自体CAR-T更低的FC预处理条件下,在患者体内实现了长期存留和有效杀伤,安全性、有效性等各方面指标达到甚至超过了传统自体CAR-T。未来,我们将积极推进该产品的国内外申报工作,与临床专家一起争取早日完成新药的临床转化,惠及广大患者。”
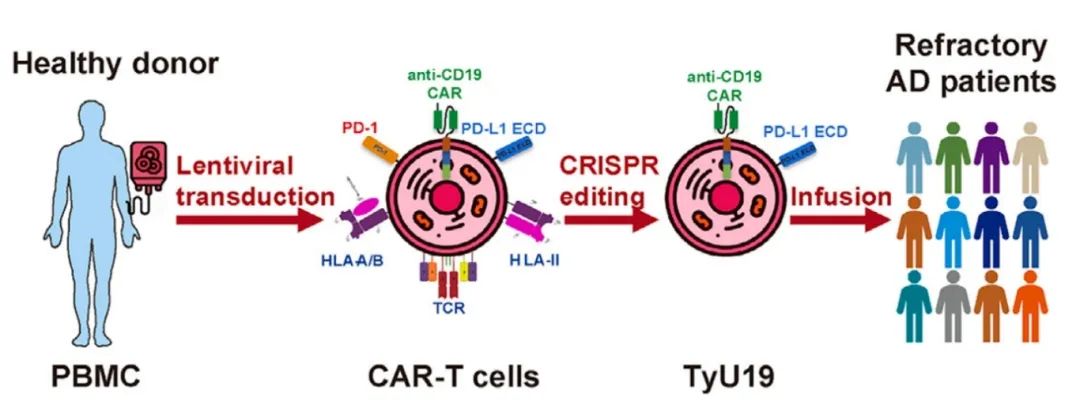
BRL-303细胞制备和使用
与国内外同类型产品相比,邦耀生物新一代BRL-303 UCAR-T产品具有以下临床优势:
邦耀生物UCAR-T产品通过系统的基因编辑和改造已经实现有效的免疫逃逸,在治疗过程中,无需对患者进行HLA分型筛选,可实现真正的现货可供,极大拓展了产品的适用范围。并且目前已经实现了单次几百人以上的生产规模,不仅极大降低了生产成本,还减少了患者等待时间,极大提高了细胞治疗产品在临床使用中的便利性,在临床治疗中体现出了卓越的优势。
邦耀生物UCAR-T产品无需对患者进行额外的清淋或者免疫抑制。仅采用常规甚至更低的清淋方案,就可以实现肿瘤细胞的完全清除,还能够有效避免对患者过度免疫抑制所带来的感染、粒细胞缺乏、淋巴细胞恢复慢等风险,显示出了极高的临床安全性。
邦耀生物UCAR-T产品的T细胞来自于年轻的健康供者,其活性远远优于长期血液病患者自身的免疫细胞,在回输体内后具有极佳的扩增潜力和持久性。在产品前期的IIT研究中,邦耀生物的UCAR-T表现出显著且持久的肿瘤清除能力,能快速实现疾病的完全缓解。
可以说,邦耀生物全新一代UCAR-T产品解决了CAR-T治疗行业的痛点和难点,实现了疗效、安全性与临床可及性的全面提升,具有非常显著的产业化优势;且其优异的临床安全性、治疗效果和极低的生产成本能够让更多自免疾病及肿瘤患者充分享受到CAR-T治疗这一高科技带来的红利。此前,邦耀生物针对B细胞恶性肿瘤疾病领域,用于治疗适应症“B急性淋巴细胞白血病”的UCAR-T产品(管线代号:BRL-301)的临床试验申请(IND)已于2023年7月获得中国国家药品监督管理局药品审评中心(CDE)的批准。未来,邦耀生物将继续全力推动UCAR-T在自身免疫性疾病和实体肿瘤治疗中的临床转化与应用,为广大患者带来更优的治疗选择。
[1] Wan, X. et al. Allogeneic CD19-targeted CAR-T therapy in patients with severe myositis and systemic sclerosis. Cell 187, https://doi.org/10.1016/j.cell.2024.06.027 (2024)
[2] Papatriantafyllou, M. Off-the-shelf CAR T cells for refractory autoimmunity. Nat Rev Rheumatol (2024). https://doi.org/10.1038/s41584-024-01148-y



邦耀实验室
为人类健康提供解决方案
长按二维码关注我们
合作、投稿、转载授权事宜请联系
邮箱:wjinfang@brlmed.com



































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论