
新闻纲要
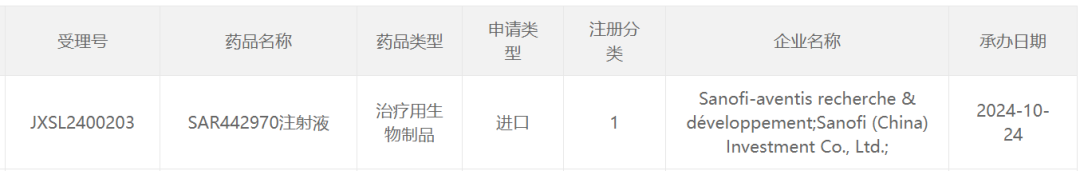
10月24日,中国国家药监局药品审评中心(CDE)官网公示,赛诺菲(Sanofi)申报的1类新药SAR442970注射液临床试验申请获得受理。公开资料显示,SAR442970是一款靶向TNFα和OX40L的双特异性纳米抗体(VHH),目前正在国际范围内处于2期临床阶段。本次是该产品首次在中国申报IND。
新闻详情
SAR442970注射液是一款基于Nanobody技术开发而成的双特异性抗体。据赛诺菲此前公开资料介绍,通过连接Nanobody分子片段,该公司团队可以创建新的化合物(称为“多价”纳米体分子),可一次结合多个不同的靶点。例如,一种单一治疗性纳米体分子可以通过与肿瘤细胞和免疫细胞上的多个位点结合,为肿瘤细胞和免疫细胞之间建立桥梁,帮助机体免疫系统抗击癌症。

其中一项试验是为了评估 SAR442970 注射液与安慰剂在治疗成人化脓性汗腺炎方面的效果和安全性。在这项试验中,参与的患者会每两周接受一次 SAR442970 注射液的治疗。安慰剂是一种没有实际治疗作用的物质,通过与使用 SAR442970 注射液的患者进行对比,可以看出该药物是否真正有效以及是否安全。
另一项试验则是将 SAR442970 注射液与另外两款阳性对照药进行比较,以评估其在治疗原发性局灶节段性肾小球硬化或微小改变疾病患者时的疗效和安全性。阳性对照药是已知具有一定治疗效果的药物,通过与它们对比,可以更好地了解 SAR442970 注射液的优势和不足。
入群交流


为促进生物医药行业的合作交流,小编决定组建微信交流群,供行业相关从业人员进行交流,请添加上方小编微信入群,备注:公司+职位+姓名。

未来会议安排,敬请期待






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论