据《药融云医药行业观察周报》数据统计,在2023.04.10-2023.04.16期间,共有65个创新药/改良型新药注册申请获CDE承办(按受理号统计,不含补充申请)。其中,国产药品受理号45个,进口药品受理号20个。
在这期间,共计48款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药26款,生物药20款,中药2款。
获批临床创新药/改良型新药信息速览(部分)
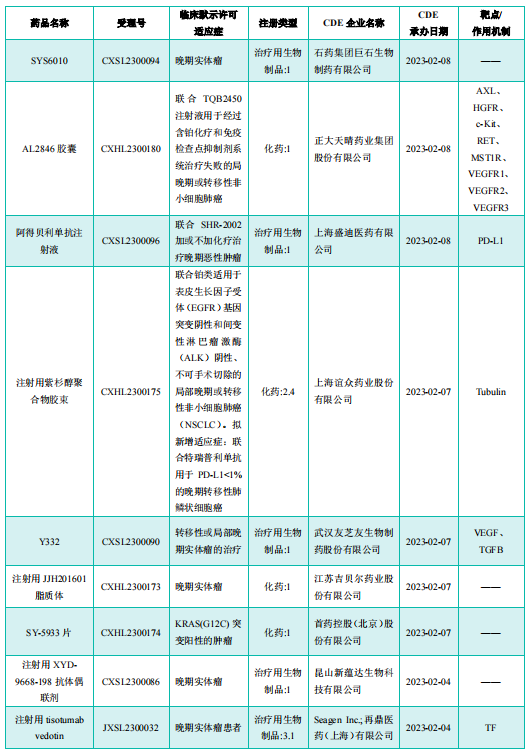
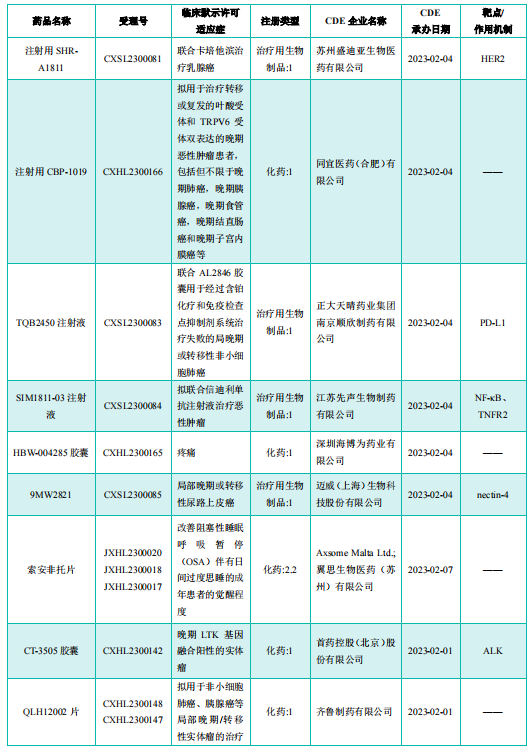
图片来源:《药融云医药行业观察周报》
注:想要获取《药融云医药行业观察周报》完整内容,可以关注“药融云(yrydata)”公众号,后台回复关键词“报告”进行领取;或者前往“药融文库(wenku.pharnexcloud.com/?mh)”「原创报告」中进行全文下载。
(1)HBW-004285胶囊——Nav1.8抑制剂
海博为药业HBW-004285胶囊获得临床试验默示许可,批准开展用于疼痛临床试验。HBW-004285胶囊是一款Nav1.8抑制剂,通过阻断Nav1.8通道,阻滞痛觉信号由外周神经系统向中枢神经系统传递,从而产生镇痛作用。
Nav1.8是一种主要表达于伤害感受神经元上的河豚毒素不敏感型电压门控钠离子通道,在外周神经系统的痛觉信号传导中起着关键作用,是疼痛治疗的高选择性作用靶点。
药融云数据库显示,HBW-004285是海博为药业继HBW-3220、HBW-3210之后获批临床的第三款1类创新药。HBW-3220胶囊是三代非共价BTK抑制剂,已于2022年2月获得B细胞淋巴瘤的临床试验批件,近日海博为药业又正式提交了HBW-3220胶囊新增适应症(肾小球肾炎)临床试验申请。
HBW-3220审评时间轴(直观呈现审评状态变化及时间节点)
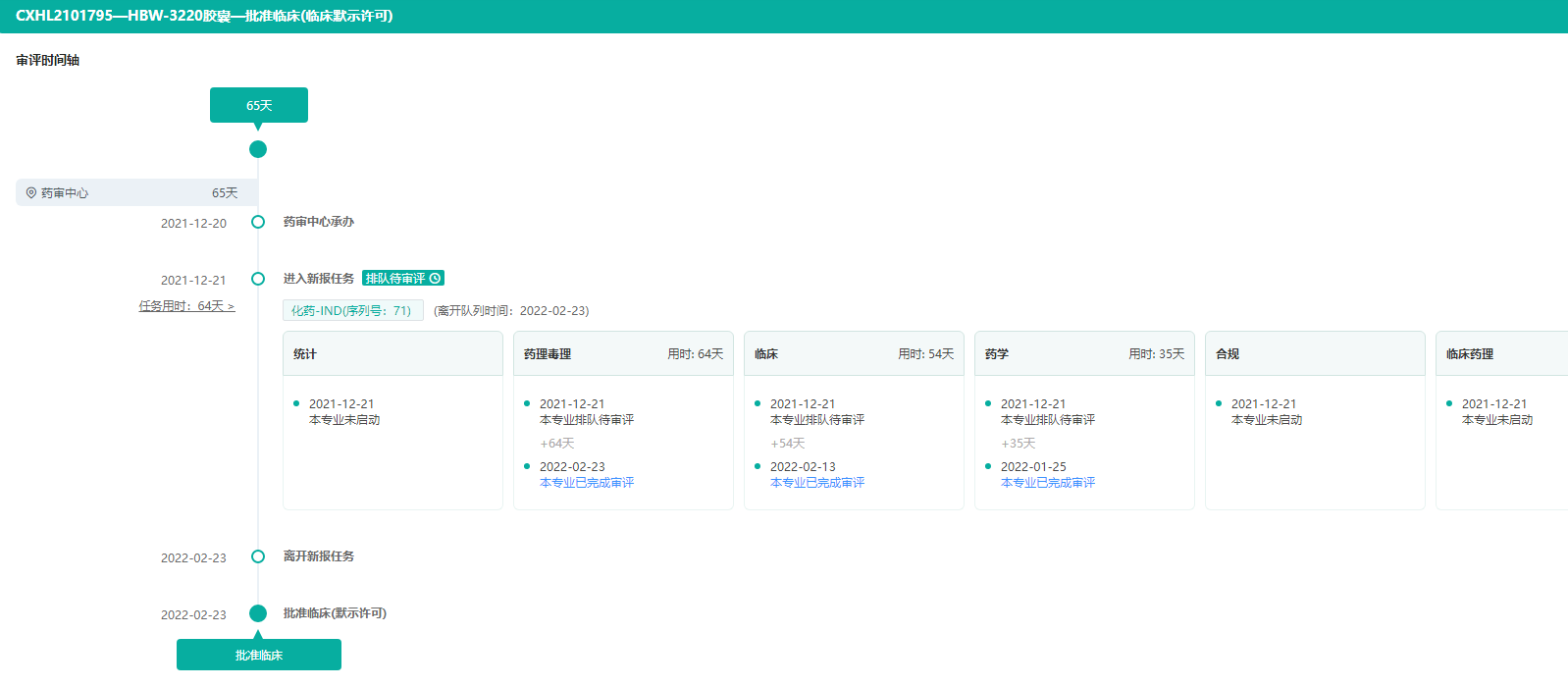
图片来源:药融云中国药品审评数据库
注:药融云中国药品审评数据库,可以通过订阅受理号/品种/企业,实时监控目标药品、企业的注册审评最新动态,预测受理号审评完成时间,提前制定市场推广计划和策略,增强市场竞争力和先发优势。
HBW-3210胶囊是海博为药业自主研发的首款强透脑、可逆抗耐药三代BTK抑制剂,拟用于B细胞非霍奇金淋巴瘤,主要开发适应症为原发性/继发性中枢神经系统淋巴瘤(PCNSL/SCNSL)或可能累及中枢神经系统的弥漫大B细胞淋巴瘤(DLBCL);于2022年10月获得国家药品监督管理局临床试验默示许可。
据药融云全球药物研发数据库统计,全球已有36家企业涉足Nav1.8抑制剂领域,包括美国福泰制药公司、辉瑞、GSK、默沙东、恒瑞医药、上海济煜医药等。目前,在研Nav1.8抑制剂有美国福泰制药的VX-548,Algotherapeutix的ATX-01,日本住友的DSP-2230,济煜医药的JMKX-000623,海博为药业的HBW-004285等等。其中进度最快的是VX-548,目前已进入III期临床,曾被FDA授予治疗中、重度急性疼痛的突破性疗法认定。
全球Nav1.8抑制剂研发情况查询
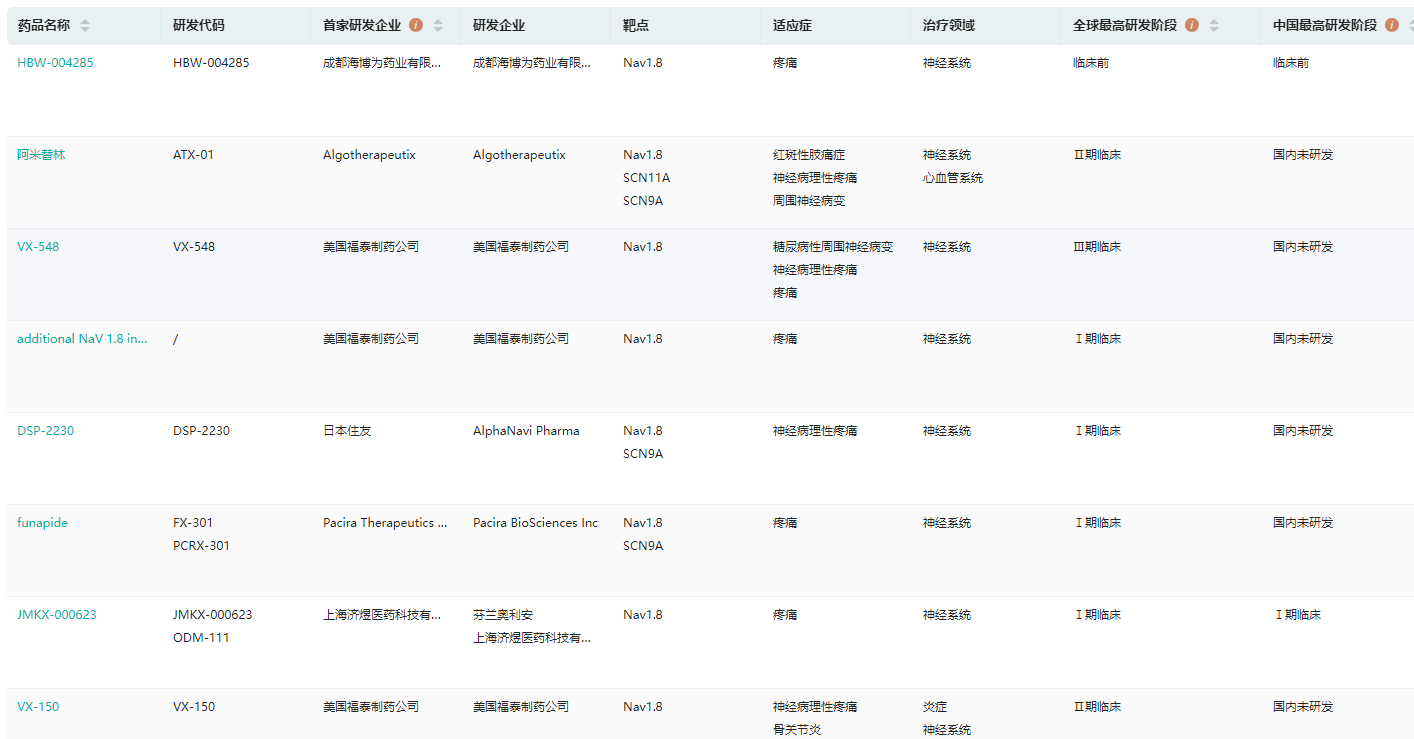
图片来源:药融云全球药物研发数据库
(2)JS401注射液——拟治疗高脂血症
君实生物的1类新药JS401注射液获得临床试验默示许可,拟用于治疗高脂血症。JS401注射液是一款靶向血管生成素样蛋白3(ANGPTL3)信使RNA(mRNA)的小干扰RNA(siRNA)药物,在肝细胞内特异性降解ANGPTL3mRNA,并持续性抑制ANGPTL3蛋白的表达,从而发挥其降脂的作用。ANGPTL3是一种在脂质代谢中起关键作用的蛋白质。
药融云数据库显示,目前全球仅再生元有一款靶向ANGPTL3的单克隆抗体类药物Evkeeza获批上市,用于家族性高胆固醇血症治疗。Evkeeza是FDA批准的首个结合并阻断血管生成素样3(ANGPTL3)的治疗药物,为这一患者群体提供了一种新的治疗选择。
Evkeeza基本信息查询(部分)
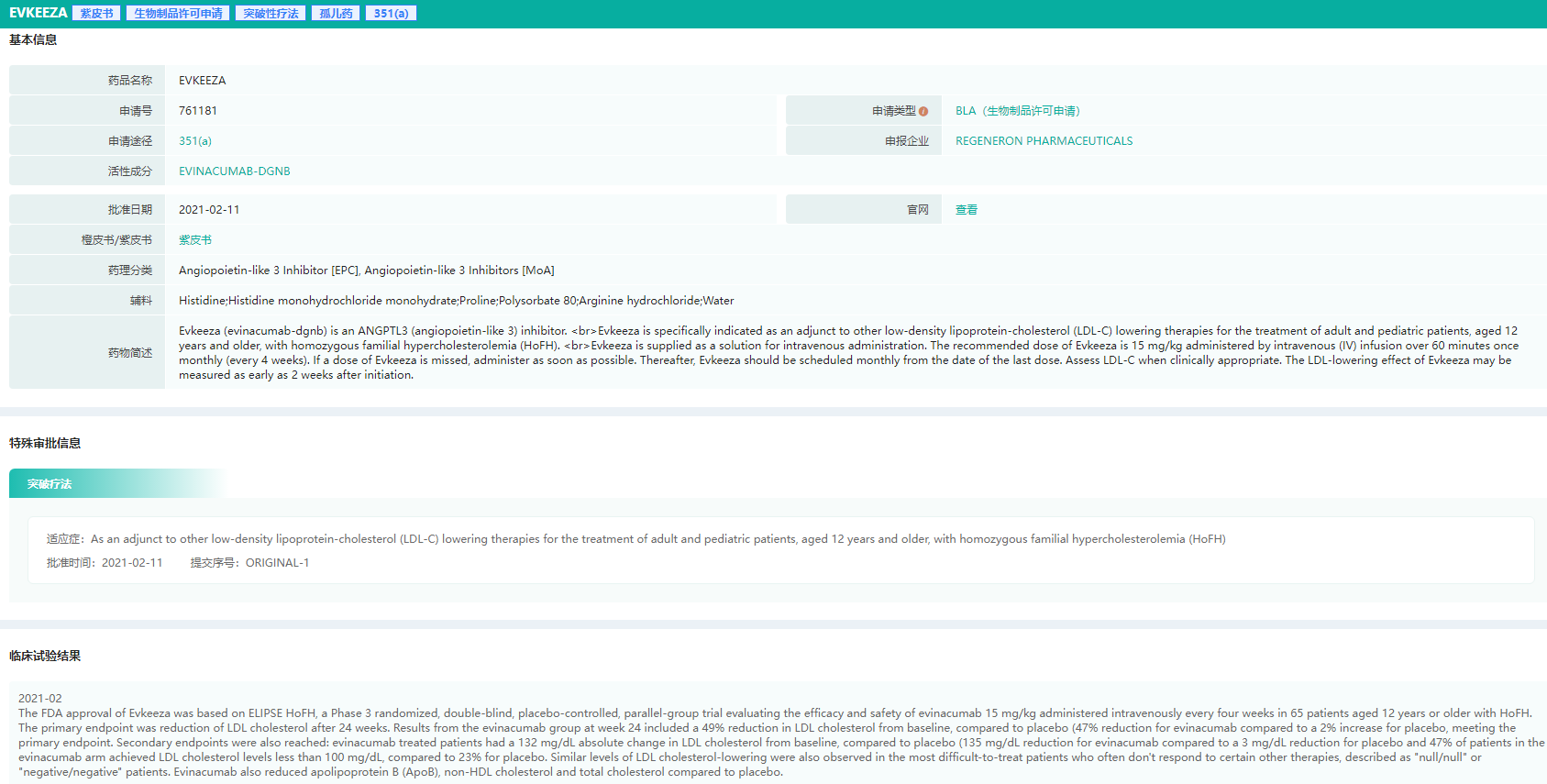
图片来源:药融云-美国FDA批准药品数据库
(3)NFS-02眼用注射液——新型眼内注射基因治疗产品
纽福斯NFS-02眼用注射液获得临床试验默示许可,拟用于治疗Leber遗传性视神经病变。公开资料显示,NFS-02是一款重组腺相关病毒血清型2载体(rAAV2)的新型眼内注射基因治疗产品,通过单次玻璃体内注射,将正确的基因通过玻璃体腔注射递送至患者受损的视神经节细胞,修复线粒体生物呼吸链,使视神经节细胞恢复活力与视功能。
药融云数据库显示,这也是纽福斯公司的第二款基因治疗药物获得国家药品监督管理局(NMPA)颁发的临床试验默示许可(IND)。NFS-02已于2022年1月被FDA授予了孤儿药称号(ODD)。NFS-02是目前全球唯一在研针对ND1-LHON的基因疗法,在全球存在未被满足的临床空白。
纽福斯的另一款核心产品NR082,用于治疗ND4介导的Leber遗传性视神经病变(ND4-LHON),是首个同时获得中国NMPA及美国FDA授予的临床试验IND许可的中国籍基因治疗新药。目前已完成中国III期临床试验所有患者入组给药,并在美国启动多个临床研究中心。
NR082眼用注射液研发历程时间轴
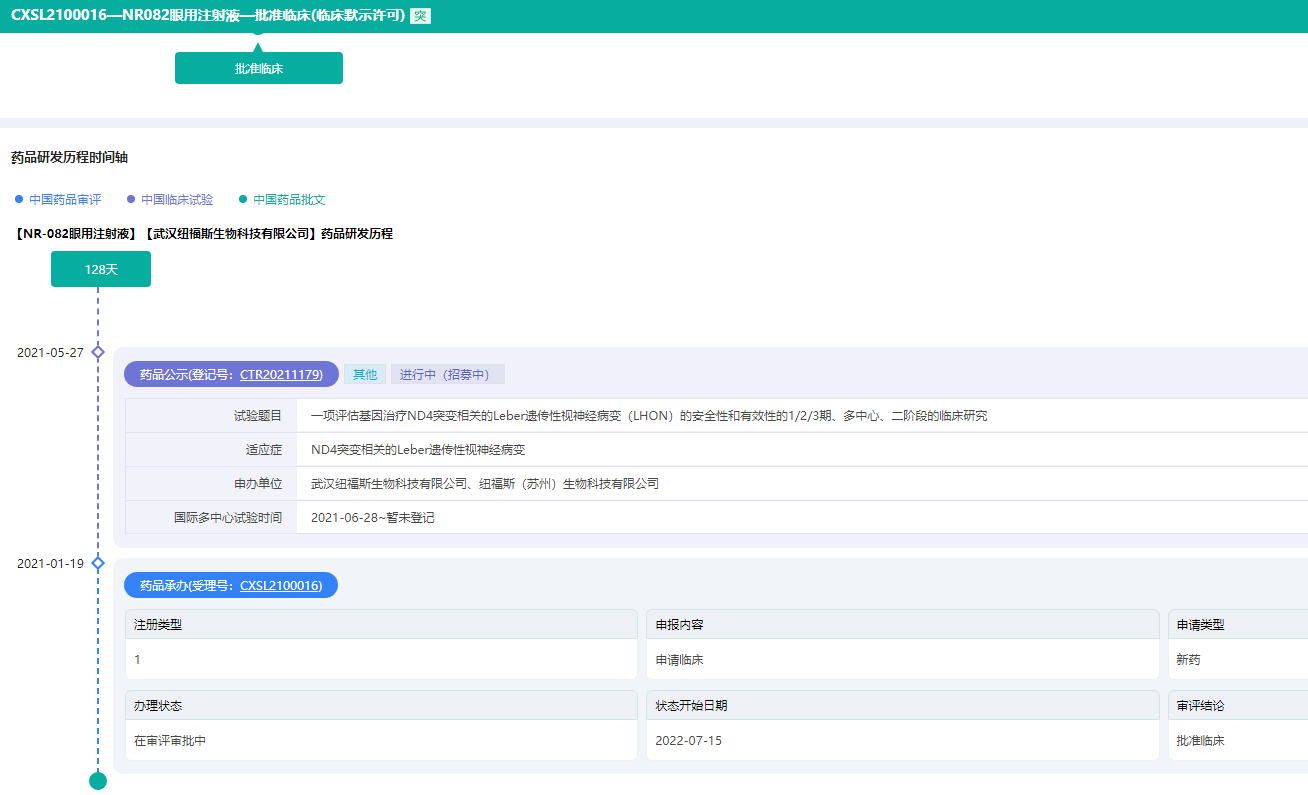
图片来源:药融云中国药品审评数据库
(4)人参总次苷片——辉昱生物1.2类中药
上海辉昱生物医药的1.2类中药人参总次苷片获得临床试验默示许可,用于治疗糖尿病黄斑水肿(气阴两虚,络脉瘀阻证),以及视物模糊,目睛干涩,或视物变形,或眼前黑花飘舞等。
药融云中国药品审评数据库显示,中国医药研究开发中心曾在2005年2月申报人参总次苷片、口崩片5类(有效部位及制剂)临床,在2007年12月获批临床,后于2014年开展临床试验,用于治疗慢性稳定型心绞痛。
药融云中国医药专利数据库显示,人参总次苷的相关专利共有11条,其中《一种人参总次苷药物组合物及其制备方法和应用》(200510083855.6,有权),专利权在2012年从中国医药研究开发中心转移至上海弘医堂(2022更名为上海辉昱),该组合物主要有效成分是Rg3、Rg2、Rh1,用于胸痹心痛、心肌缺血、失血性休克、心力衰竭疾病。
人参总次苷专利信息查询
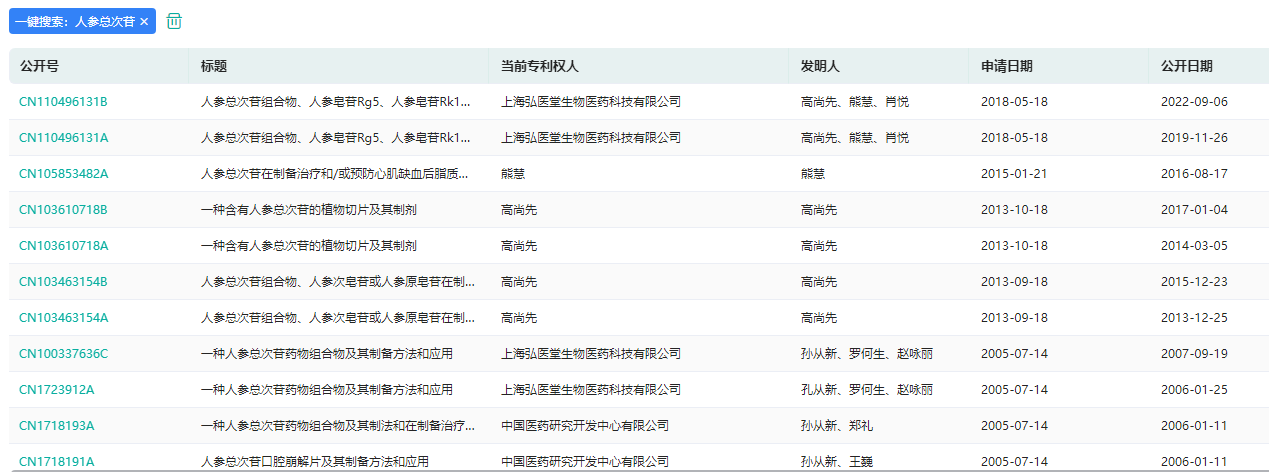
图片来源:药融云中国医药专利数据库
(5)HYR0201颗粒——治疗小儿急性上呼吸道感染
天地恒一制药的HYR0201颗粒获得临床试验批准,用于治疗小儿急性上呼吸道感染,症见头痛、咽痛、肌肉酸痛、发热、咳嗽、鼻塞、流涕等。
药融云数据库显示,天地恒一制药目前拥有药品生产批文30个,涉及27个品种,包括三七止血胶囊、一清颗粒、复方益肝灵胶囊、普瑞巴林胶囊、阿托伐他汀钙片、麝香心脑乐胶囊、绛糖宁片、夏天无胶囊、伤痛宁胶囊、恩替卡韦片等。
天地恒一制药每年获批批文趋势
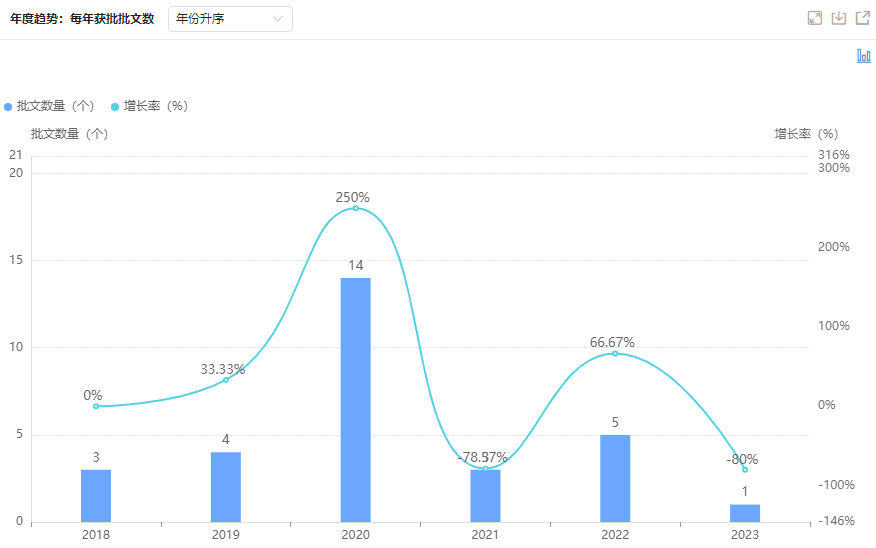
图片来源:药融云中国药品批文数据库
药融云全国医院销售数据库显示,天地恒一制药2022年在医院端的TOP3销售药品是:清热消炎宁片、复方益肝灵胶囊、活络消痛胶囊,销售额分别为8,690.47万元、5,929.02万元、4,788.24万元。
清热消炎宁片由单味药九节茶经现代工艺精制而成,用于流行性感冒,咽喉炎,肺炎,菌痢,急性胃肠炎,阑尾炎,烧伤,疮疡脓肿,蜂窝织炎。
天地恒一制药的清热消炎宁片,2022年还通过国家GLP认证的“新药药效与安全性评价湖南省重点实验室”完成了系列体内外药效及毒理研究,证明清热消炎宁片具有显著的抗冠状病毒(HCoV-229E)、甲型流感病毒(H1N1、H3N2)、乙型流感病毒(IBV)、鼻病毒(VR-1187)、呼吸道合胞病毒(RSV)作用,能有效降低病毒在细胞中的复制和增殖,改善病毒导致的组织病变;还能明显减轻咽部炎症水平,减少咳嗽次数;具有良好的抗炎、退热效果和安全性,可用于预防和治疗多种病毒导致的各类炎症和感染。
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论