
据药融云数据库统计,在2022.12.19-2022.12.25期间,共有28项创新药/改良型新药注册申请获CDE承办(按受理号统计,不含补充申请)。其中,国产药品受理号8个,进口药品受理号20个。
同时,在这期间共计有92款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药62款,生物药28款,中药2款。(想要获取《药融云医药行业观察周报》中获批临床创新药/改良型新药信息的完整版,请关注“药融云”公众号(yrydata)后台回复“报告”关键词)
一、获批临床的创新药/改良型新药
其中,获得“默示许可”的创新药/改良型新药临床试验中,值得注意的有:恩华药业的NH130枸橼酸盐片、锦篮基因的GC301腺相关病毒注射液、CleaveTherapeutics的CB-5339胶囊、先声药业的注射用SIM0237。
获批临床创新药/改良型新药信息速览(部分)
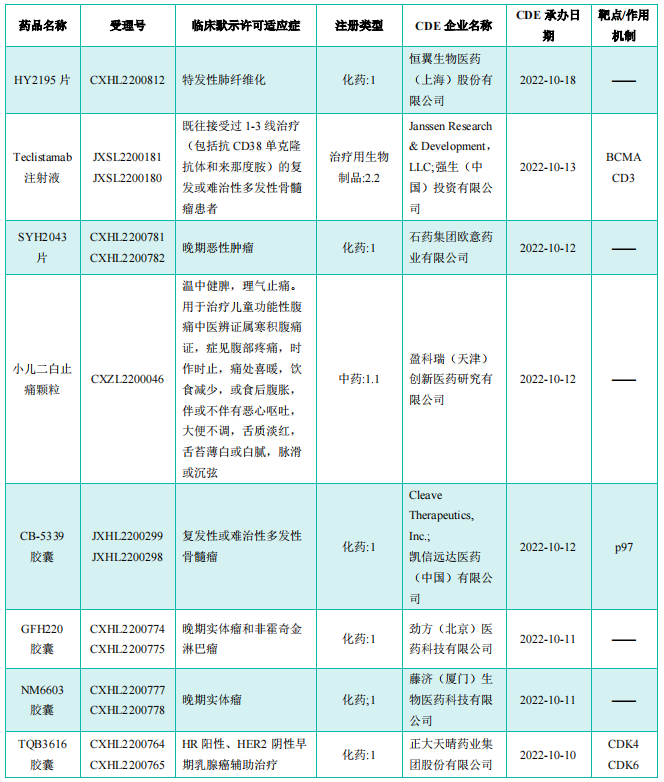
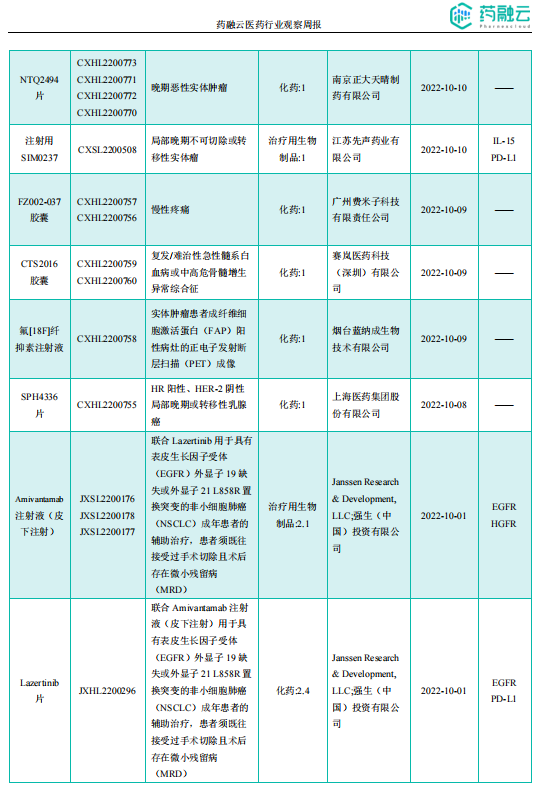
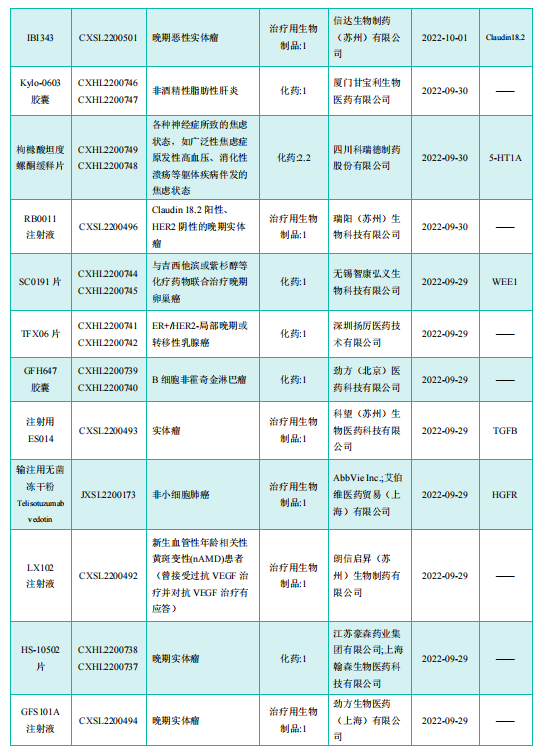
图片来源:《药融云医药行业观察周报》
(1)NH130枸橼酸盐片——治疗帕金森病精神病
NH130枸橼酸盐片,是恩华药业研发的一款强效的5-羟色胺2A(5-HT2A)受体反向激动剂,这是该品种首次获批临床(默示许可),也是国内首个PDP治疗药物获批临床,拟用于治疗帕金森病精神病。5-HT2A受体是致幻剂和治疗精神疾病的药物的典型靶标。
NH130枸橼酸盐片的临床前试验结果显示,其对帕金森精神病动物模型有效且不影响运动功能。同时,心脏毒性和磷脂沉积等不良反应小,安全窗大,具有较好的药代特性。至此,恩华药业共有至少10款神经系统1类新药迈入IND及以上阶段。
NH130枸橼酸盐片基本信息(部分)
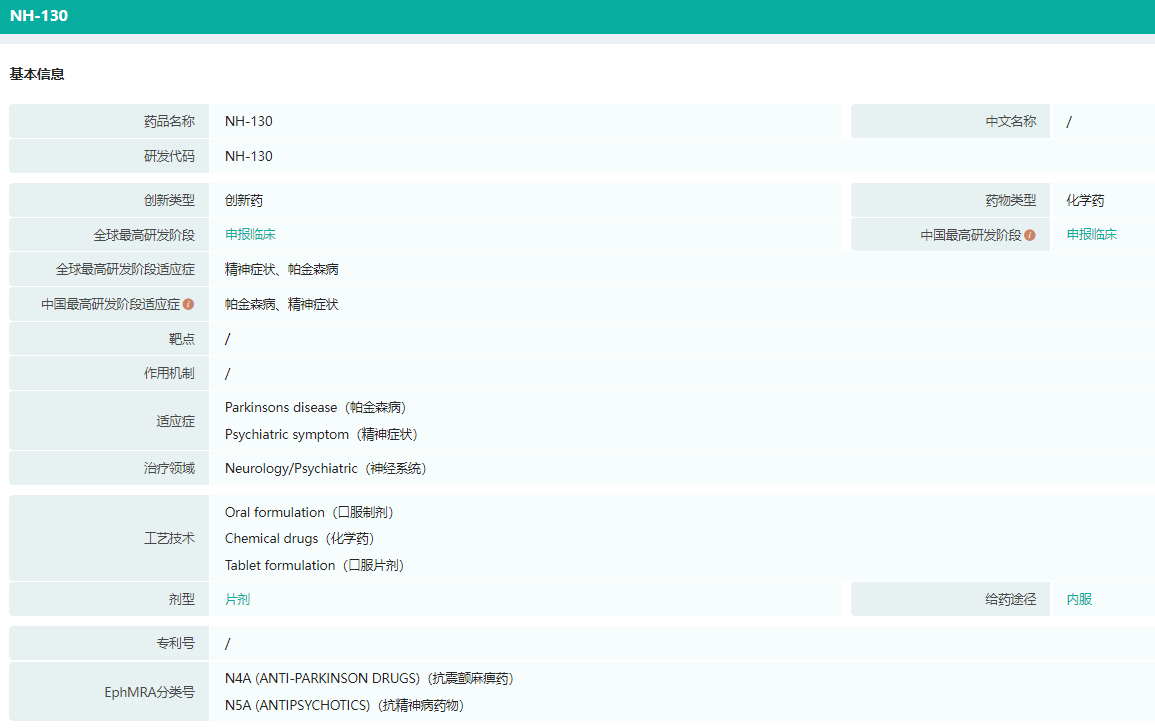
图片来源:药融云全球药物研发数据库
据药融云全国医院销售数据库统计,中国神经系统用药院内市场销售额峰值超880亿元,近两年有所下滑,2021年院内销售额为834亿元,为整体医药市场热门领域。目前,国采已进行了七批,已中标国采的神经系统药物共38个。
现阶段已过评企业数量在4家以上且暂未纳入国采目录的产品中,有丙戊酸钠注射用浓溶液、氢溴酸伏硫西汀片、阿立哌唑口服溶液、艾司唑仑片、吸入用七氟烷等产品,或将成为第八批国采的热门产品。
(2)GC301腺相关病毒注射液——早发型庞贝病AAV基因治疗药物
GC301腺相关病毒注射液由锦篮基因研发,是国际上首个获批临床试验的早发型庞贝病AAV基因治疗药物,用于治疗早发型庞贝病(IOPD)。
庞贝氏病,又称为酸性麦芽糖酵素缺乏症,是一种罕见的代谢贮积症疾病,主要是由于体内缺少酸性-α-1,4-葡萄糖苷酶,使人体内的糖原不能转化分解为葡萄单糖,导致大量糖原累积,出现肌肉无力,心脏扩大等症状。目前的主要治疗手段是酶替代疗法,即向体内注射含有缺失的α-1,4-葡萄糖苷酶,这种方法需要终生持续进行,且治疗成功率受到疾病严重程度、酶治疗剂量、抗体产生等多种因素影响。
GC301是一款以重组AAV(recombination AAV,rAAV)为载体搭载GAA基因表达序列的基因治疗药物,采用独创的系统性递送,通过单次静脉输注,可在心脏、骨骼肌、肝脏、神经系统等广泛分布,达到长期改善GAA酶活力水平、持续清除累积糖原和恢复肌肉力量的目的。
GC301腺相关病毒注射液I期临床实验信息(ChiCTR2200063229)
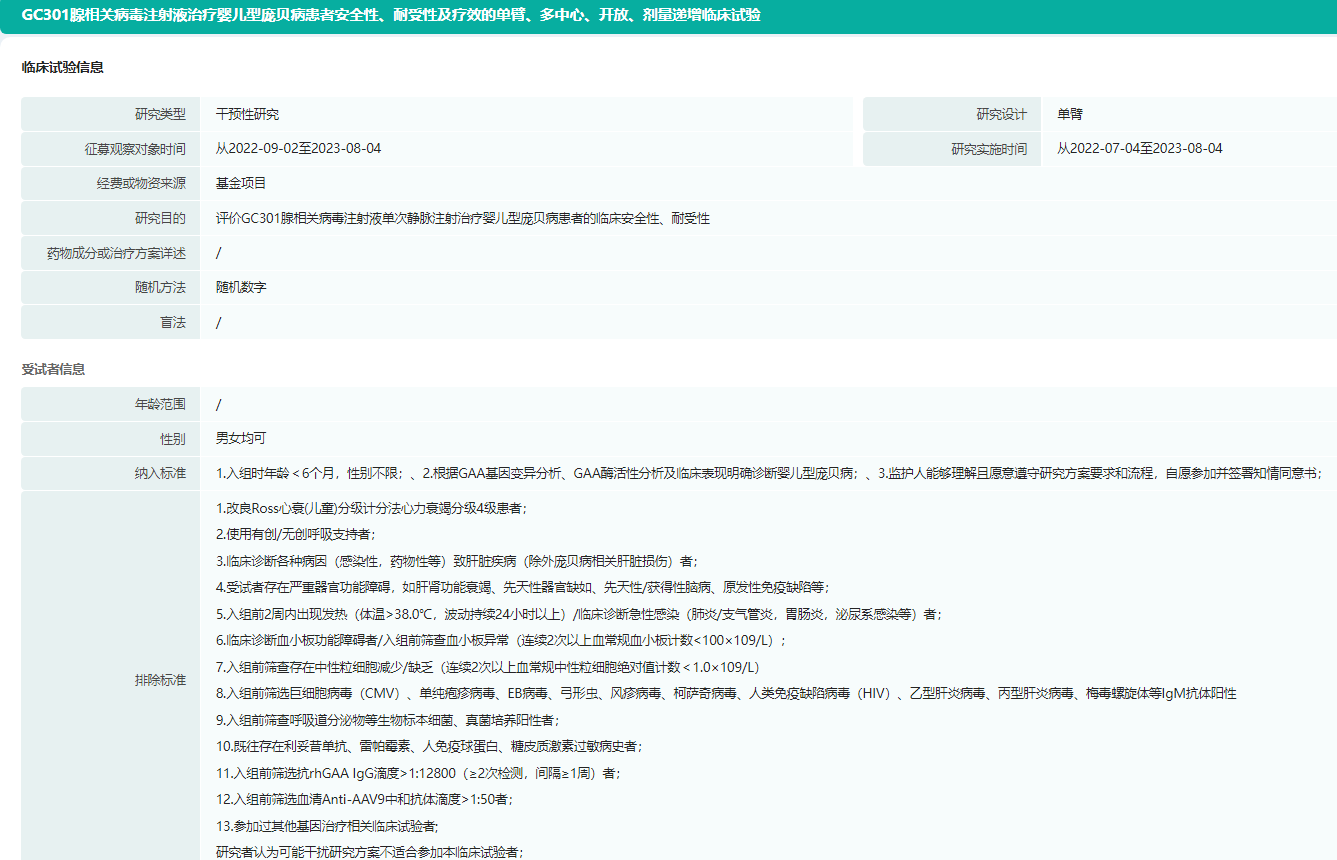
图片来源:药融云中国临床试验数据库
依托锦篮基因的AAV基因递送技术平台,锦篮基因开发了脊髓性肌萎缩症(SMA)基因治疗药物、高甘油三酯血症基因治疗药物、庞贝病基因治疗药物、家族性LCAT缺乏症基因治疗药物在内的多条基因治疗药物研发管线。
据药融云投融资数据库显示,锦篮基因于2021年2月完成近亿元的天使轮融资,由东方富海管理的中小企业发展基金、元生创投、赛盈资本、谢诺辰途基金共同投资完成。
(3)CB-5339胶囊——血液肿瘤和实体瘤的全球首创新药
CleaveTherapeutics的CB-5339胶囊获得临床试验默示许可,用于治疗复发性或难治性多发性骨髓瘤。CB-5339胶囊是一种新型口服二代小分子药物,通过含缬酪肽蛋白质 VCP/p97 这一在蛋白质稳态、DNA 损伤反应以及其它细胞应激通路上起关键作用的新靶点治疗癌症。
CB-5339是一种非常有潜力的新型药物,可以选择性靶向VCP/p97以治疗癌症。据药融云全球临床试验数据库显示,CB-5339用于急性髓性白血病(AML)和骨髓增生异常综合症(MDS)的I期临床研究正在进行中。
CB-5339临床试验NCT04402541基本信息(部分)
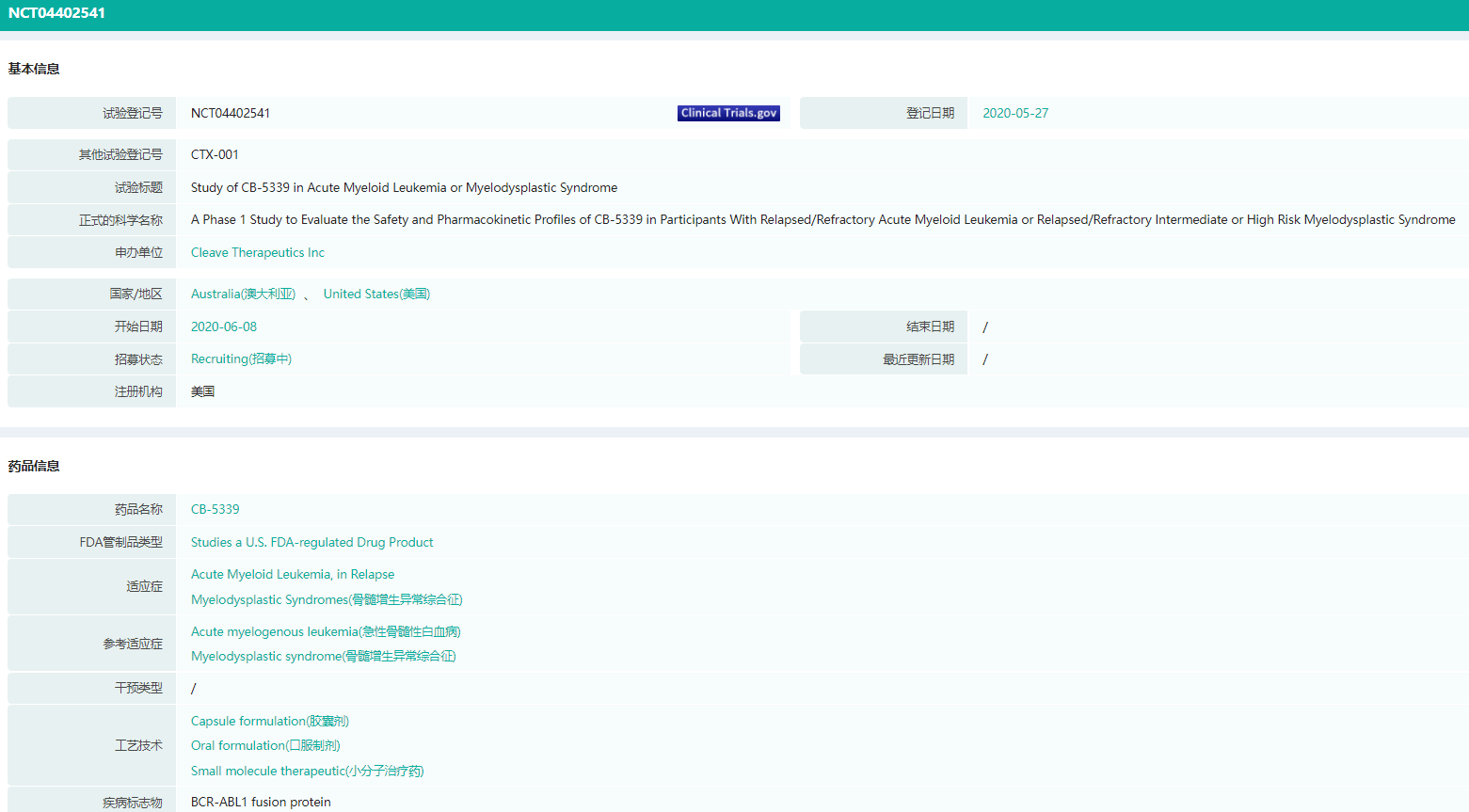
图片来源:药融云全球临床试验数据库
(4)注射用SIM023——用于局部晚期不可切除或转移性实体瘤
SIM0237是一种抗PD-L1/IL-15双特异性抗体,是先声药业基于自有蛋白质工程技术平台开发的一种抗PD-L1单抗与IL-15/IL-15Rα融合蛋白,可通过结合PD-L1阻断PD1/PD-L1免疫抑制通路,同时通过IL-15激活免疫系统,从而发挥解除免疫抑制和激活免疫系统的双重协同作用,达到抗肿瘤疗效。
此次注射用SIM0237获得临床试验默示许可,用于局部晚期不可切除或转移性实体瘤。注射用SIM0237是国内首款进入临床阶段的PD-L1/IL-15双抗。2022年10月,该药物已在美国获批临床。
注射用SIM0237审评时间轴
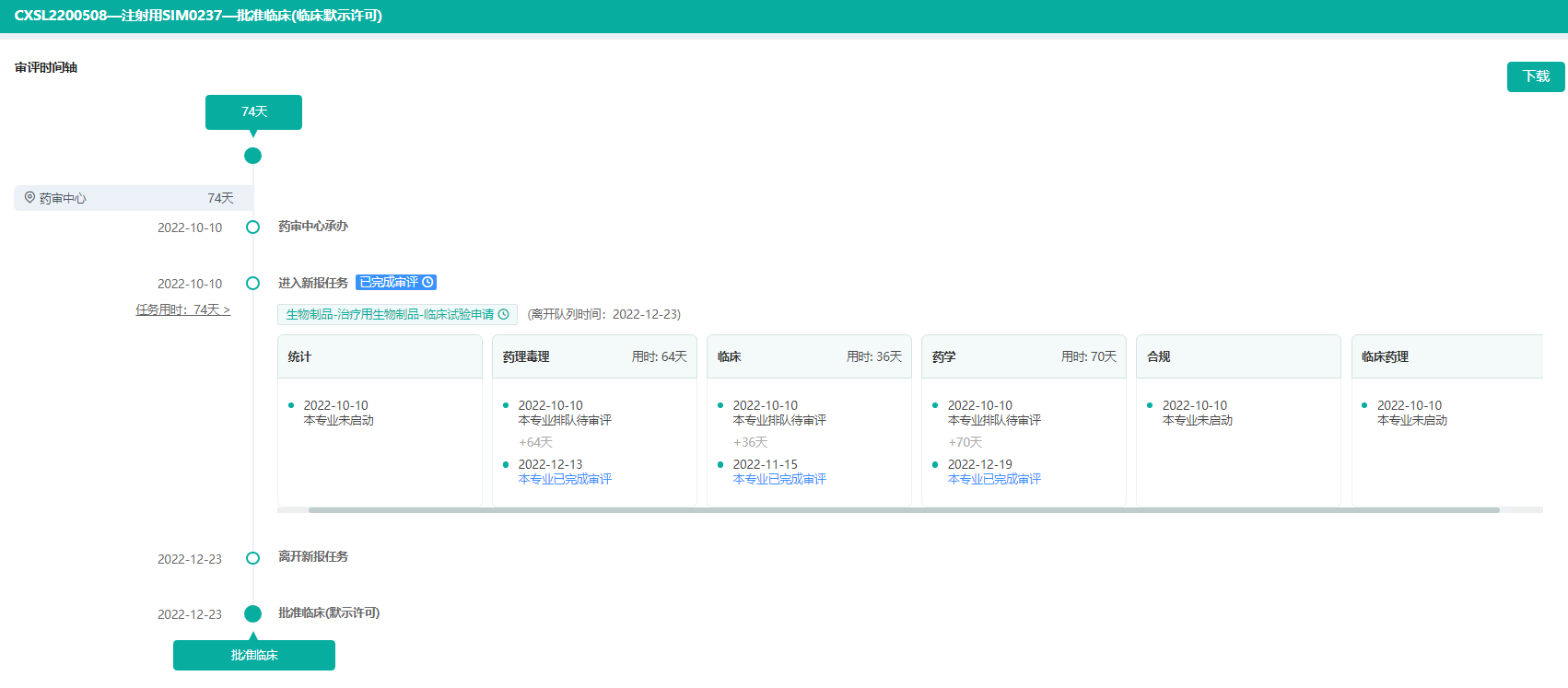
图片来源:药融云中国药品审评数据库
值得一提的是,2022年12月29日,先声药业宣布,其自主研发的两款抗肿瘤生物创新药——人源化TIGIT/PVRIG双特异性抗体SIM0348注射液、抗PD-L1/IL-15双功能融合蛋白注射用SIM0237也获批了临床。
据药融云数据库统计,截至目前,先声药业处于临床阶段或取得临床批件的在研创新药项目达18个,其中2个项目在中美两国获准开展临床研究。
二、获批上市的中药创新药
在2022.12.19-2022.12.25期间,还有1款新药获批上市——康恩贝的中药创新药侧金盏口腔溃疡贴片(5类)。
侧金盏口腔溃疡贴片的功能为清心泄热,用于心脾积热所致轻型复发性口腔溃疡。公开资料显示,侧金盏口腔溃疡贴片是从中药黄蜀葵花中采用先进的提取、分离、纯化技术,得到有效部位“黄蜀葵花总黄酮提取物”,采用现代制剂技术,研制而成的双层口腔贴片,是国内首个中药双层口腔贴片,为广大口腔溃疡患者提供了新的治疗选择。
想要获取完整《药融云医药行业观察周报》内容,实时了解分析国内外创新药/改良型新药注册申报情况、仿制药/生物类似物注册申报情况、盘点全球医药大健康行业投融资事件等,关注“药融云”公众号(yrydata),后台回复“报告”关键词,即可进行领取。
<END>












































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论