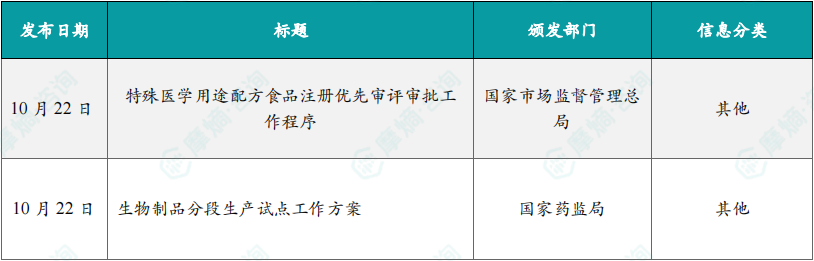
1.3.1本周国内医药大健康行业政策法规速览

1.3.2本周重点行业政策详细说明
(1)《特殊医学用途配方食品注册优先审评审批工作程序》
10月22日,市场监管总局发布《特殊医学用途配方食品注册优先审评审批工作程序》(以下简称《工作程序》),进一步规范特殊医学用途配方食品(以下简称“特医食品”)注册优先审评审批工作,引导企业加大对罕见病类特医食品和临床急需的新类型特医食品(糖尿病全营养配方食品、呼吸系统疾病全营养配方食品、肾病全营养配方食品、肝病全营养配方食品、肌肉衰减综合症全营养配方食品、创伤、感染、手术及其他应激状态全营养配方食品、炎性肠病全营养配方食品、食物蛋白过敏全营养配方食品、难治性癫痫全营养配方食品、胃肠道吸收障碍、胰腺炎全营养配方食品、脂肪酸代谢异常全营养配方食品、肥胖、减脂手术全营养配方食品等临床急需且尚未批准过的新类型特医食品。)的创新研发力度,更好满足病患临床营养需求。
(2)生物制品分段生产试点工作方案
10月22日,为深入贯彻党的二十大和二十届二中、三中全会精神,落实党中央、国务院支持生物医药产业高质量发展决策部署,国家药监局研究制定了《生物制品分段生产试点工作方案》,试点工作基于我国生物医药产业发展现状和监管实际,积极回应产业发展需求,以委托生产方式探索部分创新、临床急需等生物制品的分阶段生产,有利于进一步激发企业研发创新活力,促进药品研发生产专业化分工,提升创新和临床急需生物制品的供应保障能力,更好满足广大群众用药需求。
同期事件:
1. 2024年第43周10.21-10.27国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2024年第43周10.21-10.27国内仿制药/生物类似物申报/审批数据分析
3. 2024年第43周10.21-10.27全球医药大健康行业投融资数据
4. 2024年第43周10.21-10.27全球创新药研发概览
以上内容均来自{摩熵咨询医药行业观察周报(2024.10.21-2024.10.27)},如需查看或下载完整版报告,可点击!
<END>
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论