
6月4日,华东医药宣布,其在研1类新药HDM2005获批临床,适应症为晚期恶性肿瘤。据药融云数据库显示,目前,该公司有15款1类新药申请并获批临床。

截图来源:华东医药公告
1类新药 ROR1 ADC 获批,直击抗肿瘤药千亿市场
注射用HDM2005是由杭州中美华东制药研发并拥有全球知识产权的1类生物新药,是一款靶向受体酪氨酸激酶样孤儿受体 1(ROR1)的抗体偶联药物(ADC)。临床前研究显示,HDM2005进入体内后,抗体部分与表达肿瘤抗原的靶细胞特异性结合,HDM2005被肿瘤细胞内吞后,细胞毒素在胞内释放,从而完成对肿瘤细胞的杀伤;现有数据显示HDM2005具有良好的成药性和安全性。 据药融云数据库显示,抗肿瘤药和免疫调节药在全国院内市场销售峰值超千亿元,2022年全国院内销售额超1300亿元。
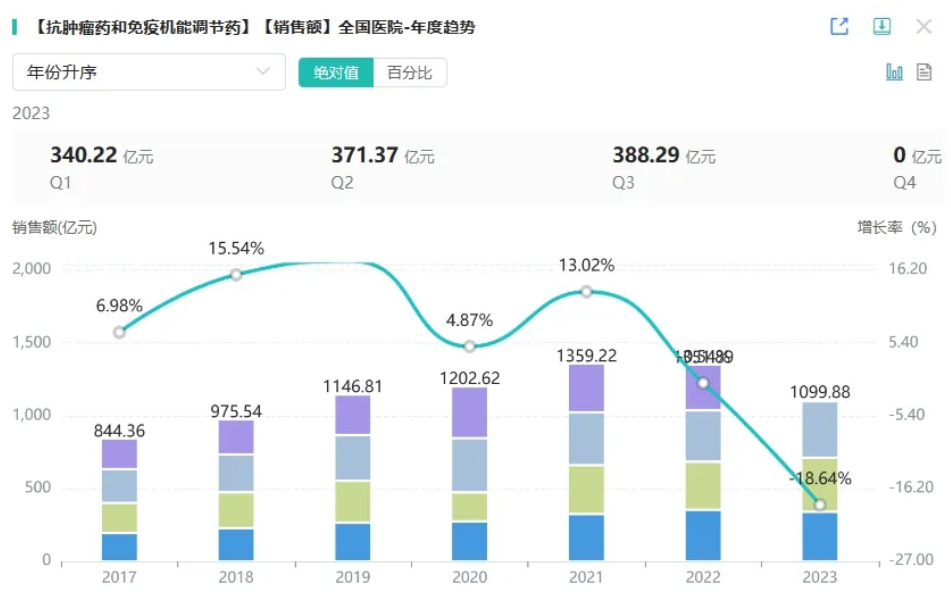
截图来源:药融云全国医院销售数据库
2024年3月,中美华东向CDE递交注射用HDM2005的临床试验申请获受理,并于近日获得NMPA批准,同意本品开展临床试验。
ADC赛道竞争激烈,华东医药积极布局
近年来国内ADC赛道日渐拥挤,新药研发如火如荼。华东医药也积极投身其中,公司首个全自研的小分子抗肿瘤药物、首个全自研的HPK-1 PROTAC(造血祖激酶1蛋白降解靶向嵌合体)药物HDM2006已进入IND研究阶段,拟用于晚期实体瘤和血液瘤的单药和联用治疗,预计于2024年底递交IND申请。据药融云数据库显示,目前,华东医药有15款1类新药申请并获批临床。

截图来源:药融云中国药品审评数据库
据药融云数据库显示,目前有17款在研的靶向ROR1抗癌药物,其中3款ADC药物。进入临床的除 HDM2005外,仅3款。进展最快的是默沙东的 Zilovertamab Vedotin,已进入III 期临床阶段。
全球3款进入临床阶段 ROR1 ADC
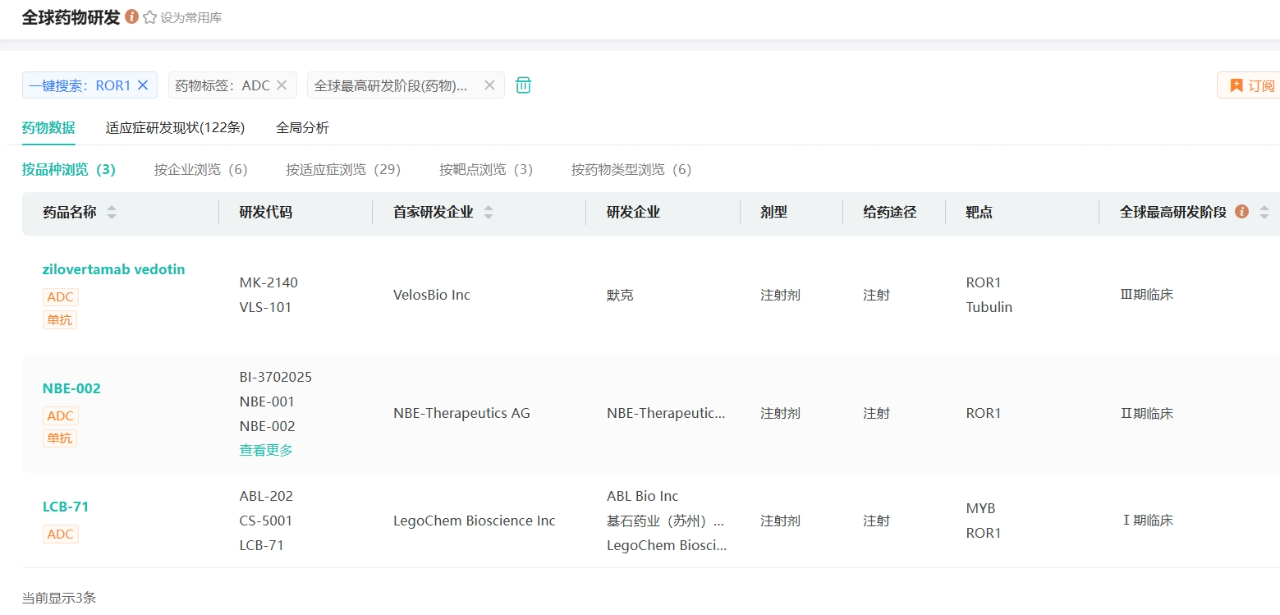
截图来源:药融云全球药物研发数据库
截至2023年,公司创新产品管线已超60项,6款创新产品有望于2024年迎来成果收获期,分别是2024年年初获批上市的CAR-T产品泽沃基奥仑赛注射液(商品名 赛恺泽®)以及处在上市冲刺关键阶段的ARCALYST两款适应症、ELAHERE®、塞纳帕利和乌司奴单抗。
小结
本次注射用HDM2005临床试验获批,是该款产品研发进程中的重要里程碑,将进一步提升公司在ADC肿瘤治疗领域的核心竞争力。公司后续将继续全力推进该款产品的临床及注册工作,争取为临床患者提供更多的治疗选择。
参考来源:
[1] 华东医药官方公告
[2] 药融云数据库
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)


















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论