
解读全球新药研发进展与趋势,剖析仿制药产品竞争力与市场前景,洞察医药资本脉络,尽在《药融云医药行业观察周报》。据《药融云医药行业观察周报》数据统计,在2023.09.11-2023.09.17期间,共有94个创新药/改良型新药注册申请获CDE承办(按受理号统计,不含补充申请)。其中,国产药品受理号71个,进口药品受理号23个。
同时,在这期间共计32款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药14款,生物药16款,中药2款。
获批临床的品种以1类新药为主,其中值得关注的有:康方生物的AK132注射液、恒瑞医药的注射用SHR-A1912、诺诚健华的ICP-189片、信达生物的IBI334、康德赛医疗的CUD002 注射液等。
1. AK132注射液
康方生物的AK132注射液获得临床试验默示许可,拟用于治疗晚期恶性肿瘤。公开资料显示,AK132注射液是一种可以同时阻断CLDN18.2和CD47的双特异性抗体药物。
AK132独特的结构设计降低了对CD47的亲和力,减少了抗体与红细胞的结合,有望降低临床上贫血发生的可能性,并且可特异性靶向肿瘤双表达的CLDN18.2和CD47,提高对实体瘤的靶向性,逆转肿瘤对髓系细胞的先天免疫抑制。
药融云数据库显示,这是康方生物的第6个双抗IND,此前已有的双抗产品包括已上市的PD-1/CTLA-4双抗卡度尼利,以及已提交上市申请的PD-1/VEGF双抗依沃西,PD-1/LAG-3双抗AK129,全球唯一且在研的TIGIT/TGF-β双功能融合蛋白AK130、PD-1/CD73双抗AK131、Claudin18.2/CD47双抗AK132等全球领先双抗均已进入临床。
康方生物研发管线进度查询
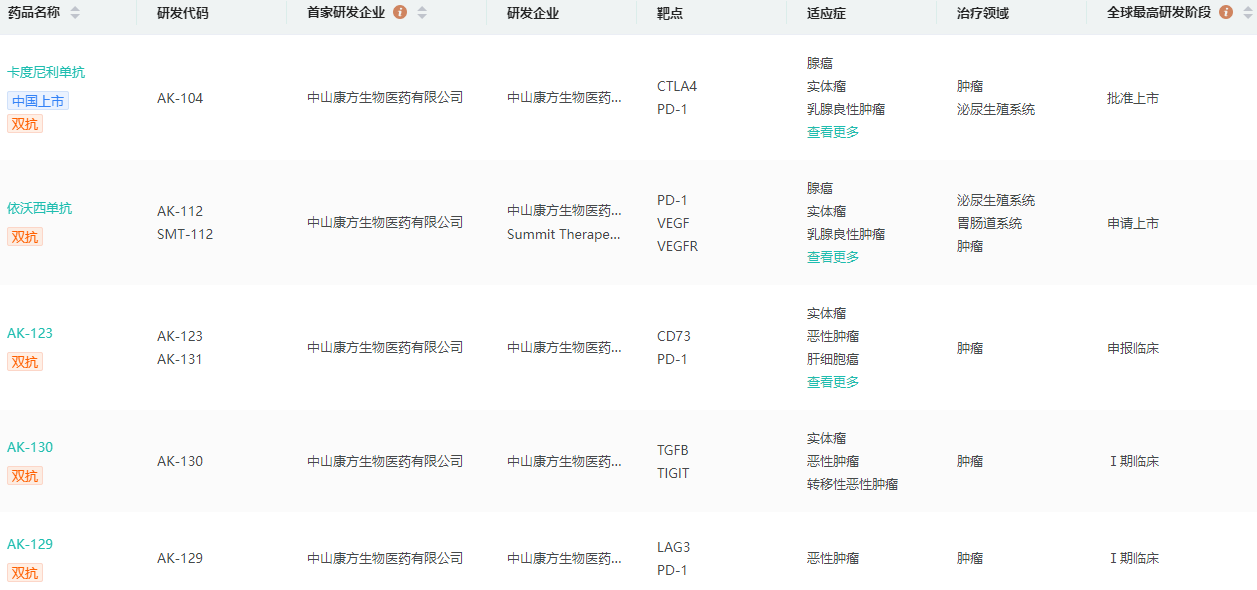
图片来源:药融云全球药物研发数据库
2. 注射用SHR-A1912
恒瑞医药靶向CD79b的ADC药物注射用SHR-A1912获批临床(受理号:CXSL2300453),拟联合含利妥昔单抗的治疗方案用于初治或复发难治的B细胞非霍奇金淋巴瘤。
近年来,恒瑞医药积极布局ADC领域,8款药物处于获批临床及以上阶段。药融云数据库显示,其中靶向HER2的SHR-A1811进度最快,目前处于III期临床;此外,6款药物在国内处于临床I期,包括SHR-A1201(Kadcyla类似物)、SHR-A1403(靶向MET),以及SHR-A1904(靶向Claudin 18.2)、SHR-A1912(靶向CD79b)、SHR-A2102(尚未披露靶点)等。
恒瑞医药ADC管线布局查询(部分)

图片来源:药融云全球药物研发数据库
3. ICP-189片
诺诚健华的SHP-2抑制剂ICP-189片获批临床,拟用于治疗晚期实体瘤以及联合甲磺酸伏美替尼片用于治疗EGFR突变的局部晚期或转移性非小细胞肺癌。
ICP-189片是诺诚健华研发的1类新药,是一种强效口服SHP2变构抑制剂,相对其他磷酸酶具有优选性。它是为了治疗实体肿瘤而开发,可用作单药疗法及╱或结合其他抗肿瘤药的联合疗法,旨在为肺癌、头颈癌及消化道肿瘤等实体瘤提供新的临床治疗方法。
ICP-189片获批临床-审评时间轴
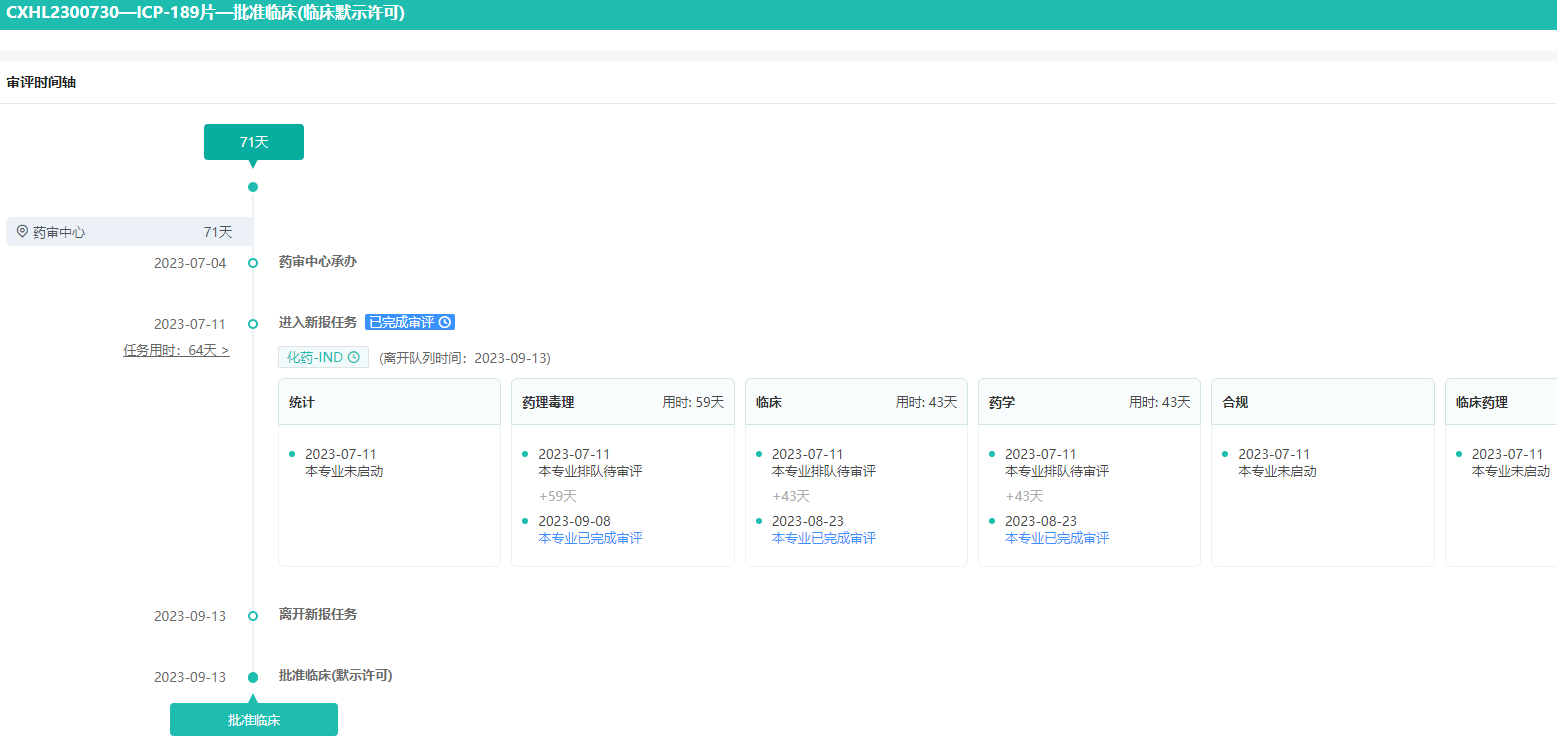
图片来源:药融云中国药品审评数据库
SHP2是一种非受体蛋白酪氨酸磷酸酶,主要在多种组织的细胞质中广泛表达,属于蛋白酪氨酸磷酸酶(PTP)家族。研究表明,SHP2的失调与异常的细胞增殖、分化、粘附迁移和凋亡有关,使得SHP2成为癌症治疗的有潜力的治疗靶点。
截至目前,针对SHP2靶点尚无药物批准上市,多种不同作用模式的SHP2抑制剂已被成功开发,其中一些已经处于临床试验阶段。其中,进展较快的有诺华研发的TNO-155和加科思的JAB-3068与JAB-3122、青峰药业的BR-790等,均处于Ⅱ期临床阶段;TNO-155是首款进入临床阶段的SHP2抑制剂,领跑SHP2赛道。
药融云数据显示,SHP2作为一个明星癌症靶点,吸引了国内外50多家药企布局研发,包括诺华、艾伯维、加科思、贝达药业、诺诚健华、豪森药业、奕拓医药、勤浩医药、凌达生物、君实生物等。
全球SHP2靶点研发管线进度查询
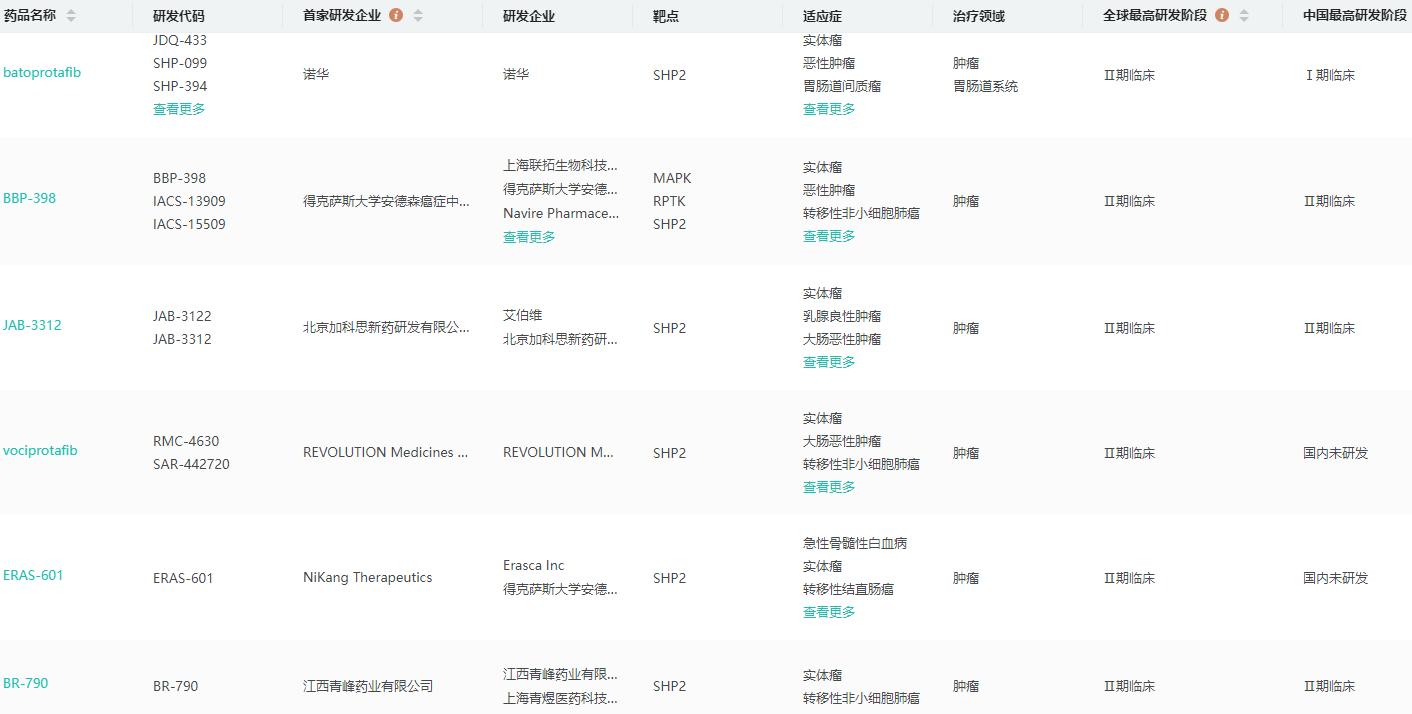
图片来源:药融云全球药物研发数据库
4. IBI334
信达生物1类新药IBI334获批临床,拟用于治疗不可切除、局部晚期或转移性实体瘤患者。IBI334是针对EGFR(表皮生长因子受体)和B7-H3两种靶点的双抗药物,一方面可以通过抑制EGFR信号阻断肿瘤细胞的增殖,另一方面通过阻断B7-H3信号激活T细胞,增强其对肿瘤细胞的攻击,也是全球首款此类药物。
信达生物是国内药企布局双抗的“大户”之一,药融云数据库显示,信达生物目前已有10款双抗新药进入临床阶段,其中进度较快的是IBI-303、IBI-318,已处于临床III期阶段;2款处于II期临床,6款处于I期临床。
信达生物研发管线靶点格局
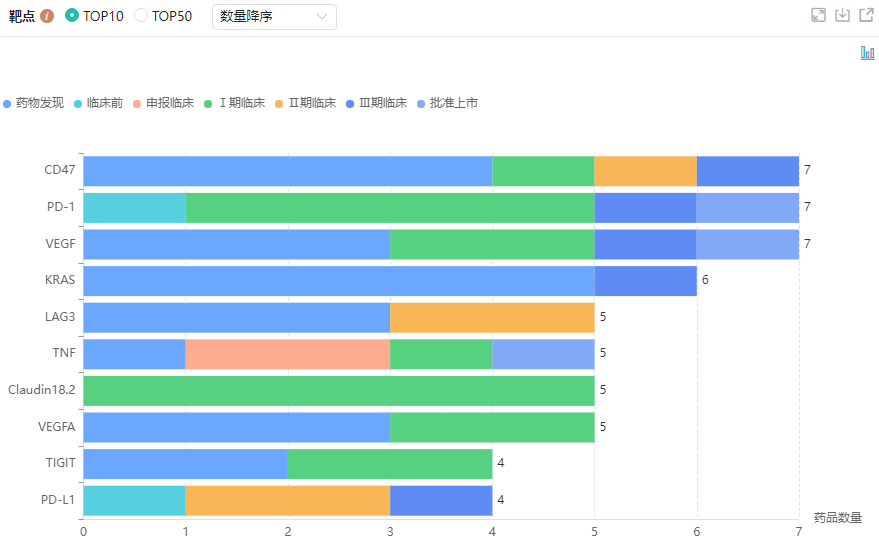
图片来源:药融云全球药物研发数据库
IBI-318是一款重组全人源IgG1抗PD-1/PD-L1双特异性抗体,其通过桥接表达PD-1的T细胞和表达PD-L1的肿瘤细胞,同时阻断PD-1和PD-L1的信号通路,增强免疫突触的形成,从而有望提高抗肿瘤活性及疗效,是全球首个进入临床阶段的PD-1/PD-L1双特异性抗体,由信达生物和礼来共同研发。
IBI-319也是由信达生物和礼来共同研发,是全球首款PD-1/4-1BB(CD137)双抗,临床前的各项研究结果均显示,IBI319具有靶点明确、药物稳定性好等特点,保留了PD-1的药效活性;并同时激活CD137的信号,协同增强药效。
<END>
想要获取完整报告内容,请关注“药融云”公众号,后台回复“报告”关键词进行领取;或者前往药融云“药融文库”网站【原创报告】栏目进行全文下载。























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论