
创新药的研发可以为目前无法治愈或治疗难度较大的疾病提供新的治疗手段,从而帮助患者获得更好的健康和生活质量;创新药的研发可以预防一些疾病的发生,例如疫苗等,从而降低人们患病的风险;创新药的研发可以推动医疗技术和医疗设备的发展,使医疗水平不断得到提高。全球新药研发的发展也直接影响着人类防病治病的质量和进程。
近年来,中国医药改革持续深化,政策驱动之下,越来越多企业开始创新药布局,对于全球新药研发进展的关注也愈发强烈。关注《药融云医药行业观察周报》,获取最新全球创新药研发进展。
根据药融云数据统计,2023.07.31-2023.08.06期间全球共有18款创新药研发获新进展,涉及骨质疏松症、肿瘤、慢性炎症疾病、肝癌等众多适应症,力图为其治疗领域带来新发展和新选择。
1. 泽璟制药CD3×DLL3×DLL3三抗获批临床
近期,泽璟制药宣布其三特异性抗体注射用ZG006(CD3×DLL3×DLL3)用于治疗晚期实体瘤的临床试验申请获得中国国家药监局(NMPA)批准。
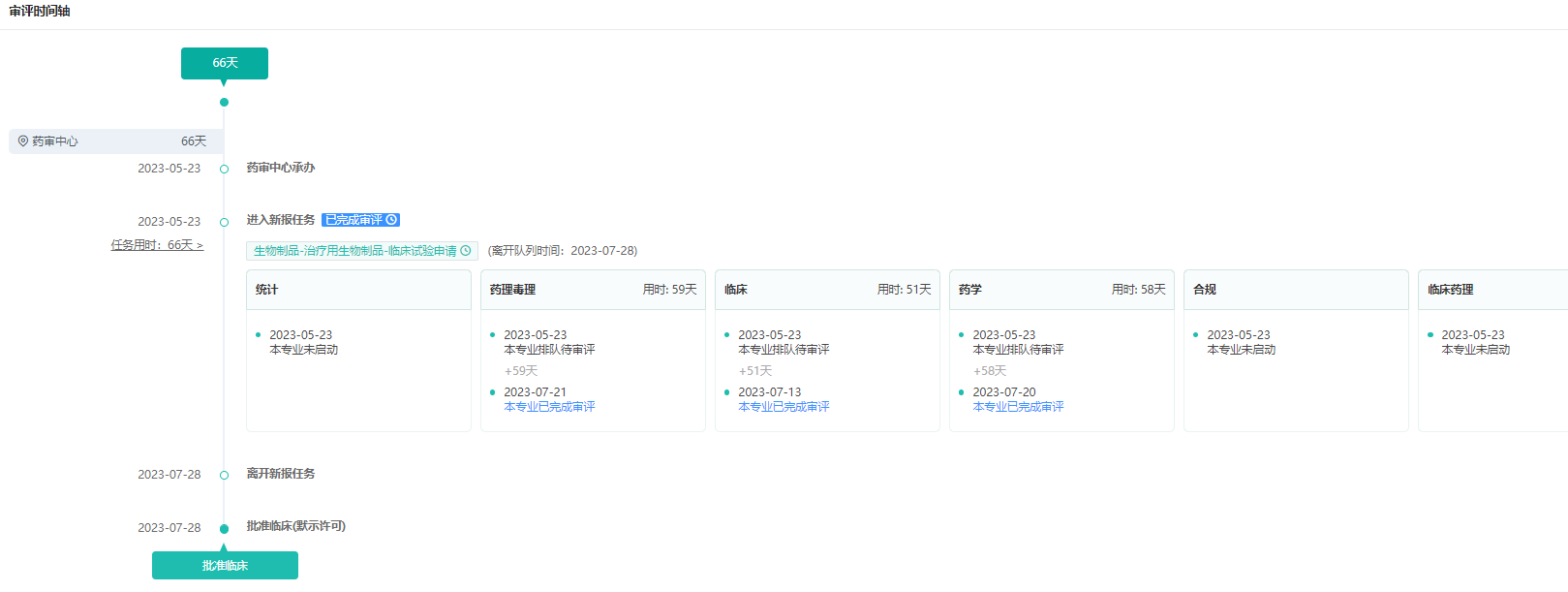
截图来源:药融云中国药品审评数据库
公开资料显示,ZG006是一款针对DLL3表达肿瘤的三特异性抗体,此前已经在美国获批临床,目标适应症为小细胞肺癌和其它实体瘤。研究发现,DLL3中文全称为delta样典型Notch配体3,在大约85%的小细胞肺癌和大细胞神经内分泌癌患者的肿瘤细胞表面表达。
另外,它还于多形性胶质母细胞瘤、黑色素瘤、胰腺癌和直肠癌等癌细胞中高表达,但在健康组织中表达较少。DLL3的肿瘤表达特异性使其成为了治疗小细胞肺癌等肿瘤的潜力靶点之一。ZG006是一种针对CD3及两个不同DLL3表位的三特异性抗体。它的抗DLL3端与肿瘤细胞表面不同DLL3表位相结合,抗CD3端结合T细胞,通过衔接肿瘤细胞和T细胞,将T细胞拉近肿瘤细胞,从而利用T细胞特异性杀伤肿瘤细胞。
2. 肝癌一线治疗!恒瑞医药“双艾”组合上市申请获FDA受理
7月31日,恒瑞医药发布新闻稿称,该公司提交的注射用卡瑞利珠单抗(艾瑞卡)联合甲磺酸阿帕替尼片(艾坦)(“双艾”组合)用于不可切除或转移性肝细胞癌患者的一线治疗的生物制品许可申请(BLA)获得了美国FDA正式受理。
肝癌为全球高发肿瘤,死亡率较高。肝细胞癌的治疗根据疾病分期而选择不同疗法,晚期肝细胞癌的治疗以系统性抗肿瘤治疗为主,包括分子靶向治疗、含奥沙利铂化疗和免疫检查点抑制剂及其联合治疗,近年来治疗上的进步在一定程度上提高了晚期肝细胞癌患者的生存,但是仍不能令人满意,还有较大的提升空间,亟需更多有效的治疗方案和药物。
卡瑞利珠单抗是恒瑞医药研发的人源化PD1单克隆抗体,于2019年5月在中国获批上市,此前已在肺癌、肝癌、食管癌、鼻咽癌以及淋巴瘤五大瘤种中获批了9个适应症。
卡瑞利珠单抗适应症查询(部分)
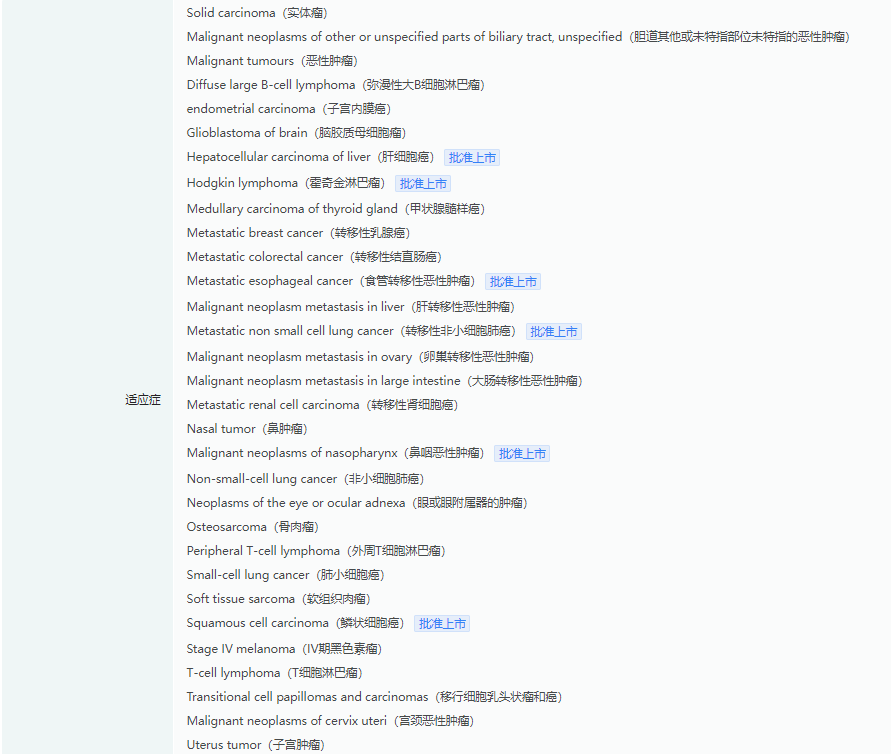
截图来源:药融云全球药物研发数据库
阿帕替尼是恒瑞医药开发的一款针对血管内皮生长因子受体(VEGFR)的小分子酪氨酸激酶抑制剂,于2014年10月在中国获批上市,目前有3个适应症获批,分别为单药用于晚期胃腺癌或胃-食管结合部腺癌、既往接受过至少一线系统性治疗后失败或不可耐受的晚期肝细胞癌、联合卡瑞利珠单抗用于不可切除或转移性肝细胞癌。
阿帕替尼适应症查询(部分)
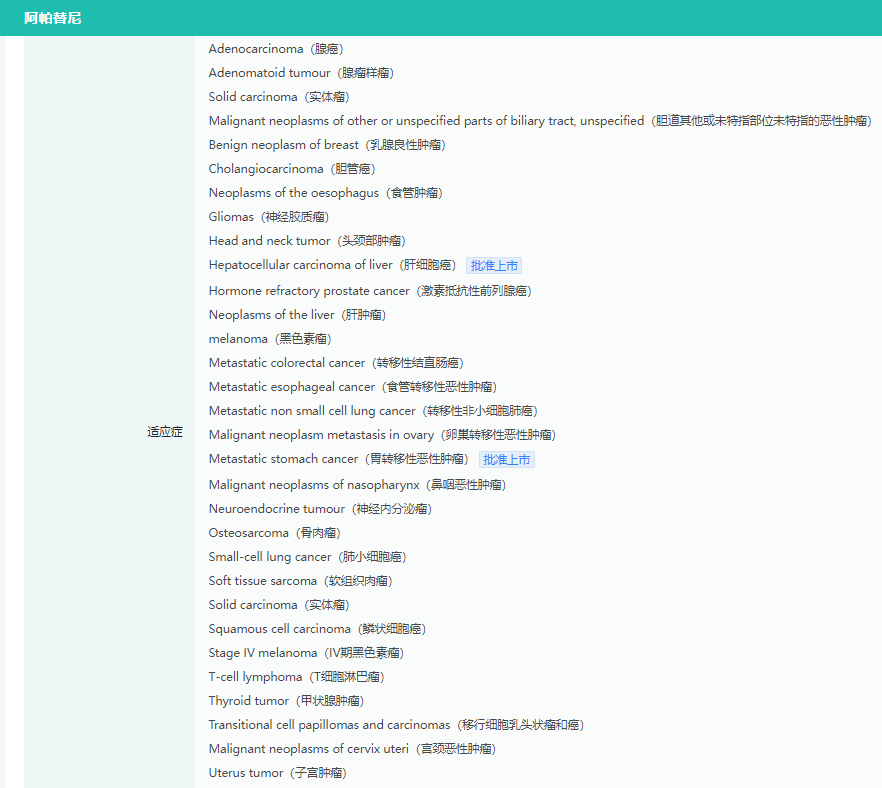
截图来源:药融云全球药物研发数据库
2021年4月,卡瑞利珠单抗联合阿帕替尼一线治疗不可切除或转移性肝细胞癌适应症获得FDA孤儿药资格。
3. 康方生物PD-1/VEGF双抗「依沃西单抗」申报上市
8月1日,中国国家药监局药品审评中心(CDE)官网最新公示,康方生物PD-1/VEGF双抗依沃西单抗已递交新药上市申请并获得受理。
依沃西单抗(AK112/SMT112)是康方生物研发的PD-1/VEGF双特异性抗体。基于该公司Tetrabody技术设计,依沃西单抗可阻断PD-1与PD-L1和PD-L2的结合,并同时阻断VEGF与VEGF受体的结合。鉴于VEGF和PD-1在肿瘤微环境中的共表达,与联合疗法相比,该产品作为单一药物同时阻断这两个靶点,可能会更有效地阻断这两个通路,增强抗肿瘤活性;与联合疗法相比,依沃西单抗安全性优势显著,与VEGF靶点相关的毒副作用大幅度降低。
依沃西单抗全球研发进度查询

截图来源:药融云全球药物研发数据库
目前,依沃西单抗在全球范围内已启动/正在开展多项关键注册性3期临床研究,其中3项是以抗PD-1单抗为阳性对药物的头对头研究。这些试验针对适应症包括:EGFR突变的nsq-NSCLC、PD-L1表达阳性NSCLC一线治疗、晚期鳞状NSCLC一线治疗等。
4. 加科思KRAS抑制剂又一适应症拟纳入突破性治疗品种
7月31日,中国国家药监局药品审评中心(CDE)官网公示,加科思申报的1类新药JAB-21822(格来雷塞,glecirasib)又一适应症拟纳入突破性治疗品种,拟用于治疗既往经过吉西他滨联合白蛋白紫杉醇或FOLFIRINOX方案治疗后出现疾病进展的KRASG12C突变的局部晚期或转移性成人胰腺癌患者。
JAB-21822研发进度查询

截图来源:药融云全球药物研发数据库
胰腺癌是一种恶性程度极高的肿瘤,目前患者缺少标准治疗手段,五年总生存率仅为5%,大约90%的胰腺癌患者带有不同类型的KRAS突变。KRAS是人类癌症中常出现突变的致癌基因之一,它的突变不仅能直接促进肿瘤细胞的增殖和生存,还能够对肿瘤微环境产生影响。研究显示,KRAS基因突变存在于多种肿瘤中,其中G12C突变主要存在于肺癌、结直肠癌和胰腺癌,因此KRASG12C抑制剂有望成为这类肿瘤患者的有效治疗手段。
作为一种KRASp.G12C共价抑制剂,JAB-21822可以将KRASp.G12C锁定在非活化状态,阻断KRAS向下游的信号转导,从而发挥抗肿瘤作用。
<END>
想要获取《药融云医药行业观察周报》完整报告内容,请关注“药融云”公众号,后台回复“报告”关键词进行领取;或者前往药融云“药融文库”网站【原创报告】栏目进行全文下载。

















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论