
11月11日,上海葆隆生物和亚邦生物联合递交的罂粟乙碘油注射液上市申请CDE受理,这是本月该品种第2家报产的企业。目前国内该药由恒瑞医药独家生产。
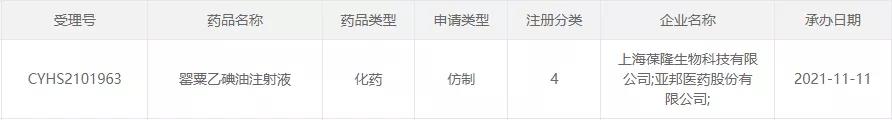
图片来源:CDE官网
罂粟乙碘油为非水溶性造影剂,是一种特殊的、更具优势的碘化油。注入体内后能比周围软组织结构吸收更多X线,从而在X线照射下形成密度对比,显示出所在腔道的形态结构,适用于淋巴造影、肝细胞癌造影、子宫输卵管造影等。
全球首个碘化造影剂为法国药企加柏大药厂(Guerbet)公司开发的碘化油注射液,最早于1954年3月获美国FDA批准(商品名:Lipiodol),临床上用于成人输卵管造影、成人和儿童淋巴系统造影和患有未知肝细胞癌的成人患者肝动脉造影。目前该药已在全球多个国家上市,我国于2001年8月批准法国加柏公司的碘化油注射液进口。
据药融云中国批文数据库,国内目前有3家企业生产碘化油注射液,包括1家进口原研厂家和2家国内药企(上海旭东海普药业、烟台鲁银药业)。
碘化油注射液已获批文

图片来源:药融云中国药品批文数据库
据恒瑞医药公告,早前国产碘化油注射液与进口产品不同,多为未进行乙酯化的碘化核桃油或碘化豆油,而恒瑞医药仿制的罂粟乙碘油注射液与进口产品主要活性成分一致,为碘化罂粟籽油脂肪酸乙酯,具有超液态、杂质少、不饱和脂肪酸含量高的特点,是一种特殊的、更具优势的碘化油。
恒瑞医药的罂粟乙碘油注射液最早于2016年10月按6类获批上市,于2021年9月以仿制3类获批上市,视同通过一致性评价,为该品种首家。据药融云统计,2020年罂粟乙碘油注射液斩获近1.5亿元的院内销售额,今年上半年同比增长178%,销售额已超1亿。目前该药的适应症包括:
- 用于碘缺乏病的治疗;淋巴造影(首次获批适应症)
- 成人肝细胞癌中期患者的动脉化疗栓塞治疗(2020年1月新增)
- 用于子宫输卵管造影(2021年9月新增)
恒瑞医药罂粟乙碘油注射液院内销售情况
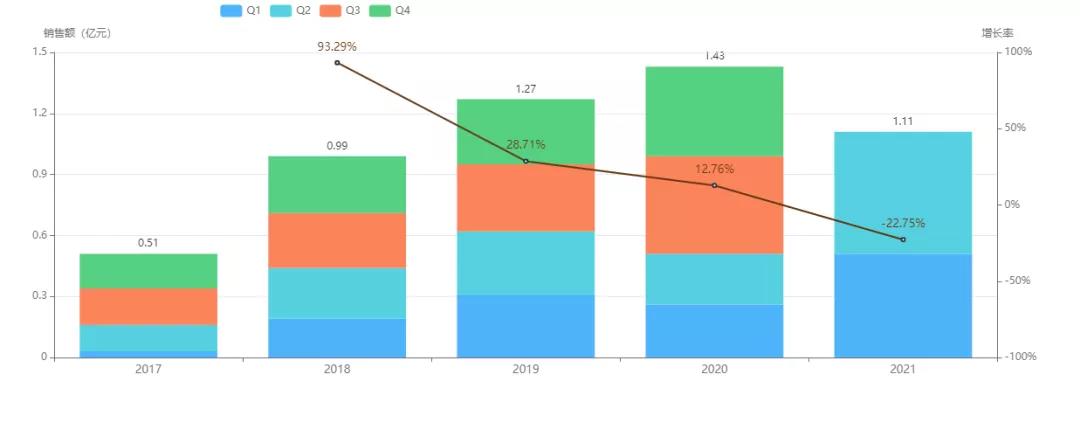
图片来源:药融云全国医院销售数据库
恒瑞医药罂粟乙碘油注射液以仿制3类获批2个月后,2021年11月3日,烟台鲁银药业以仿制4类递交了罂粟乙碘油注射液的上市申请,成为该品种第2家报产的企业;11月11日,上海葆隆生物/亚邦生物递交上市申请。
—END—






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论