- 2021.05.01-2021.05.20期间药审中心受理总量为502个,涉及品种343个。
- 71个1类新药申请临床获CDE受理。
- 新增49个按仿制药质量和疗效一致性评价品种申报的受理号。
- 53个品种通过(含视同通过)一致性评价。
- 6款国产新药获批上市:百济神州1类创新药帕米帕利胶囊获批上市
2021年5月16日至5月20日,6款国产新药、6款进口药,53个品种通过(含视同通过)一致性评价。恒瑞医药帕立骨化醇注射液等8款首仿获批上市,百济神州1类创新药帕米帕利胶囊重磅获批,详细信息如下: 6款国产新药获批上市
6个品种批准进口
过评品种信息
在审评审批阶段
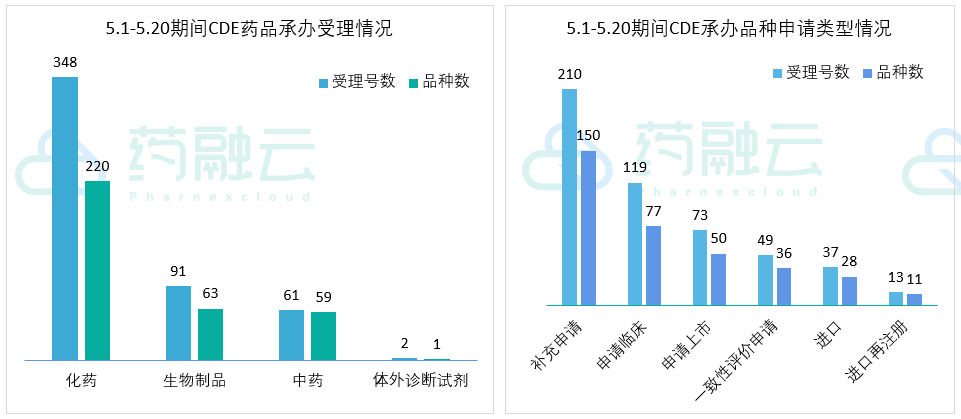
根据药融云中国药品审评数据,5月1号-5月20号期间共343个(按品种计,下同)药品获CDE承办,包括化药230个,生物制品63个,以及中药59个。
近期CDE承办的共有77个品种申报临床,其中包括58款国产新药,另有36个品种提交一致性评价。
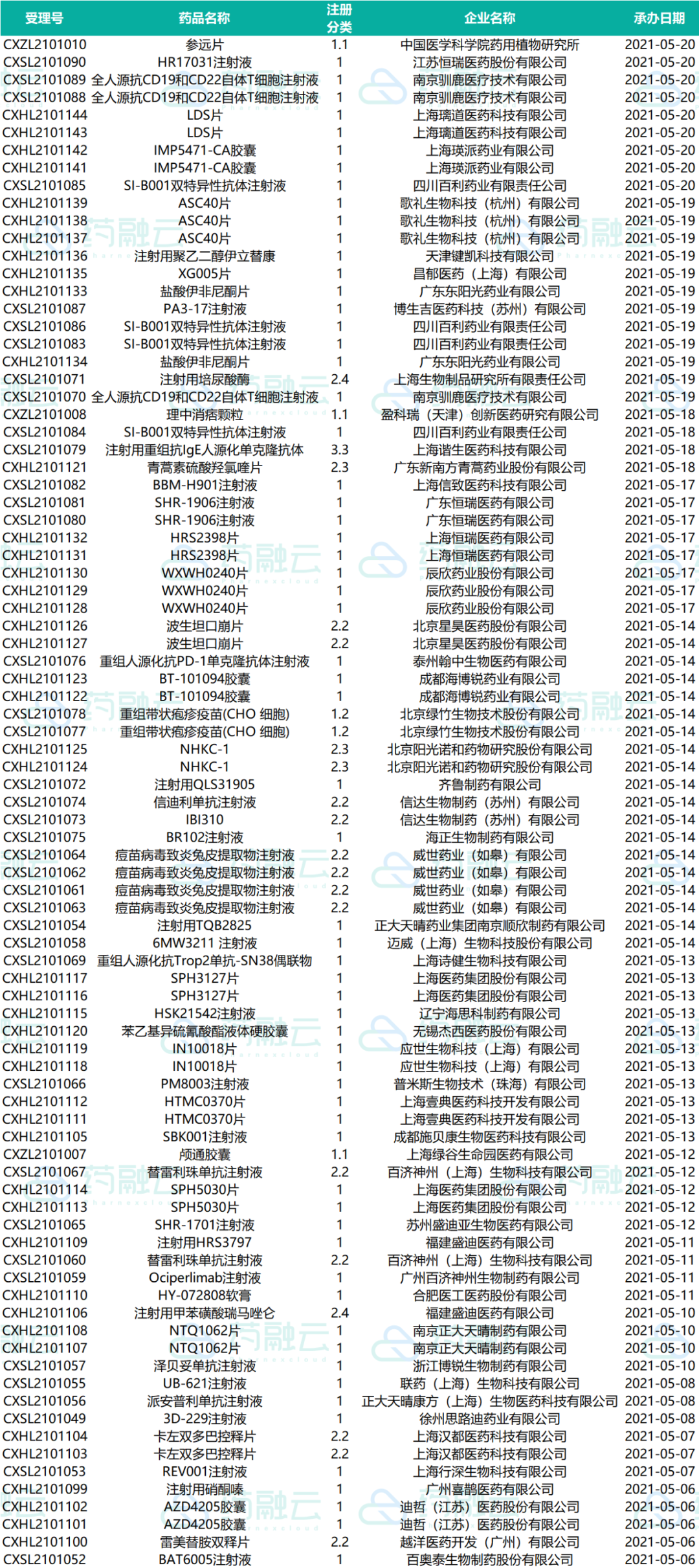
近期受理国产新药共计97个受理号,涉及65个品种59家企业,其中上海璎黎药业的林普利司片、上海倍而达药业的甲磺酸瑞泽替尼胶囊等8款新药提交上市申请,其余均为申请临床,这其中包括46款1类新药申请。
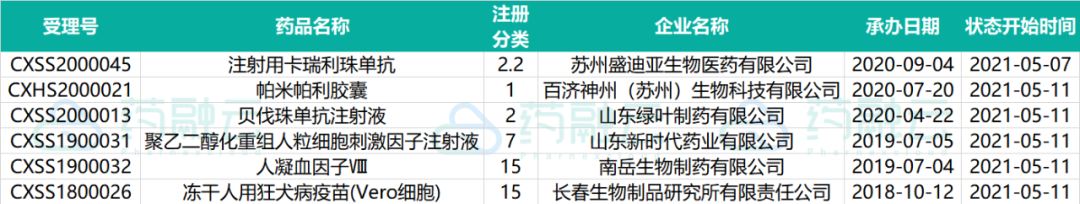
下表为2021.05.01-2021.05.20申请上市的药物情况
下表为2021.05.01-2021.05.20申请临床的新药药物情况
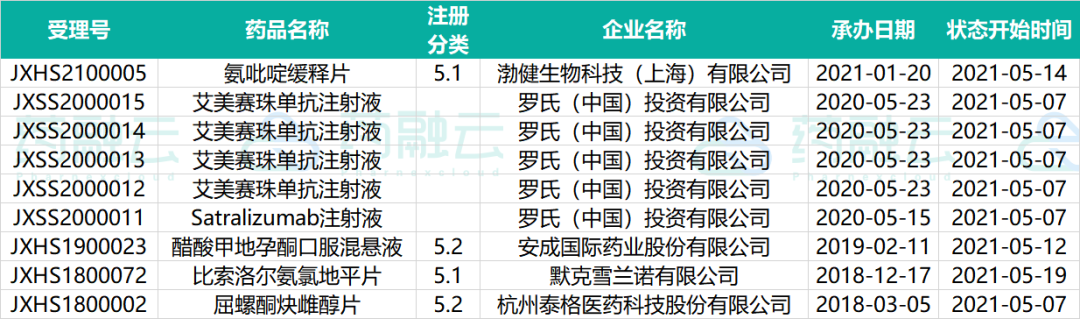
下表为2021.05.01-2021.05.20申请临床的进口药物情况
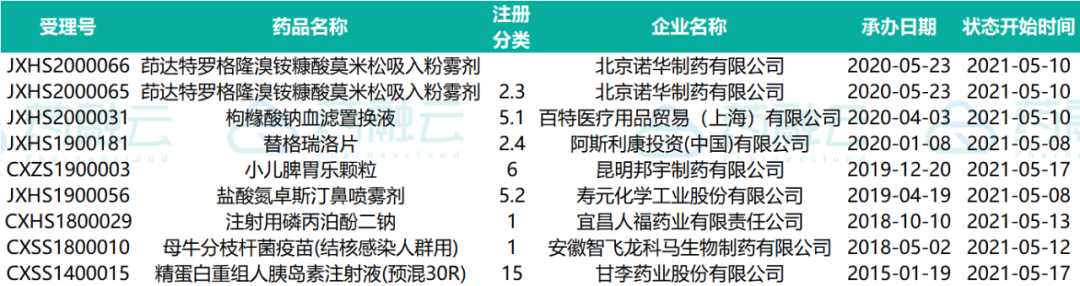
下表为2021.05.01-2021.05.20申请进口的进口药药物情况
在审批阶段
近期共有51个品种(73个受理号)进入审批阶段。
2021.05.01-2021.05.20在审批阶段进口和新药药物情况
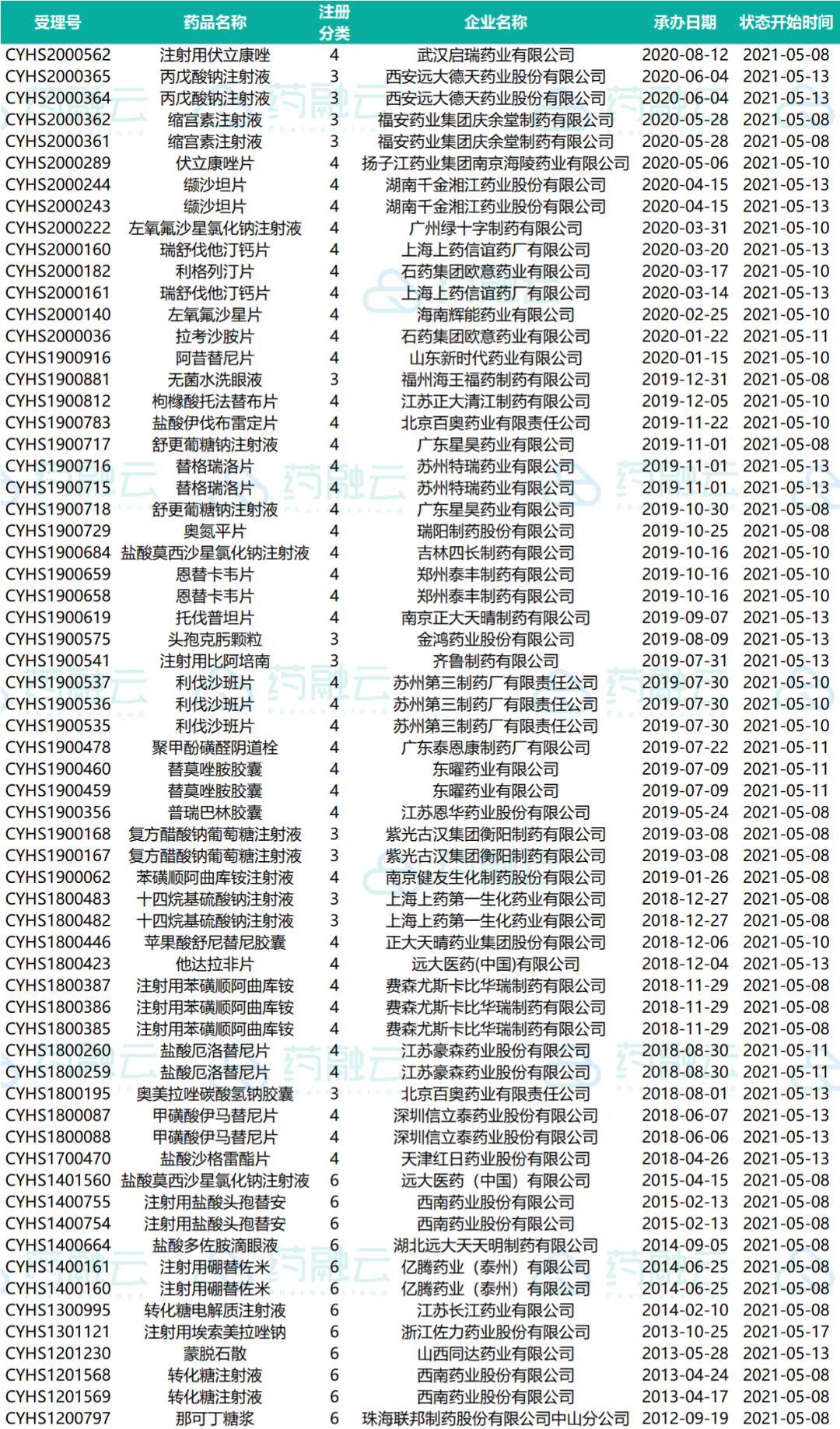
2021.05.01-2021.05.20在审批阶段仿制药药物情况
制证完毕-待发批件
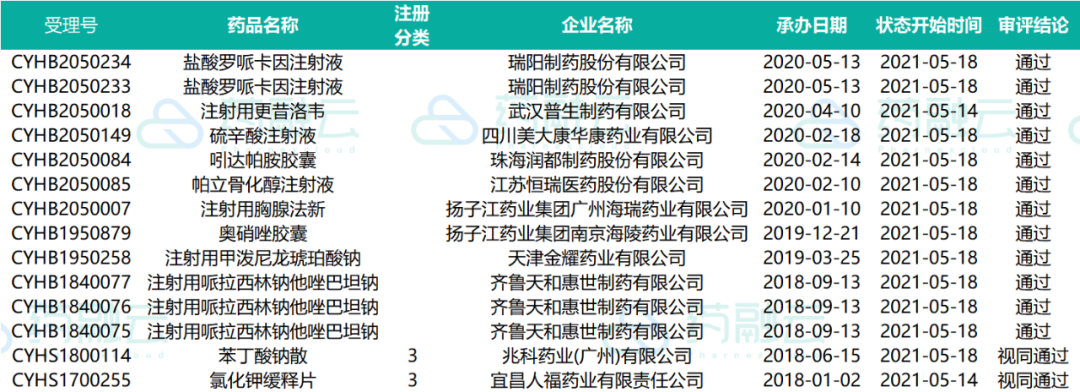
近期共计59个品种(涉及受理号91个)制证完毕-待发批件。下表是处于制证完毕-待发批件的过评药物情况。
2021.05.01-2021.05.20制证完毕-待发批件过评药物情况
一致性评价申请
近期有36个品种提交一致性评价申请。



















收藏
登录后参与评论