
CAR-T细胞的制备流程复杂(图1)[1],从T细胞的富集、分化、扩增,通过病毒载体进行CAR基因转移,然后再进行体外CAR-T细胞扩增,最终制成细胞产品。目前大部分CAR-T细胞的制备都是以慢病毒载体为主,病毒载体是决定CAR-T细胞能否成药的关键一环。
面对逐渐复杂的CAR转基因序列和细胞工艺,阳性对照成为了工艺开发过程中的重要工具,不仅提升了实验的严谨性,更能帮助企业客户理解工艺流程及相关工艺参数,指导优化工艺,加速CAR-T细胞产品的开发进程。

▉ 谱新生物BlueKit®CD19 CAR-T现货慢病毒
BlueKit® CD19 CAR-T现货慢病毒简介
谱新生物通过引入第二代CAR-T技术(图2),利用HiLenti®慢病毒技术平台(图3),成功研发了一款在细胞层面表现良好的CD19 CAR-T慢病毒载体。客户无需再深陷复杂繁琐的慢病毒制备泥潭,即可直接利用这款现货产品,专注于核心细胞工艺的优化与创新。同时,该产品亦可作为宝贵的阳性对照,精准指导客户在细胞工艺开发过程中的每一步决策,从而显著加速整个开发流程,助力科研成果更快转化为临床应用。

图2:CD19 CAR-T现货慢病毒CAR结构示意图

图3:CD19 CAR-T现货慢病毒生产工艺流程图
BlueKit® CD19 CAR-T现货慢病毒质量标准
详见产品COA。
BlueKit®CAR-T现货慢病毒功能验证
谱新生物推出的CD19 CAR-T现货慢病毒产品,通过协同刺激结构域4-1BB,显著延长了CAR-T细胞的存活时间并强效促进了细胞增殖。在谱新生物CAR-T细胞生产工艺中,仅需培养10天,细胞的扩增倍数即可达到30倍左右。对于CAR阳性率,无论是否添加病毒转导增强剂,CD19 CAR-T现货慢病毒产品均能保证同时CD3+CAR+达到85%以上(如图4图所示)。
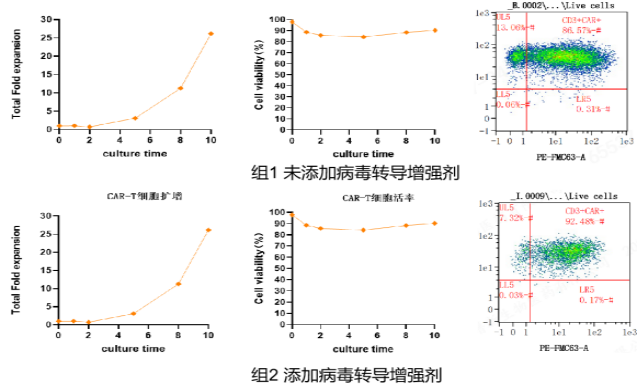
图4:CD19 CAR-T现货慢病毒细胞测试结果
▉ 结语
在细胞治疗领域,目的基因的递送方式是成败的关键。慢病毒载体(LVVs)凭借其大容量、低细胞毒性和低免疫原性、广泛感染能力、可实现稳定表达等优势,成为免疫细胞疗法中首选目的基因递送工具。然而,复杂的CAR结构设计与生产流程常导致高滴度、高效转导的慢病毒产品难以迅速产出,这严重制约了细胞工艺研究的进展。
为突破这一瓶颈,谱新生物推出了CD19 CAR-T现货慢病毒产品。该产品以VSV-G作为包膜,精准靶向并高效杀伤CD19阳性细胞。该慢病毒产品不仅病毒滴度高、杂质少,更在细胞层面展现出卓越的转染效率与CAR阳性率提升能力。作为阳性对照,此产品可以节约CAR-T细胞的工艺研发时间,加速概念验证数据(Proof-of-Concept,PoC)的获取。
参考文献:
1.Swiech, K., Malmegrim, K. C. R., & Picanço-Castro, V. (2020). Chimeric Antigen Receptor T Cells. Springer.
Related
相关产品信息及购买信息
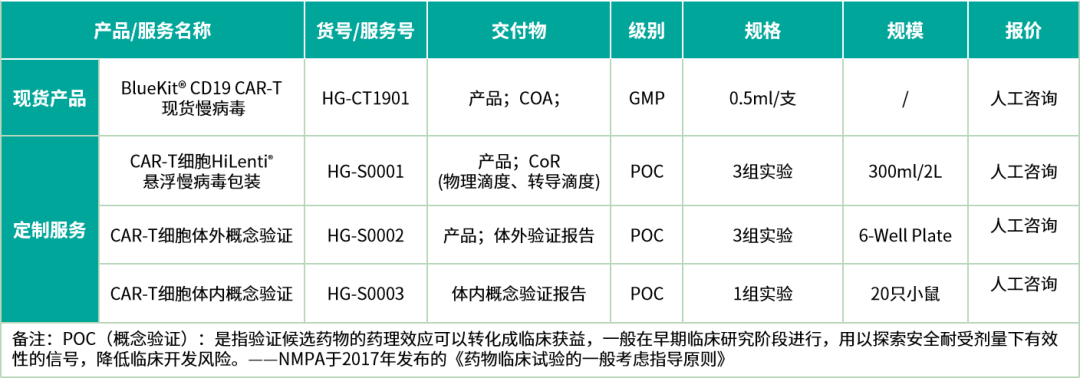
如果您对我们的产品及服务有订购需求或需要进一步的帮助,请扫描如下二维码,选择产品并填写您的信息。
电话咨询:400-900-1882
邮箱咨询:info@hillgene.com
表单咨询:扫描如下二维码,选择产品填写信息

关于谱新

(点击阅读原文可填写)



































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论