药融云中国药品审评数据库显示,近日恒瑞医药的碘佛醇注射液新增3个规格通过仿制药一致性评价(受理号:CYHB2151055、CYHB2151056、CYHB2151057)。数据库审评时间轴显示,从药审中心承办到通过一致性评价,碘佛醇注射液新增的3个规格过评耗时552天。
碘佛醇注射液一致性评价-审评时间轴
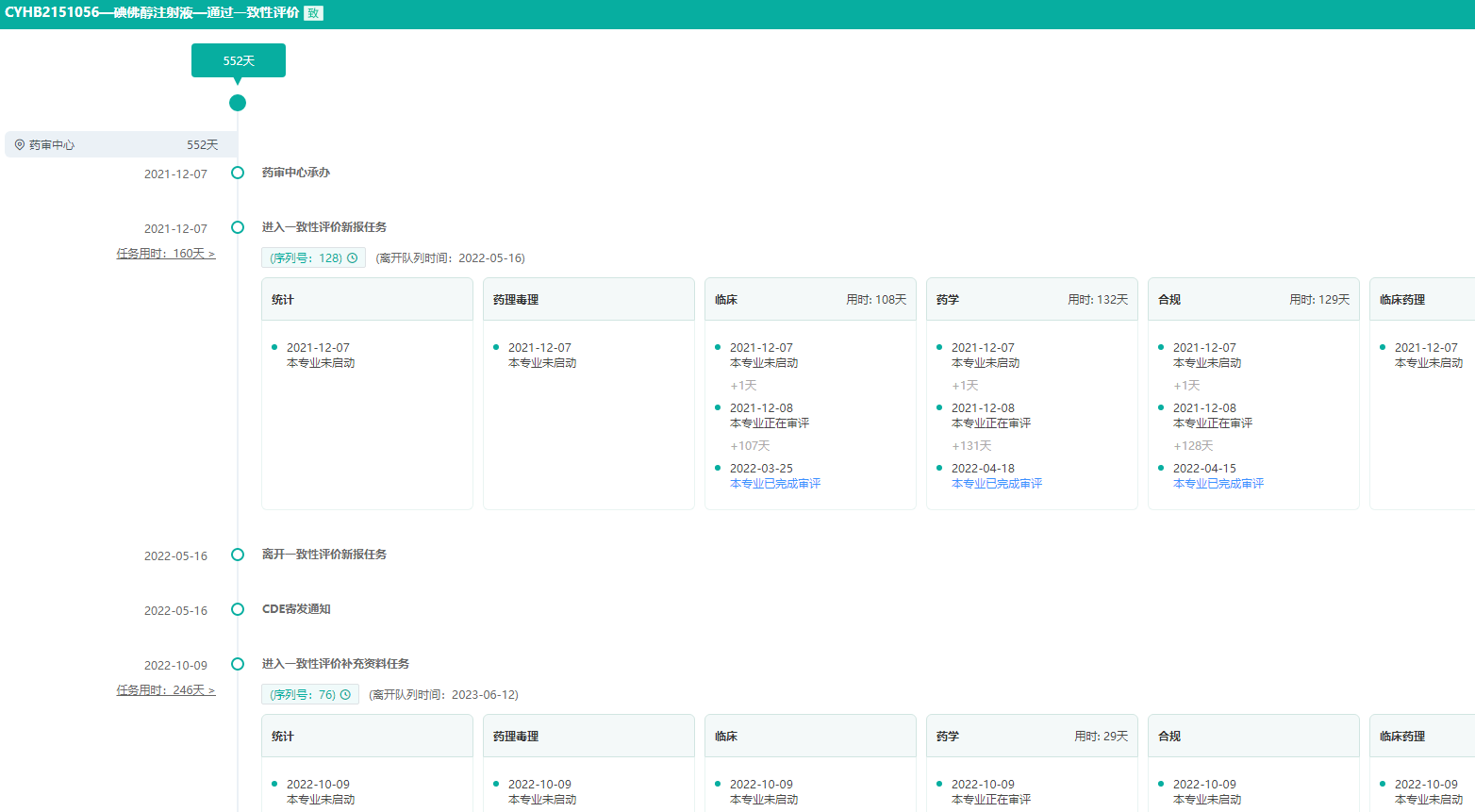
图片来源:药融云中国药品审评数据库
目前,恒瑞医药的碘佛醇注射液已有4个品规(100ml:74.1g,50ml:16g,100ml:67.8g,20ml:13.56g)通过了仿制药质量和疗效一致性评价,均是国内首仿。除此之外,司太立制药和倍特药业已提交上市申请,处于在审评审批阶段。
碘佛醇注射液是一种广泛应用于医学影像学的造影剂,具有高浓度、高渗透性和高价值的特点。其注射液中含有的碘元素可以迅速进入到人体内部的血管和组织中,使这些部位显示得更清晰、更鲜明。在医学影像诊断中,可用于增强影像对血管系统、肾脏和其他组织器官的诊断,以帮助医生做出准确的诊断和治疗决策。
碘佛醇注射液最早于1988年在美国获批上市,目前已在全球多个国家上市销售。药融云中国药品批文数据库显示,碘佛醇注射液在国内共有132条生产批文,其中在使用的仅25条,涉及3个生产企业,恒瑞医药、Guerbet SA、Liebel-Flarsheim Company LLC。
碘佛醇注射液生产批文查询(部分,完整内容请登录“药融云数据库www.pharnexcloud.com/?mh”查看)
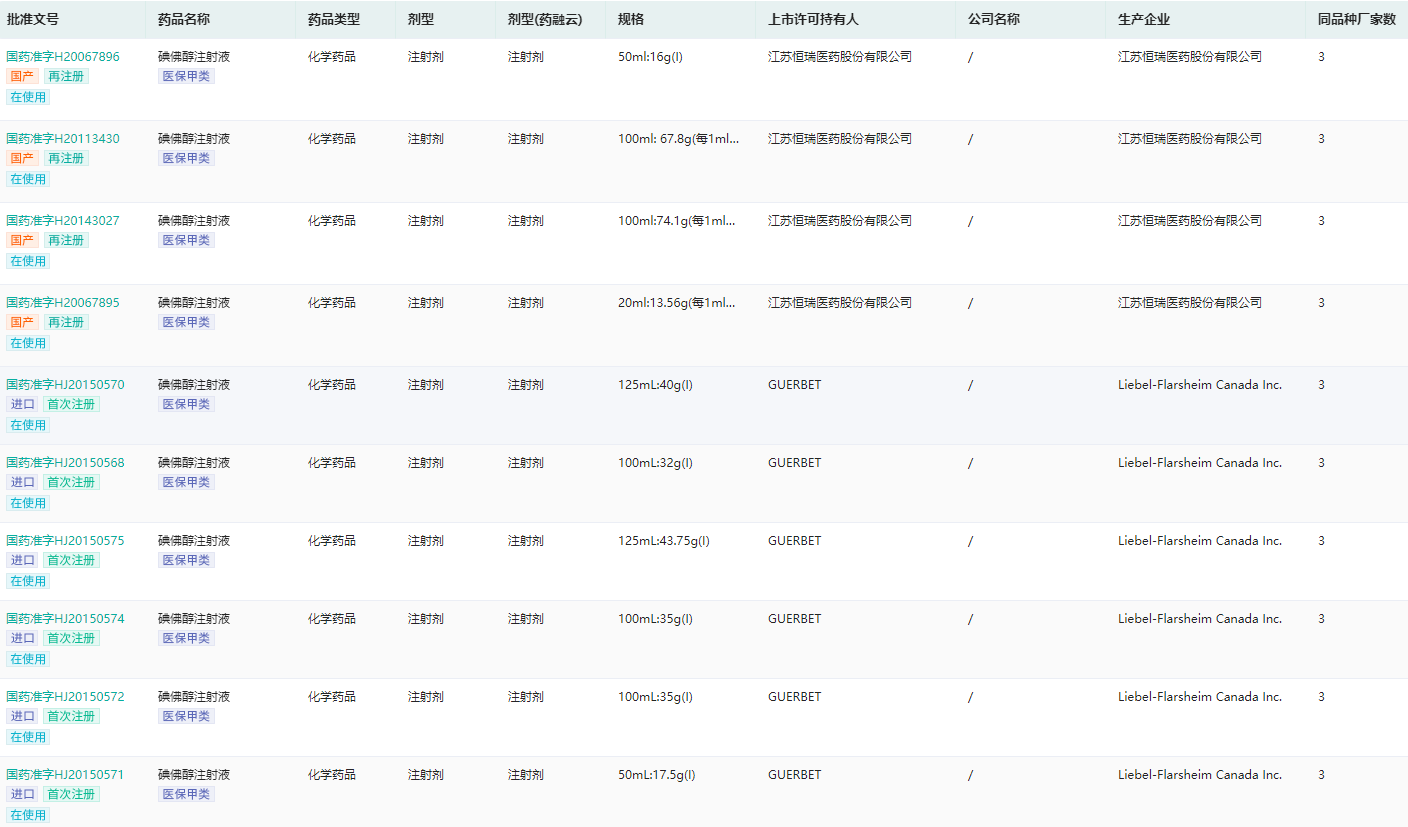
图片来源:药融云中国药品批文数据库
一、12个造影剂品种过评,恒瑞医药、司太立领跑!
截至目前,恒瑞医药已有5款造影剂过评,包括碘佛醇注射液、碘克沙醇注射液、罂粟乙碘油注射液、钆布醇注射液、钆特酸葡胺注射液,且均已进入医保目录。除了碘克沙醇注射液,其余4款造影剂均由恒瑞医药首家过评。
恒瑞医药过评造影剂查询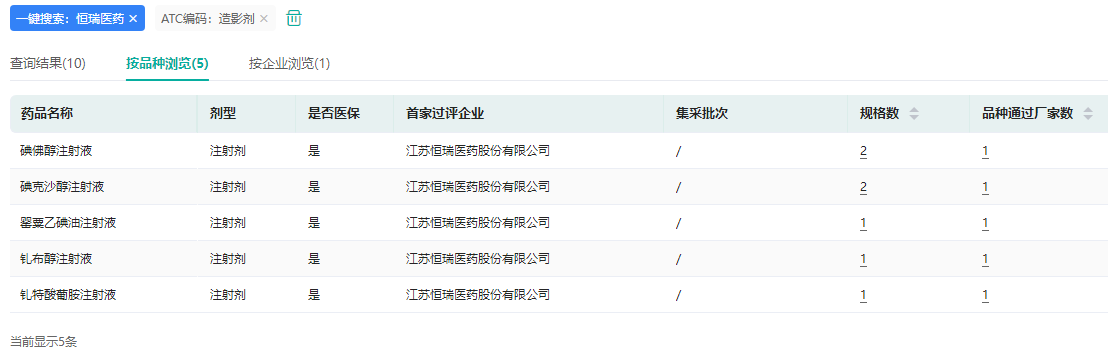
图片来源:药融云过评药品汇总数据库
药融云数据库显示,目前造影剂已有12个品种过评,首家过评方面,恒瑞医药和司太立制药领跑,分别拿下4个,其次是湖南科伦制药拿下2个,北陆药业和倍特药业各获得1个品种的首家过评。
其中,司太立制药首家过评的造影剂品种分别是碘美普尔注射液、碘克沙醇注射液、碘海醇注射液、碘帕醇注射液;湖南科伦的首家过评品种是钆塞酸二钠注射液,北陆药业的首家过评品种为钆喷酸葡胺注射液,倍特药业的为碘普罗胺注射液。
造影剂已过评品种信息查询
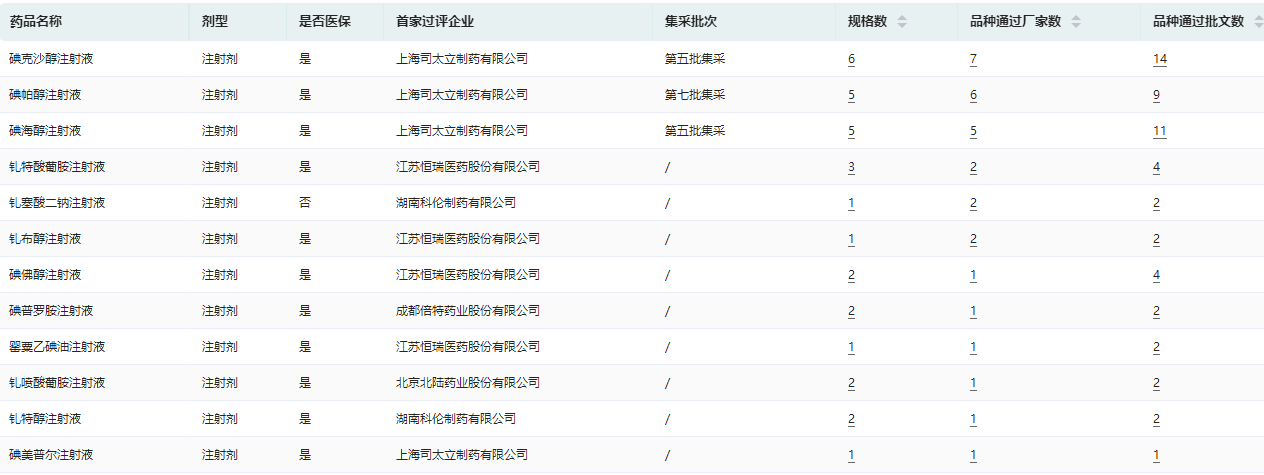
图片来源:药融云过评药品汇总数据库
已过评的造影剂品种中,碘克沙醇注射液是过评大户,过评企业最多,达到7家,包括扬子江药业、北陆药业、倍特药业、正大天晴、恒瑞医药、司太立制药、南京正大天晴制药。其次是碘帕醇注射液和碘海醇注射液,过评企业分别为6家、5家。这三个品种均已进入国家药品集采。此外,钆特酸葡胺注射液过评企业已达三家。
二、恒瑞医药品种登顶“销冠”,司太立跻身前十强!
药融云全国医院销售数据库显示,2021年全国医院端市场造影剂销售规模达到146.47亿元,同比增长14.66%;因受集采影响,2023年医院终端市场销售额下滑了23.09%。
其中,2022年医院端市场造影剂销售额TOP10品种中,排名前三的分别是碘佛醇注射液、碘克沙醇注射液、碘普罗胺注射液,分别占据了26.13%、16.74%、12.85%的市场份额。
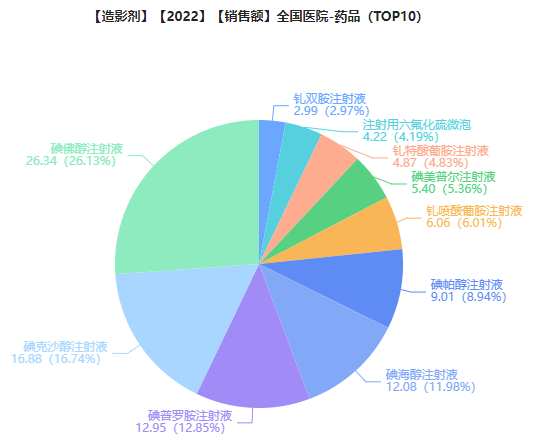
图片来源:药融云全国医院销售数据库
近年来,碘佛醇注射液在国内医院端的市场规模持续增长,2022年以26.34亿元的销售额从第三跃居榜首,同比增长19.88%;其中,恒瑞医药占据了93.02%的市场份额。
而碘海醇注射液跌落前三,排名第四,2022年医院端销售额为12.08亿元,同比下降52.14%。此外,在TOP20品种中,有16个产品销售额超过1亿元。
从生产企业格局来看,江苏恒瑞医药、拜耳、博莱科、扬子江药业、通用电气位居前五,占据了医院端78.67%的市场份额。从增长率来看,TOP10企业中有7个出现负增长,销量下滑最多的是通用电气,其次是扬子江药业;其中,上海司太立制药大涨136%,晋身前十强。
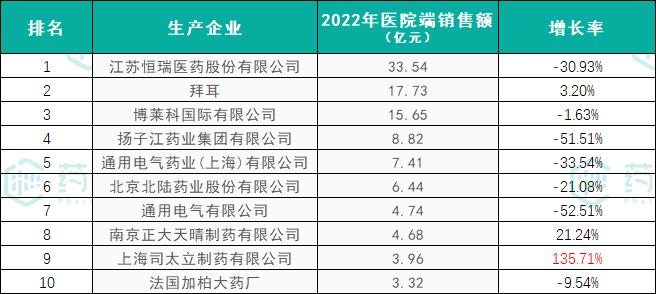
数据来源:药融云全国医院销售数据库
目前,造影剂在发达国家使用较早,市场已经成熟,使用量保持在一个较高的水平。对于以中国为首的新兴国家市场,由于市场规模尚小,加上经济快速增长、医疗设施逐渐完善、人民诊断需求等逐步提高,市场增长率高于发达国家。
受益于政策红利及人均可支配收入的增加,我国CT、MRI等医学影像设备保有量快速增长,同时造影剂市场规模迅速扩张。虽然与发达国家相比仍有较大差距,但相信在未来,医学影像设备及造影剂市场仍将保持高速增长,市场规模进一步扩大。
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论