2023年2月24日,科伦博泰生物提交港股上市申请招股书正式披露(740页,药融云公众号(yrydata)后台回复“科伦博泰”下载)。科伦博泰成立于2016年,专注于生物技术药物及创新小分子药物开发,重点关注肿瘤、自身免疫、炎症和代谢疾病等重大疾病领域。目前,公司拥有33个以上创新药在研产品,10多个项目进入临床研究阶段,其中抗PD-L1单抗(泰特利单抗注射液,KL-A167)已在中国申报上市,靶向TROP-2的ADC药物(SKB264)已经被中国国家药监局(NMPA)纳入突破性治疗品种。


截图来源:科伦博泰招股书披露
科伦博泰正在推进33款差异化且具有临床价值的资产创新药研发管线,其中14款处于临床阶段,此外有10款ADC药物处于临床前开发,创新实力十足。2022年科伦博泰与默沙东在ADC药物创新领域先后达成3笔BD交易,交易合计总金额已经超过118亿美元,首付款累计2.57亿美元。
科伦博泰与默沙东达成的3笔ADC药物交易
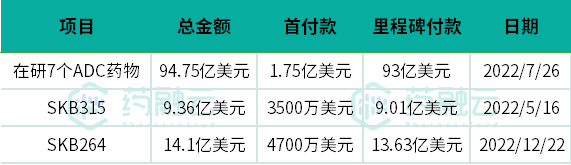
来源:药融云数据
根据此前公司发布的预案公告显示,科伦药业直接持有科伦博泰59.75%的股份,默沙东持有科伦博泰6.95%的股份,是科伦博泰的第二大股东。

截图来源:科伦博泰招股书披露
一、科伦博泰部分核心创新药在研管线分析
01.PD-L1单抗:泰特利单抗注射液(KL-A167)
泰特利单抗注射液是科伦博泰自主研发的靶向PD-L1的创新人源化单克隆抗体,通过特异性地与PD-L1结合,抑制PD-L1/PD-1的相互作用,解除PD-1/PD-L1信号通路介导的免疫抑制,促进T细胞的增殖和细胞因子的分泌,从而增强肿瘤免疫反应。
据药融云数据库显示,2021年11月19日,科伦博泰研发的PD-L1单抗,泰特利单抗注射液(产品代号:KL-A167),提交的上市许可申请,获得国家药品监督管理局药品审评中心注册受理,适应症为“适用于治疗既往接受过二线及以上化疗失败的复发或转移性鼻咽癌”。
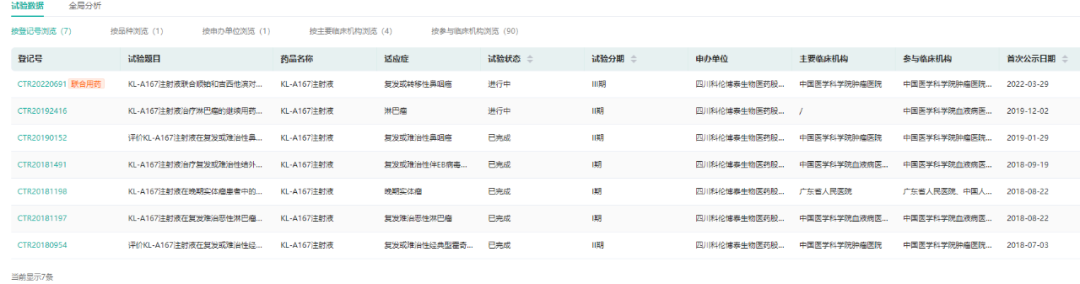
数据来源:药融云中国临床试验数据库
目前泰特利单抗注射液在国内开展了7项临床试验,适应症涉及包含鼻咽癌、淋巴瘤等多个癌种。在超级内卷的PD-1/L1领域,期待国产PD-L1新药的表现。
02.靶向TROP-2的ADC药物:SKB264
SKB264是一款TROP-2 ADC药物,使用了重组抗Trop-2人源化单抗,毒素使用的是拓扑异构酶Ⅰ抑制剂,二者由一个含2-(甲基磺酰基)嘧啶接头的连接子连接。
2023年1月29日,科伦药业公告其控股子公司科伦博泰与默沙东合作开发的创新TROP2-ADC(SKB264,MK2870),正式获得国家药品监督管理局(NMPA)药品审评中心(CDE)突破性疗法认定(BTD),用于EGFR-TKI治疗失败的局部晚期或转移性EGFR突变非小细胞肺癌(NSCLC),该项认定是基于SKB264的Ⅱ期拓展研究数据。此前SKB264用于治疗局部晚期或转移性三阴乳腺癌(TNBC)已被CDE纳入突破性治疗品种名单。截止目前,SKB264已经收获了两个突破性疗法认定。
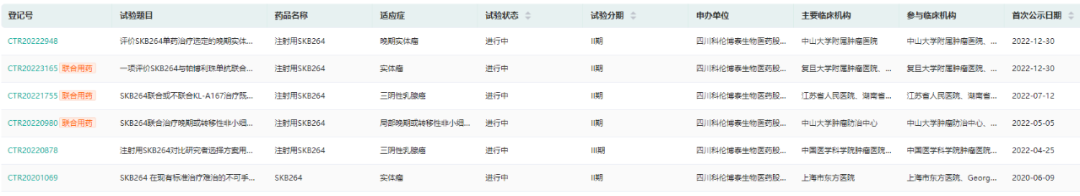
数据来源:药融云中国临床试验数据库
目前SKB264在中国和美国均开展了临床试验,针对多个瘤种的单药/联用的2期和3期临床试验正在推进。
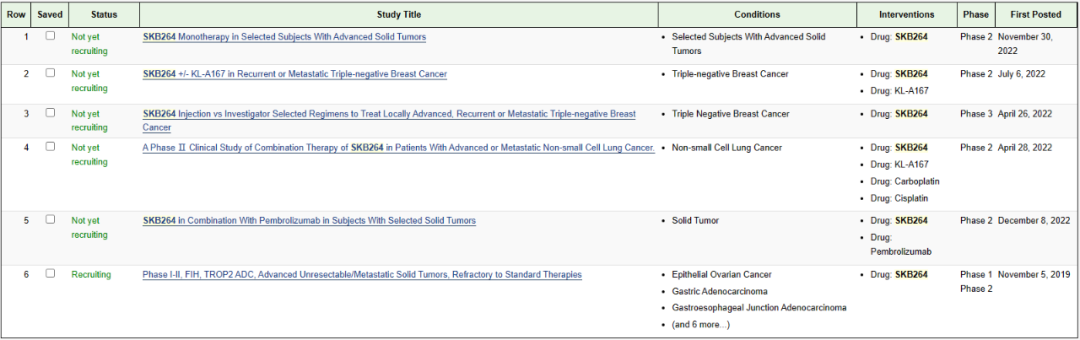
截图来源:科伦博泰招股书披露
03.靶向HER2的ADC药物:A166
A166是第三代靶向HER2的ADC药物(抗体药物偶联物),通过蛋白酶可裂解linker将新型毒素分子(Duo-5,微管蛋白抑制剂)定点偶联至HER2抗体(曲妥珠单抗)。
在2022年ASCO年会上,公布了由复旦大学附属肿瘤医院胡夕春教授和张剑教授团队主导的A166用于经过多线治疗的HER2+乳腺癌患者的Ⅰ期剂量扩展研究的更新数据,4.8mg/kg组客观缓解率(ORR)为73.9%,中位PFS为12.3个月,不良反应可控,A166疗效和安全性再次得到验证,未来可期。
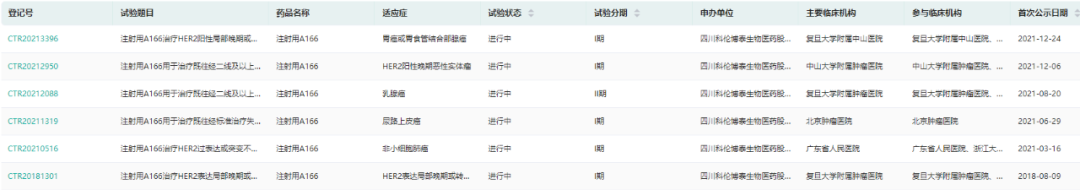
数据来源:药融云中国临床试验数据库
目前A166在中国和美国开展了多项临床试验,首发适应症HER2+乳腺癌已经进入临床II期。I期试验适应症包括NSCLC、结直肠癌和胃癌,正快速推进临床进展中。期待A166能尽快上市,造福患者。
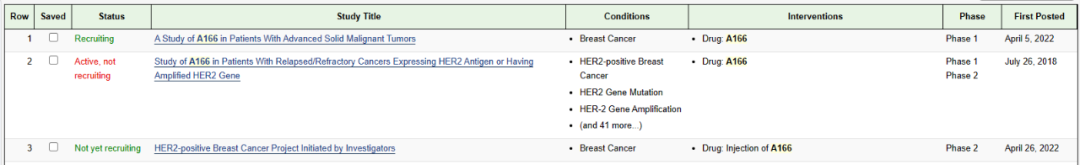
截图来源:科伦博泰招股书披露
04.JAK1/2抑制剂:KL130008
KL130008胶囊为靶向JAK1和JAK2激酶的选择性抑制剂。临床前研究显示,该产品可高效、选择性抑制JAK激酶活性,有望在发挥治疗作用的同时,兼具良好的安全性和耐受性。目前,KL130008正在开展治疗重度斑秃和活动性类风湿关节炎的II期临床试验。
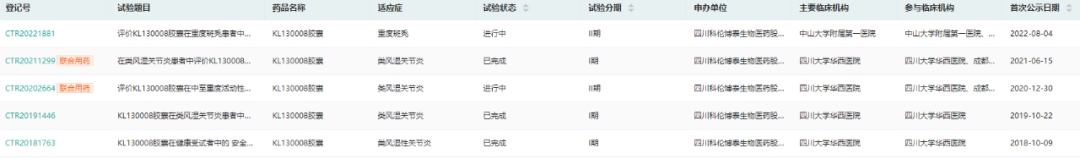
数据来源:药融云中国临床试验数据库
05.κ阿片受体(KOR)激动剂:KL280006
KL280006注射液为科伦药业研发的具有自主知识产权的选择性外周κ阿片受体激动剂,为阿片类镇痛药。实现有效镇痛的同时,能避免中枢镇痛类药物的不良反应,可用于急性疼痛(如术后疼痛)的治疗。
研究数据证实KL280006注射液作用机制明确,对外周κ受体具有高亲和性和高选择性,不易透过血脑屏障,镇痛效果确切,兼具良好的安全性和耐受性,无心脏、呼吸及中枢神经系统等不良反应。
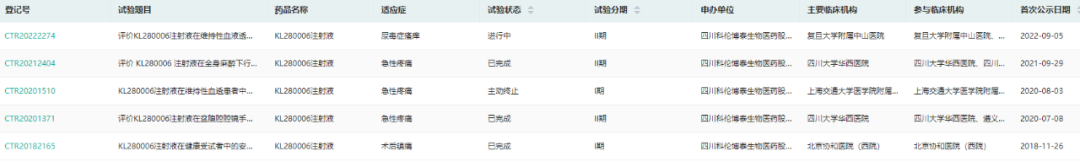
数据来源:药融云中国临床试验数据库
目前KL280006有关尿毒症瘙痒和急性疼痛两个适应症均开展了临床II试验,期待该药后续的进展。
06.靶向Claudin 18.2的ADC药物:SKB315
SKB315是靶向Claudin 18.2的第三代ADC药物,该新型抗体与Claudin 18.2具有高度亲和力,Claudin 18.2是一种在胃癌和胰腺癌细胞上特异表达的蛋白。SKB315配备了科伦博泰专利所有的linker和payload分子,采用第三代ADC技术,可裂解Linker,保留抗体ADCC和CDC效应,在临床前研究中显示出了良好的疗效和安全性。
2022年2月14日,SKB315开展了Ⅰ期临床试验,旨在评价注射用SKB315治疗Claudin18.2表达的晚期实体瘤患者的安全性、耐受性、药代动力学和初步疗效。该药与默沙东达成了重磅合作,国外的Ⅰ期临床试验预计即将展开,
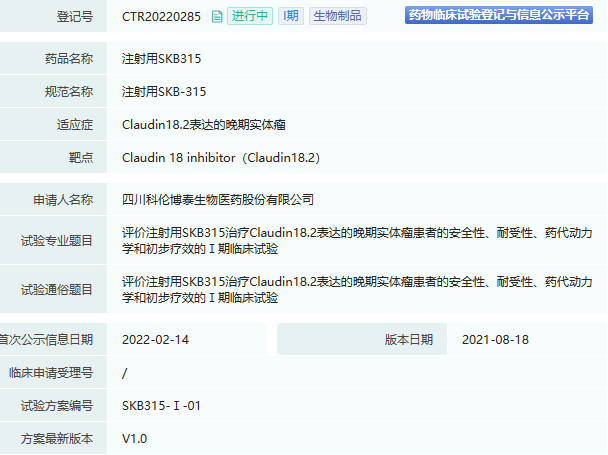
数据来源:药融云中国临床试验数据库
由于科伦博泰的研发实力十分强劲,管线众多,其余文中未涉及的新药大家可使用药融云小程序进行搜索。
二、结语
科伦博泰作为科伦药业的子公司,是集团布局创新药研发领域的一面旗帜,标志着科伦药业从仿制药往创新药转型的决心。管线的深度布局、与跨国大药企的深入合作,都彰显出科伦博泰不俗的潜力。作为国内ADC药物领头企业,期待科伦博泰能够在竞争中脱颖而出,走向国际化。
参考来源:
[1] 药融云数据库
[2] 科伦博泰招股书披露
想要解锁更多药企创新药研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品管线、研发现状、申报审批情况、临床试验信息、最新进展、市场规模与前景等,以及帮助企业抉择可否投入研发时提供数据参考!注册立享15天免费试用!

<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论