
靶点TIGIT素有“下一个PD-(L)1”之称,是近年来新兴的癌症免疫靶点,被视为继PD-(L)1之后最有潜力的免疫检查点之一。
7月初,复宏汉霖宣布其自主开发的HLX301(重组抗PD-L1与抗TIGIT双特异性抗体)的I/II期临床研究在国内已完成首例受试者给药,适应症为局部晚期/转移性实体瘤或淋巴瘤。
该临床试验(CTR20221234)旨在评估HLX301在局部晚期/转移性实体瘤或淋巴瘤患者中的安全性、耐受性、药代动力学及初步的抗肿瘤疗效。研究分为三个部分:Ia期剂量递增阶段、Ib期剂量扩展阶段、II期临床扩展阶段。
主要目的:
- Ia期:在没有或无法接受标准治疗的局部晚期/转移性实体瘤或淋巴瘤患者中确定HLX301的安全性、剂量限制性毒性(DLT)、最大耐受剂量(MTD)。
- Ib期: 在经过1线治疗且未使用过免疫检查点抑制剂(ICIs),且PD-L1 阳性(TPS≥50%)的局部晚期或转移性鳞状NSCLC患者中确定HLX301的推荐2期剂量(RP2D)。
- II期:评估HLX301在组织学或细胞学确诊为非小细胞肺癌、胃/食管胃交界处腺癌、头颈部鳞状细胞癌、广泛期小细胞肺癌、其他实体瘤或淋巴瘤患者中的抗肿瘤活性。
主要终点为研究者评估的客观缓解率(ORR)、疾病控制率(DCR)和缓解持续时间(DOR),次要目的为确认HLX301的安全性并评估PD-L1表达水平与HLX301抗肿瘤活性之间的关系。
CTR20221234临床试验信息(部分)
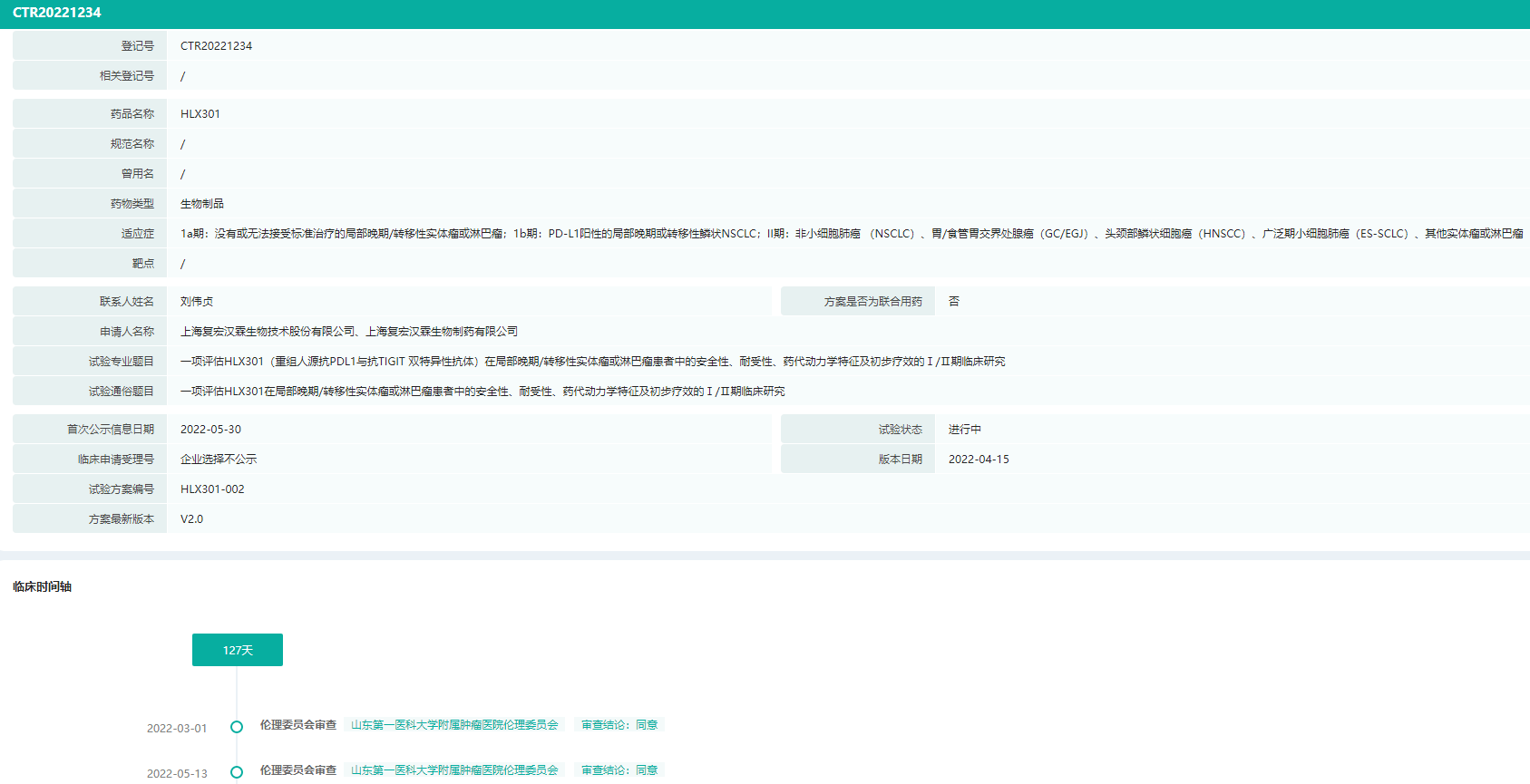
图片来源:药融云中国临床试验数据库
目前,全球范围内尚无同类靶向PD-1/L1和TIGIT的双特异性抗体获批上市,HLX301有望成为first-in-class抗PD-L1×TIGIT双抗。
1.TIGIT靶点机制
靶向PD-1及其配体PD-L1的药物在肿瘤免疫治疗中取得了突破性进展,但整体应答率不高,很多患者无法从中获益。因此寻找新的免疫检查点和生物标志物,扩大受益人群和更精准的筛选治疗适用人群是亟待解决的难题。
T细胞免疫球蛋白和 ITIM结构域蛋白(TIGIT)是一种共抑制性受体,于2009年被Yu等首次报道。研究发现TIGIT在多种恶性肿瘤中高表达,且与患者预后密切相关。靶向TIGIT单抗可有效地恢复T细胞功能,进而发挥抗肿瘤作用。因此,TIGIT及其配体CD155有望成为肿瘤免疫治疗的新靶点或预测预后的生物标志物。
TIGIT主要表达于各种免疫细胞,包括 CD8+CTL、CD4+滤泡辅助性T(Th)细胞、FOXP3+调节性T(Treg) 细胞和NK细胞。
研究发现,TIGIT与树突状细胞上的 CD155相互作用可增加IL-10的分泌,同时减少促炎细胞因子IL-12的分泌,从而抑制T细胞反应。CD155主要在树突状细胞、T细胞、B细胞和巨噬细胞表面表达,但在非造血组织如肾、神经系统和肠道中也有不同程度表达。CD155 作为一种免疫球蛋白样黏附分子,参与细胞运动、NK和T细胞介导的免疫。
TIGIT的功能
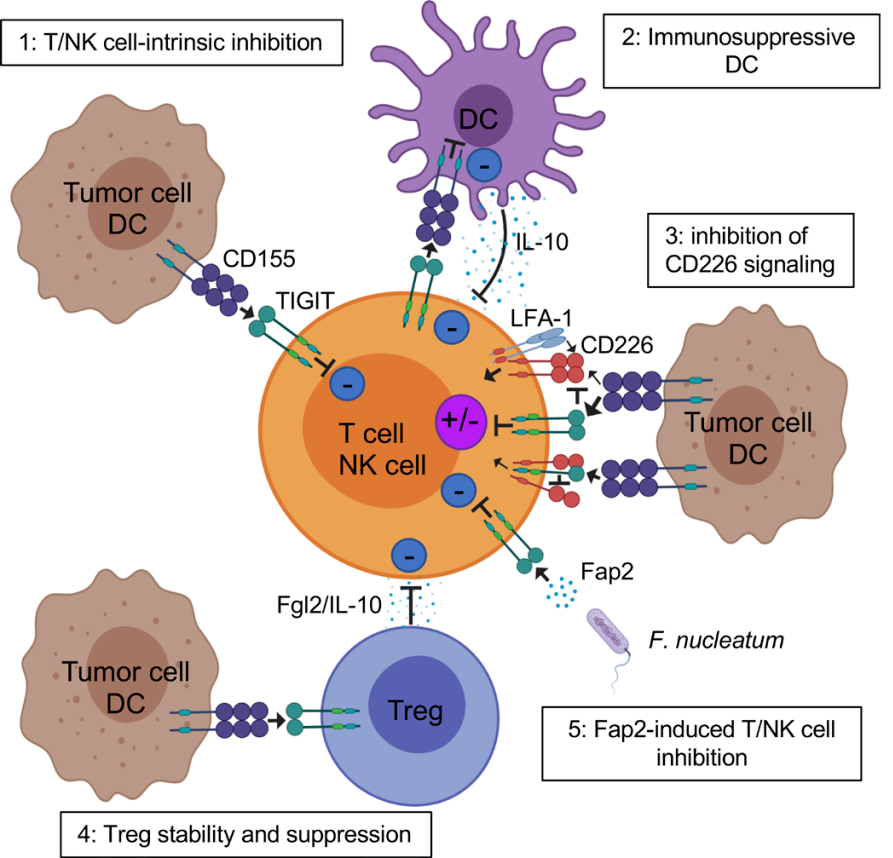
研究发现,CD155 通过上调Cyclin D2激活ERK信号,下调p27并缩短G0/G1期,在RAS突变癌细胞的增殖中起着积极作用。另一方面,CD155下调抑制肿瘤细胞增殖并诱导细胞周期停滞在G2/M期。除了在免疫细胞表达以外,与细胞程序性死亡受体1(PD-1)在黑色素瘤细胞表达类似,TIGIT在肿瘤细胞上也被发现存在表达,并且表达范围更加广泛。
在小鼠模型中,多发性骨髓瘤的进展与CD8+T细胞上TIGIT的高水平表达有关,TIGIT+ CD8+ T细胞在抗 CD3/CD28/CD2或骨髓瘤抗原刺激下表现为功能紊乱的表型,增殖减少、不能产生细胞因子。
临床研究中,许多恶性肿瘤,包括 NSCLC、黑色素瘤、头颈部鳞状细胞 癌(HNSCC)、结直肠癌(CRC)、胶质母细胞瘤(GBM)、胃癌、肝癌、MM、急性髓系白血病(AML)和滤泡性淋巴瘤(FL)的T细胞的TIGIT都高表达。
2.TIGIT研究现状
根据药融云数据统计,目前全球共有56个TIGIT相关项目正在推进中,其中临床一期12个,临床二期7个,临床三期5个,涉及40余家企业。
全球TIGIT靶点药物研发情况
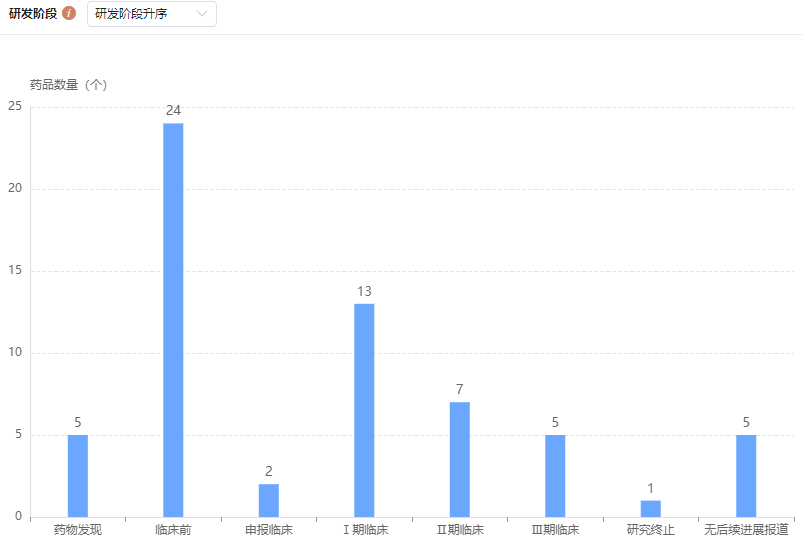
图片来源:药融云全球药物研发数据库
Tiragolumab(MTIG7192A)是 Genentech/Roche(罗氏)公司开发的结合TIGIT的全人源抗体。PD-L1/TIGIT双重阻断(atezolizumab/tiragolumab)与单独PD-L1阻断作为PD-L1阳性NSCLC患者的一线治疗相比,尽管毒性特征相似,但提供了更优的临床益处,改善了ORR和无进展存活率。这项研究包括135名NSCLC患者,其中atezolizumab联合tiragolumab的客观缓解率(ORR)为37%,而atezolizumab和安慰剂的ORR为21%。在PD-L1 +肿瘤(肿瘤比例评分>50%)中,atezolizumab联合tiragolumab的ORR为66%,而atezolizumab 和安慰剂的 ORR为24%。
目前,tiragolumab联合atezolizumab与安慰剂联合atezolizumab治疗未经治疗的局部晚期、不能切除或转移性 PD-L1选择的NSCLC患者的Ⅲ期,随机,双盲比较研究(NCT04294810)正在美国、澳大利亚、法国、中国等多个国家开展,预计将在2022年8月结束试验。
NCT04294810临床试验信息(部分)
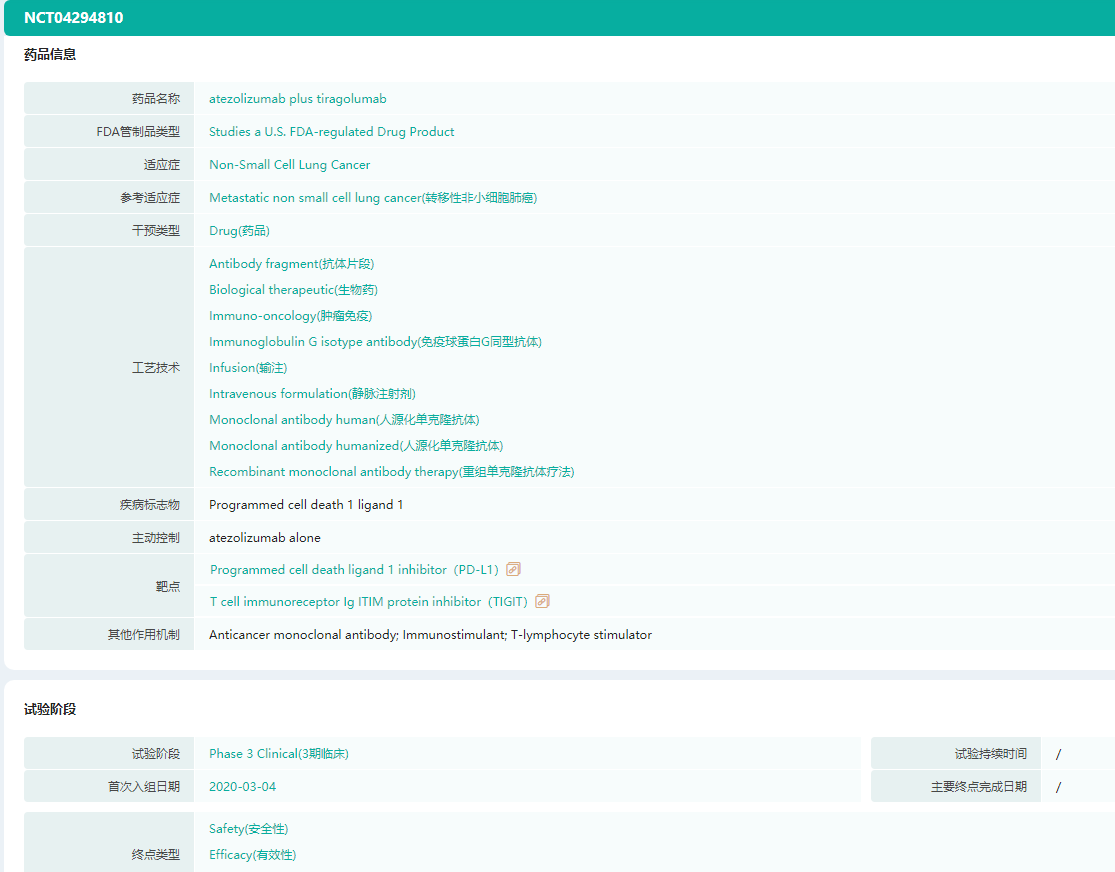
图片来源:药融云全球临床试验数据库
默沙东的vibostolimab、vibostolimab +pembrolizumab,百济神州的ociperlimab多项Ⅲ期临床试验也已在包括中国在内的全球多个国家开展。其他处于TIGIT抗体临床研究各阶段的还有吉利德、安斯泰来、百时美施贵宝、恒瑞医药、天境生物、泽璟生物等等。
从国内研发进展来看,目前国内共有包括君实生物、复宏汉霖生物、康方生物、信达生物、华博生物等在内的16家企业参与该靶点研发,涉及在研项目25个,在全球在研项目中占比达到45%,体现出国内企业较高的参与度。(通过药融云数据库可以看到国内布局TIGIT靶点研发企业详情)
国内TIGIT靶点研发企业TOP10
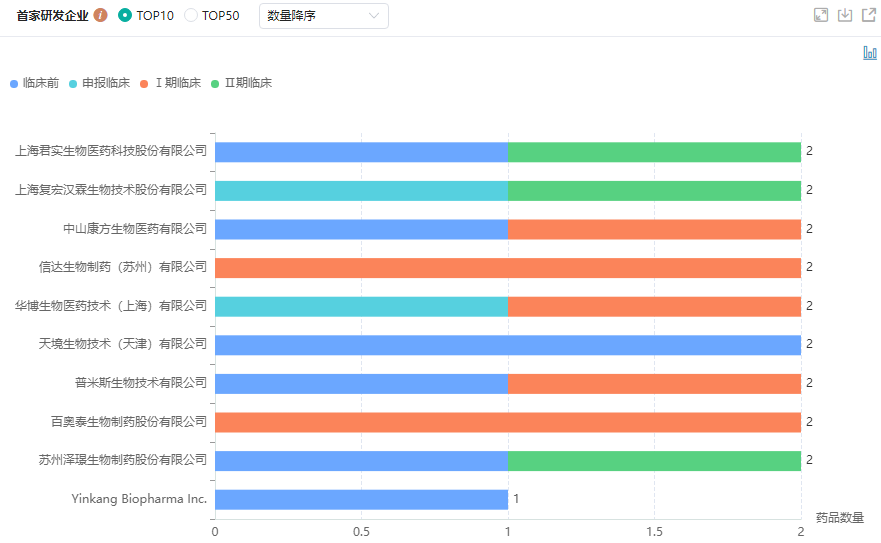
图片来源:药融云全球药物研发数据库
值得一提的是,先前TIGIT抗体单独用药的临床表现并不突出,而2020年tiragolumab与 PD-L1抗体联用的临床积极结果发布之后,TIGIT便成为了热门靶点,仅2021年就出现了几笔重磅交易,涉及阿斯利康、百时美施贵宝、葛兰素史克、吉利德等,各家的研发策略也都是和PD-(L)1抗体联合治疗。
在国产项目中,进展最快的是百济神州的Ociperlimab,目前正处于晚期非小细胞肺癌的III期试验中。2021年12月,百济神州宣布与诺华扩大合作,双方将在北美、欧洲和日本共同开发、生产和商业化百济神州在研TIGIT单抗ociperlimab,交易总额高达 27.95-28.95 亿美元,刷新了中国本土创新药单品种海外授权交易的最高纪录。
Ociperlimab非小细胞肺癌III期临床试验信息(部分)
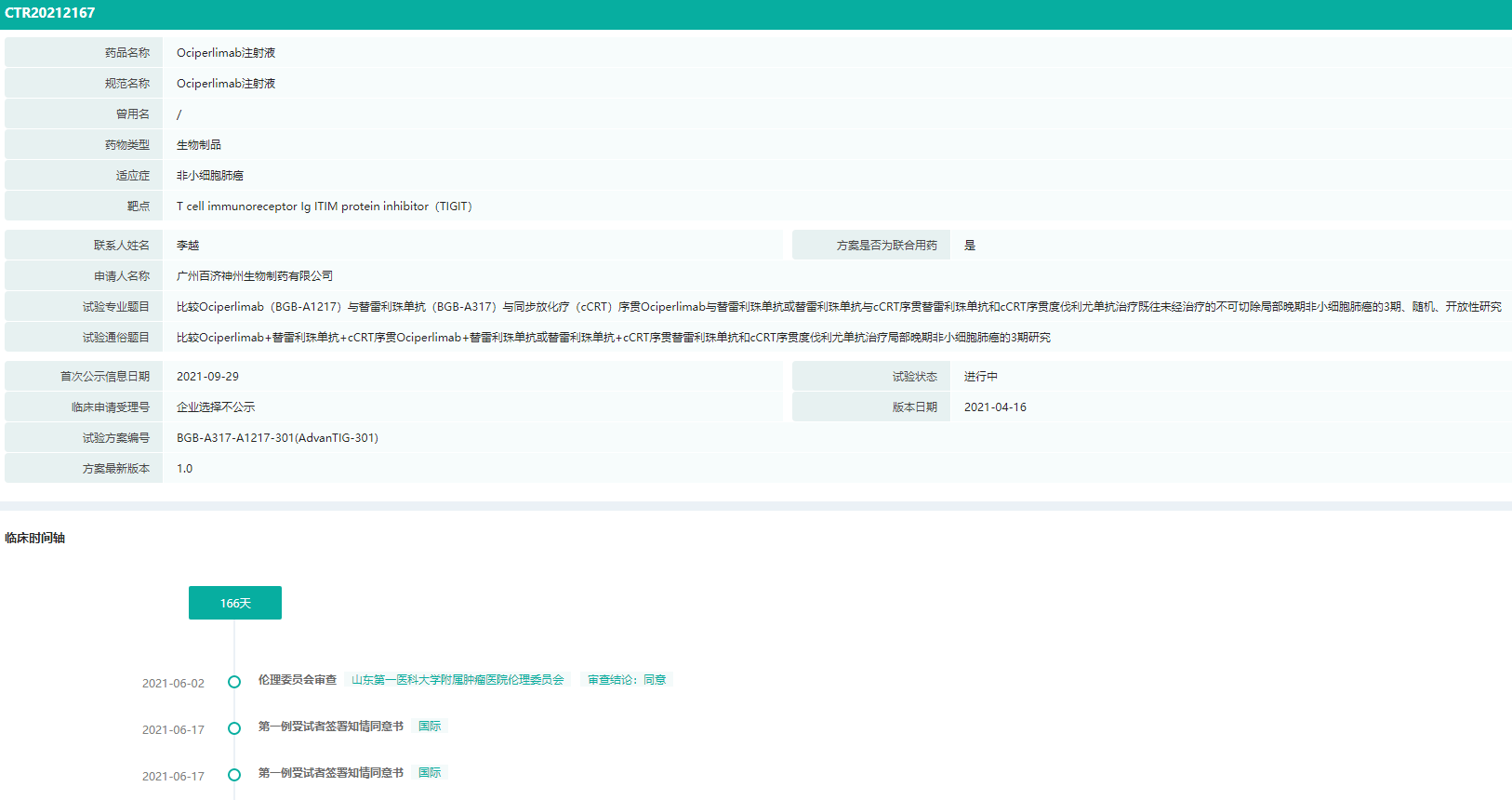
图片来源:药融云中国临床试验数据库
今年1月,君实生物宣布,Coherus已启动行使TIGIT单抗JS006在美国和加拿大的许可选择权的程序。同时,Coherus 将向君实生物支付3500万美元首付款,最高达2.55亿美元的开发、申报和销售里程碑付款,以及产品销售净额18%的销售分成。
TIGIT作为一种新的免疫治疗靶点,在机体免疫调节中具有重要作用,对T细胞和NK细胞的抗肿瘤功能都具有十分重要的调控作用。
但业界对该靶点未来前景也存在一定争议,今年以来,作为TIGIT单抗领域领头羊的罗氏研发屡屡受挫,从3月份针对广泛小细胞肺癌患者一线治疗临床三期失败,再到5月份的针对高PD-1表达人群的非小细胞肺癌患者一线治疗失败。
不过,人类探索治愈肿瘤癌症的步伐从未停止。TIGIT抗体作为目前被寄予厚望的靶点之一,未来是会步IDO抑制剂后尘还是成为下一个PD1?国内外哪家企业能率先拿下TIGIT抗体?让我们拭目以待。
药物的研发是一件极其复杂、费时费力的事情,实时掌握医药行业内发生的大小事,对药物的研发有很大的帮助。药融云咨询团队联合药学数据分析团队每月将会推出《全球在研新药与靶点月报》,内含一月内医药行业核心数据回顾。
本文选题于《药融云6月全球在研新药与靶点月报》,想要获取报告完整内容,关注“药融云”公众号(gh_d20f87bd52d9),回复关键词“报告”即可领取。
想要解锁更多靶点药物研发情况吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握靶点研发药物布局、基本信息、研发阶段、竞争格局、最新进展、申报获批情况、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论