前言:计量器具在药品的生产过程中,有比较广泛的应用。本文仅就计量器具如何分类及其校准周期的确定粗略地谈些自己的看法。
1、 目的
建立计量器具分类管理、校准周期管理体系。
2、 范围
适用于公司计量器具的分类及周期管理。
3、 参考文件
3.1 《药品生产质量管理规范》(卫生部令第79号,2010版)
4、 职责
4.1 计量人员:负责起草及修订本文件。
4.2 质量保证部、质量控制部和生产部负责本规程的审核。
4.3 质量负责人负责本规程的批准。
5、 程序
5.1 计量器具的分类方法
5.1.1 结合“中华人民共和国计量法”及“计量法实施细则”对计量器具进行分类;
5.1.2 依据计量器具的质量、性能及本公司的实际情况,按照使用地点、使用要求和频繁程度,对其进行风险评估,依据风险评估的结果对计量器具进行分类。
5.2 计量器具风险评估方法
5.2.1 风险级数(R): R= x*y*z
其中,x:对工艺管理的影响;y:对物料产品检测的影响;z:对安全方面的影响。
5.2.2 x、y、z的风险评估评分标准见表1:x、y、z 的风险评估评分标准。
表1:x、y、z 的风险评估评分标准
5.2.3 计量器具依据风险级数(R)的值的分类标准见表2:风险级数(R)的值的分类标准。
表2:风险级数(R)的值的分类标准
5.3 计量器具的分类
5.3.1 A类计量器具
5.3.1.1 用于贸易结算、安全防护、医疗卫生和环境监测方面,并列入强制检定计量器具目录,按国家相关规定送指定计量部门进行周期性检定。
5.3.1.2 计量器具风险评估为A类的计量器具。
5.3.2 B类计量器具:计量器具风险评估为B类的计量器具。B类计量器具包括但不限于:
5.3.2.1 用于工艺控制、质量检测中计量数据有准确度要求的计量器具;
5.3.2.2 用于日常监测除关键控制参数以外的工艺参数的器具;
5.3.2.3 固定安装在连续运转装置或生产线上、计量数据准确度要求较高但平时不允许拆装的计量器具。
5.3.2.4 其他不属于A类管理的检验仪器。
5.3.3 C类计量器具:计量器具风险评估为C类的计量器具。C类计量器具包括但不限于:
5.3.3.1 在生产、质量管理过程中,在生产线和装置上固定安装的、不易拆卸而又无严格准确度要求,仅起指示性作用的仪器仪表。
5.3.3.2 性能很稳定、可靠性高而使用又不频繁的,且量值不易改变的计量器具。
5.3.3.3 对计量数据无严格准确度要求的、性能不易变化的低值易耗品。
5.3.3.4 国家计量行政部门明令允许一次性使用或实行效期管理的计量器具。
5.3.4 D类计量器具:计量器具风险评估为D类的计量器具。
5.4 计量器具的管理
5.4.1 A类计量器具
5.4.1.1强制检定的计量器具必须按规定登记造册,报当地人民政府计量行政部门备案,向其指定的检定机构申请周期检定,按照周期送检并保存计量部门出具的检定证书。
5.4.1.2 非强制检定的计量器具,按评估确定的校准周期进行自校或外校。对没有能力自行校准的A类计量器具应送到有资格的单位(计量检定部门或生产厂家)进行校准;对于有能力自行校准的计量器具,必须严格按校准操作规程中规定的校准环境及步骤进行校准,校准完毕后填写校准记录。
5.4.2 B类计量器具
B类计量器具按照评估确定的校准周期进行校准。对没有能力自行校准的B类计量器具应送到有资格的单位(计量检定部门或生产厂家)进行校准;对于有能力自行校准的计量器具,必须严格按校准操作规程中规定的校准环境及步骤进行校准,校准完毕后填写校准记录。5.4.3 C类计量器具:C类计量器具可适当减少校准项目,延长校准周期或作一次性校准处理。
5.4.3.1 对准确度无严格要求、性能不易变化而又是低值易耗的计量器具实行一次性校准;
5.4.3.2对非生产关键部位指示用计量器具和在连续运转设备上固定的表盘计量器具,可进行有效期管理或延长校准周期,校准周期的延长通过评估确定,但一般控制在2~4个周期内。
5.4.4 D类计量器具:不需要校准。
5.5 计量器具校准周期确定
5.5.1 通过矩阵图对计量器具的校准周期进行风险评估,初步确定计量器具的校准周期。
5.5.2 风险评估时,考虑以下因素:对产品/工艺的重要性;装置对外界环境影响敏感性。
5.5.3 计量器具校准周期风险评估结果见图1:风险评估 。
图1:风险评估
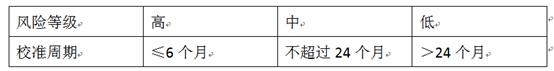
5.5.4 计量器具的风险评估结果和校准周期的的关系见表3:计量器具校准周期确定和风险等级对应表。
表3:计量器具校准周期确定和风险等级对应表
5.6 计量器具的校准周期确定后,在后续计量器具的使用过程中,在校准周期的中间时间点,依据计量器具的实际使用需求、设备的使用情况和性能表现、历次校准结果的趋势等对已制订校准周期进行复评,必要时对计量器具的校准周期做出调整。
5.6.1 计量器具校准周期的复评方法:Q=a*b*c
其中,a:测量 项目的质量控制情况及有效性;
b: 历次校准结果的趋势;
c:使用的环境条件。
a、b、c的评分标准分别见表4、表5、表6。
表4:测量项目的质量控制情况及有效性的评分标准
表5:历次校准结果的趋势的评分标准
表6:使用的环境条件的评分标准
5.6.2 计量器具的校准周期复评判断
对计量器具的校准周期进行复评时,其复评结果有三种情况:缩短校准周期、校准周期不变、可适当延长校准周期。复评结果的判断见表7:计量器具的校准周期复评判断标准。
<END>



















收藏
登录后参与评论