脂质体纳米粒在临床应用方面取得了极大的成功。无论是小分子药物领域已经上市了二十余款制剂,还是近期的RNA疫苗研制中发挥的关键作用,都显示出脂质体在药物应用领域的巨大潜力。该篇综述聚焦于脂质体纳米粒在临床中的应用。本文为第四部分,概述了脂质体纳米粒在基因治疗方面的应用。
本文译自Thai Thanh Hoang Thi 和 Nghia P. Truong等人的综述 Lipid-BasedNanoparticles in the Clinic and Clinical Trials: From Cancer Nanomedicine toCOVID-19 Vaccines,Vaccines 2021, 9, 359(4.Lipid-Based Nanoparticles for Gene Therapy)
4. 用于基因治疗的脂质纳米粒
最近,核酸疗法(如小干扰RNA(siRNA)、小激活RNA(saRNA)和信使RNA(mRNA)),得到了极大的关注。其在多种疾病的治疗和药物传递的应用潜力已经成为了药物研究的前沿。然而,这些基因药物容易被血清核酸内切酶快速降解。为了保护核苷酸,越来越多的脂质体或脂质纳米粒(LNPs,包括SLN和或NLCs)被用作药物传递系统,展现出足够的包载能力和组织细胞靶向能力。已经设计了一系列可电离脂质用于基因传递,每种脂质都具有各自的pKa和结构特性,例如1,2-二油基-3-二甲氨基丙烷(DODAP,pKa为6.6)、1,2-二硫基-3-二甲氨基丙烷、1,2-二硫基氧基-3-二甲氨基丙烷(DLinDMA,pKa为6.8)、2-二硫基-4-二甲氨基甲基-[1,3]-二氧戊环(DLin-K-DMA,pKa为5.94),2,2-二硫酰基-4-(2-二甲氨基乙基)-[1,3]-二氧戊环(DLin-KC2-DMA,pKa为6.68)(图5),和(6Z,9Z,28Z,31Z)-七烯-6,9,28,31-四烯-19-基-4-(二甲氨基)-丁酸(DLin-MC3-DMA,pKa为6.44)。除了pKa值之外,头基和烷基链之间的连接子也是传递效率的决定因素。与酯和烷氧基连接子相比,缩酮连接子被证明是最佳选择。Dlin-K-DMA与其他不含缩酮连接子的脂质相比,可以在体内实现VII因子的显著沉默。通过一系列连接子优化,获得了DLin-MC3-DMA,其被认为是一种很有希望的基因药物递送候选化合物,能够实现临床应用。Dlin-MC3-DMA在体内肝基因沉默的效力是Dlin-KC2-DMA的10倍。图1对这种以Onpattro商品名上市的脂质体进行了说明。第二个获得FDA批准的siRNA治疗药物是2019年11月的GIVLAARITM(givosiran,ALN-AS1),它也获得了欧盟的批准——这是一种靶向肝细胞中ALAS1基因的合成siRNA。该疗法适用于患有急性肝卟啉症的成年患者。急性肝卟啉症是一种遗传性疾病,在血红素产生过程中,毒卟啉分子积聚。然而,这种RNA疗法是由裸核苷酸修饰的siRNA组成的,没有载体,包含了一种直接靶向肝脏的配体。
Arcturus Therapeutics,Inc.(SanDiego, CA, USA)开发了一个用于RNA递送的脂质体平台,简称为LUNAR。其组成包括特定的可电离氨基脂质(58%mol/mol,ATX,图4)、磷脂1,2-二硬脂酰-sn-甘油-3-磷酸胆碱(7%mol/mol,DSPC)、胆固醇(33.5%mol/mol)和DMG-PEG2000(1.5%mol/mol)。ATX脂质类似于AlnylamAcuitas开发的脂质家族,可针对各种适应症的特定细胞类型或组织进行修饰。与传统阳离子脂质不同,ATX脂质在生理条件下通过酯键的断裂进行降解,从而促进脂质体的快速降解,从而加快代谢和提高安全性。非临床试验中,LUNAR被用于包载人类FIX(hFIX)的mRNA,用于治疗血友病B。LUNAR递送mRNA的效率是其他脂质载体,DLin-MC3-DMA或七烯虫胺-6,9,28,31-四烯-19-基-4-(二甲氨基)丁酸(MC3)的5倍。此外,LUNAR处方并未引发不利的免疫反应,如肝酶增加(肝酶是急性肝毒性的标志物)。
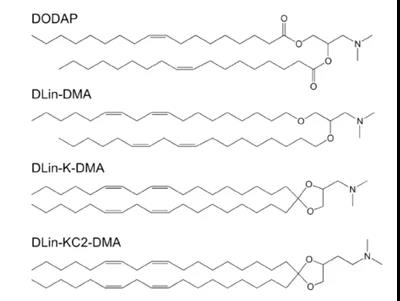
图5. 最常用的可离子化的阳离子脂质体的化学结构
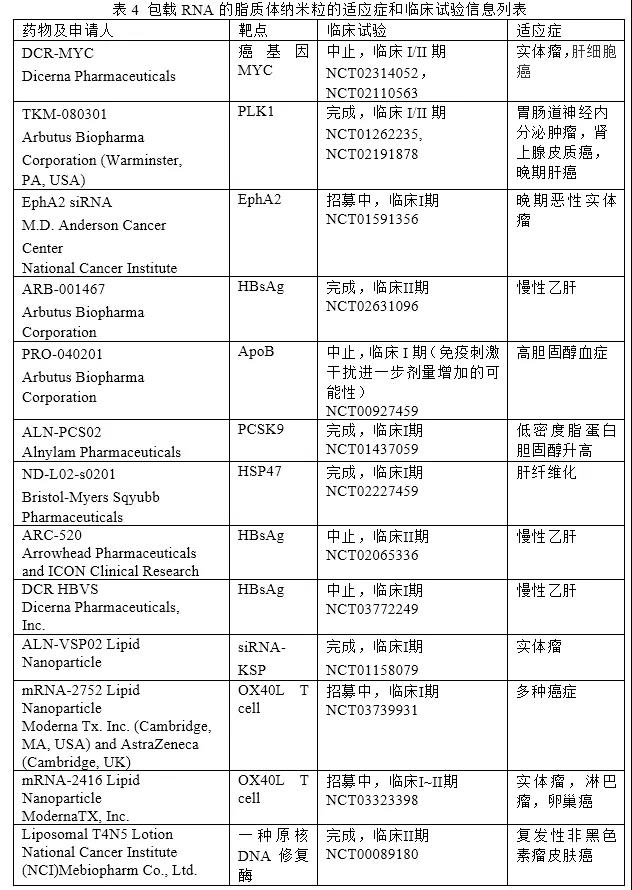
目前,除了第一个商业RNA产品Onpattro,GIVLAARITM和正处于临床前研究mRNA-LUNAR之外,许多其他RNA脂质体(RNA-LNP)已经进入了临床试验(表4)。TKM-080301由ArbutusBiopharma公司研制,用于治疗实体肿瘤,如胃肠道神经内分泌肿瘤或肾上腺皮质癌(ACC)。TKM-080301是一种可以靶向PLK1(polo-likekinase 1)的包载siRNA的脂质体,PLK1是调节肿瘤增殖的关键靶点。该候选药物进行了一项I/II期临床研究(NCT01262235),获得了有希望的安全性数据和抗肿瘤疗效数据。在以0.6或0.75mg/kg/周的剂量对16名患者进行18个周期治疗的试验后,证实TKM-080301可增加PLK1的表达并使ACC中的靶点失活。随后,在2018年,TKM-080301在晚期肝细胞癌患者中进行了安全性、药代动力学和初步抗肿瘤活性的临床评估(NCT02191878)。在这项针对43名患者的早期研究中,TKM-080301的抗肿瘤作用有限。因此,TKM-080301没有继续作为治疗肝癌的单一药物进行进一步评估,临床研究已经终止。
Dicerna Pharmaceuticals(Lexington,Massachusetts MA, USA),一家专门研究沉默基因的RNA药物的公司,已经开发出DCR-MYC,这是一种包载合成双链RNA并可以靶向MYC癌基因的脂质体颗粒,可以用于肿瘤抑制。该疗法已在多发性骨髓瘤、淋巴瘤或实体瘤患者的剂量递增研究(NCT02110563)中进行了评估。此外,DCR-MYC也在肝细胞癌的临床试验中进行了评估(NCT02314052)。然而,所有与DCR-MYC相关的临床研究均已被Dicerna终止,因为早期疗效结果未达到该公司的预期。
在将基因疗法应用于癌症方面,Wagner等人开发了一种纳米脂质体EphA2靶向疗法(EphA2siRNA),该脂质体表面为中性电荷,旨在降低与带电粒子相关的器官毒性。EphA2属于酪氨酸激酶受体的一个亚家族,在乳腺癌、肺癌、前列腺癌、卵巢癌、胰腺癌和子宫内膜癌中过度表达。因此,包载的siRNA可以干扰癌细胞增殖并减缓肿瘤生长。在临床前研究中,该制剂显示出显著的抗癌作用,对溶血反应、炎症和胃肠道、心脏和肾脏的单核细胞浸润反应轻微。这些有希望的结果使EphA2siRNA进入了I期临床试验(NCT01591356),用于晚期或复发性实体瘤患者。
ModernaTX公司和阿斯利康已开发出包载mRNA-2752的LNP,并已申请I期临床试验(NCT03739931)。该mRNA编码OX40L,这是一种T细胞共刺激因子,IL-23和IL-36γ促炎细胞因子。实体瘤患者单独使用mRNA-2752或与德瓦鲁单抗联合治疗。在晚期实体恶性肿瘤或淋巴瘤的临床前研究中,观察到单药或联用德瓦鲁单抗双药治疗,可以实现肿瘤缩小,这支持mRNA-2752进入临床I期。使用类似的技术,ModernaTX公司研究了另一种LNP候选药物(mRNA2416),用于治疗晚期恶性肿瘤。mRNA-2416被直接递送至过度表达OX40的肿瘤,然后强力激活T细胞响应,杀死肿瘤。目前,该候选药物已经开始了I~II临床试验的招募(NCT03323398)。
2012年,AlnylamPharmaceuticals还完成了ALN-VSP02的I期临床试验(NCT01158079),该药物是一种含有siRNA的LNP,靶向血管内皮生长因子(VEGF)和驱动蛋白梭形蛋白(KSP)。这些因子在许多肿瘤中过度表达,有助于肿瘤的增殖和生存。因此,ALN-VSP02使这两种mRNA沉默,并阻止KSP和VEGF蛋白的翻译,从而抑制这些患者的肿瘤生长。
LNP-RNA系统已被证明是一个多功能平台,其用途超出了癌症治疗。从2009年到2019年,有6种类似产品批准用于临床试验(表4)。Arbutus生物制药公司完成了ARB-001467的II期临床试验(NCT02631096)。该制剂中含有针对四种乙型肝炎病毒转录的siRNA,适用于乙型肝炎患者。Bristol-MyersSquibb(百时美施贵宝)和NittoDenko公司完成了ND-L02-s0201的Ib/II期临床试验,该候选药物的适应症是中度至广泛性肝纤维化患者(NCT02227459)。ND-L02-s0201是一种热休克蛋白47的siRNA,可调节胶原蛋白的合成和分泌,防止纤维化。这项临床研究在欧洲和美国启动后,也已在日本开始。ArrowheadResearch还开发了ARC-520治疗乙型肝炎病毒,并申请了II期临床试验(NCT02065336)。ARC-520由干扰RNA制备而成,干扰RNA可减少来自共价闭合环状DNA的所有RNA转录物,从而减少病毒抗原和乙型肝炎病毒DNA。然而,ARC-520因与药物递送相关的毒性而终止。目前,DicernaPharmaceuticals公司已开发出带有siRNA(命名为DCR-HBVS)的LNP,靶向乙型肝炎表面抗原(HbsAg)的mRNA,用于治疗慢性乙型肝炎。使用DCR-HBVS治疗的小鼠乙型肝炎模型显著减少,基于该临床结果,DCR-HBVS进入了I期临床试验(NCT03772249)。
Alnylam Pharmaceuticals还完成了ALN-PCS02治疗高胆固醇血症患者的I期临床试验(NCT01437059)。ALN-PCS02由脂质LNPs中包裹的siRNA制备而成,其中siRNA降低血浆胆固醇代谢的前蛋白转化酶枯草杆菌蛋白酶kexin9型(PCSK9)酶,导致低密度脂蛋白水平降低。
2009年,Tekmira注册了一项编号为NCT00927459的PRO-040201的I期临床试验,该试验的候选药物是一种包载siRNA的稳定的核酸LNP。PRO-040201可以靶向肝细胞产生的ApoB,以控制血液中的胆固醇水平。尽管初步临床试验表明PRO-040201能有效地将siRNA传递到肝脏并显著降低低密度脂蛋白,但在最高剂量时仍存在流感样症状。因此,Tekmira决定在2010年终止该研究。
临床应用和临床试验中的脂质体纳米粒(三):药物递送
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论