导读:
4月12日-4月18日,CDE新公示临床试验共计101项
从药品类型来看,化学药物共计74项,生物制品25项,中药/天然药物2项
从临床分期来看,临床I期27项,临床II期8项,临床III期14项,临床IV期4项
从实验状态来看,96项试验在进行中,5项试验已完成
BE试验45项,涉及糖尿病、感染等多个适应症,扬子江开展最多
国内外新药试验51项,涉及默沙东、葛兰素史克、恒瑞等企业
4月12日-4月18日CDE新公示临床试验概览
2021年4月12日-4月18日,CDE新公示临床试验共计101项。从药品类型来看,化学药物共计74项,生物制品25项,中药/天然药物2项。
4月12日-4月18日新公示临床试验药品分类
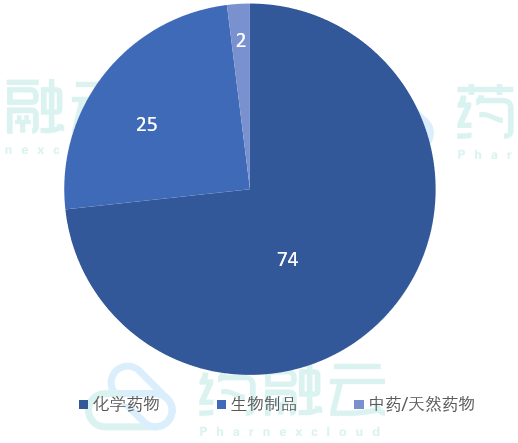
数据来源:药融云中国临床试验数据库
从临床分期来看,临床I期(含1b/II 期、I期/II期、I和IIa期)27项,临床II期(含II/III期)8项,临床III期14项,临床IV期4项,其他试验48项(主要是BE试验)。
4月12日-4月18日新公示临床试验分期
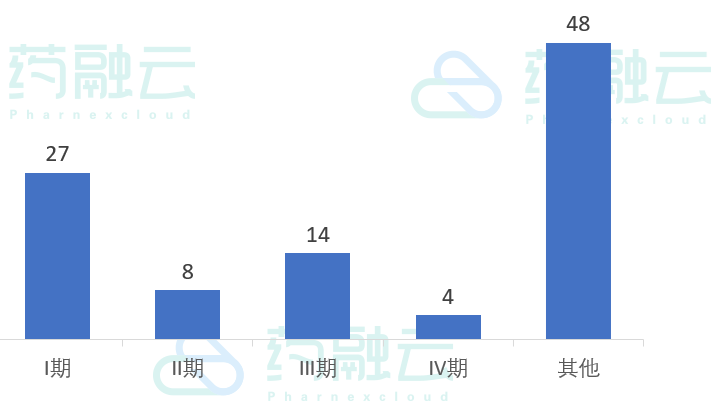
数据来源:药融云中国临床试验数据库
从实验状态来看,96项试验在进行中,其中87项尚未开始招募,8项正在招募中,1项已完成招募。5项试验已完成,其中3项是扬子江磷酸奥司他韦胶囊和雷诺嗪缓释片的BE试验,另两项分别是南京优科的巴瑞替尼和寿光富康制药的盐酸二甲双胍缓释片的BE试验
。
4月12日-4月18日新公示临床试验状态
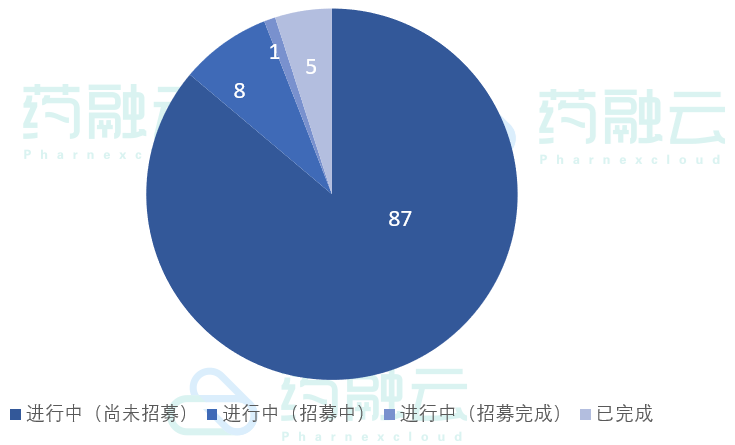
数据来源:药融云中国临床试验数据库
4月12日-4月18日公示BE试验45项,
扬子江开展最多
4月12日-4月18日公示BE试验45项,涉及糖尿病、感染等多个适应症。从试验药品来看,磷酸西格列汀片、磷酸奥司他韦胶囊开展3项BE试验,并列第一,其次是阿奇霉素干混悬剂、马来酸阿伐曲泊帕片和依托考昔片,均开展2项。从申办药企来看,扬子江开展BE试验最多,共公示3项BE试验。
4月12日-4月18日新公示BE试验汇总
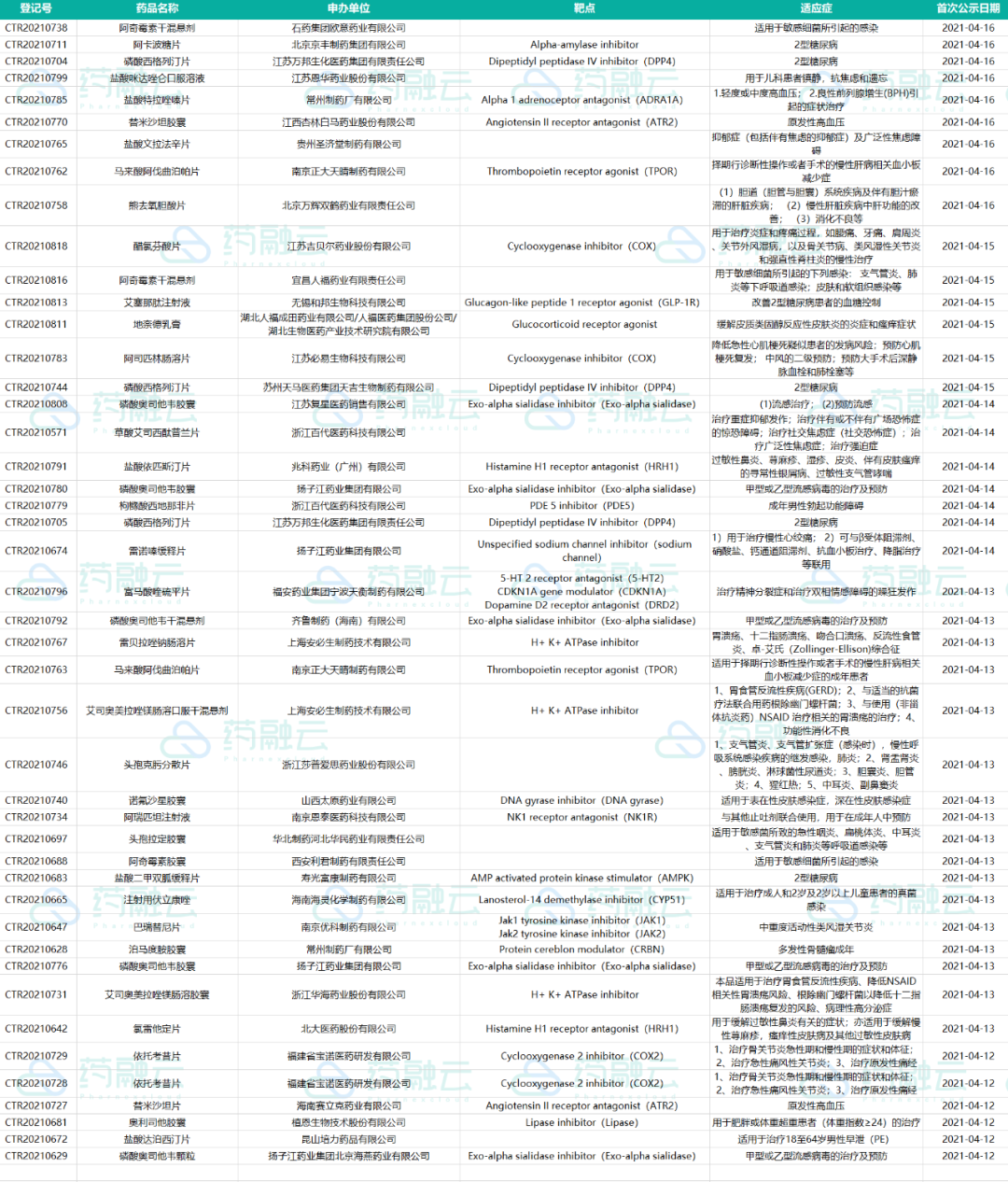
数据来源:药融云中国临床试验数据库
国内外新药试验51项,
涉及默沙东、葛兰素史克、恒瑞等企业
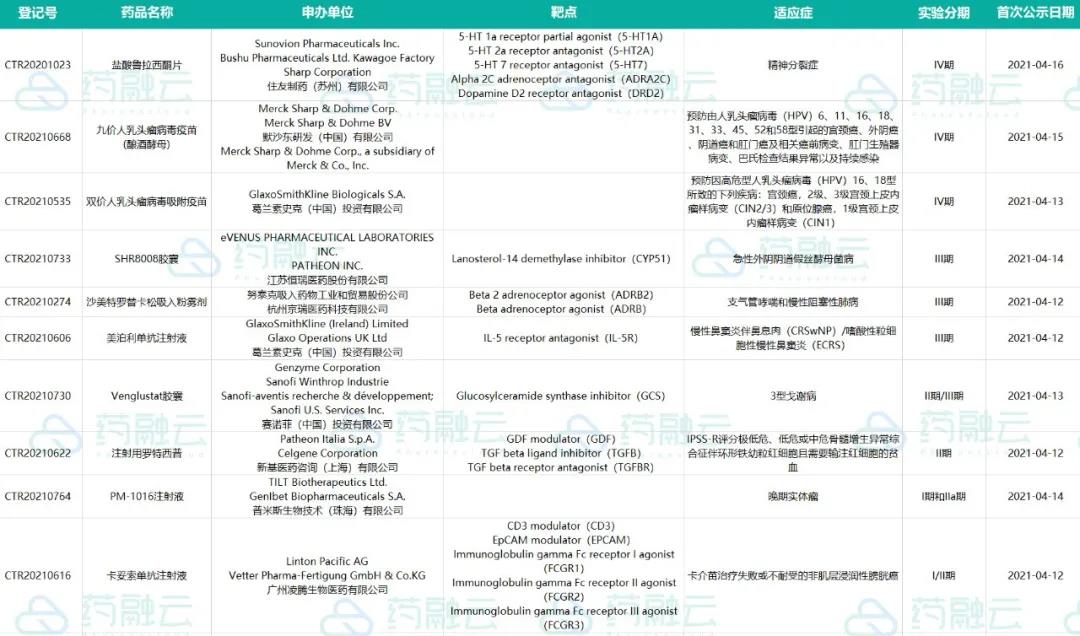
新公示进口药试验10项,过半试验处于临床后期,涉及默沙东、葛兰素史克等企业。国内新药试验共41项,超三分之一为肿瘤药物试验;信达及东阳光分别新公示2项试验,均处于临床早期。
4月12日-4月18日新公示进口药试验汇总
数据来源:药融云中国临床试验数据库
4月12日-4月18日新公示国内新药试验汇总

数据来源:药融云中国临床试验数据库
6款重点新药介绍,
涉及葛兰素史克、恒瑞、百济神州等企业
美泊利单抗注射液
申报企业:葛兰素史克
美泊珠单抗注射剂是人源化的IL-5单克隆抗体,可以选择性识别并结合IL-5,并阻止IL-5与嗜酸性粒细胞表面受体的结合,从而减轻严重的嗜酸性粒细胞哮喘,并降低嗜酸性粒细胞的水平。该药物已被批准在20多个国家/地区销售。2020年7月6日,葛兰素史克在中国提交的美泊利单抗注射液上市申请获得CDE受理,这是国内首个申报上市的IL-5单抗。
SHR-1314注射液
申报企业:恒瑞
SHR-1314是恒瑞医药自主开发的人源化单克隆抗体药物,以IL-17A为靶点,能特异结合 IL-17A从而抑制GROα等细胞因子的产生,达到阻断信号传导通路的作用,主要用于银屑病的治疗,其它拟开发适应症还包括克罗恩病、多发性硬化症、哮喘和红斑狼疮、类风湿性关节炎等。截至目前,全球仅上市2个IL-17单抗药物,分别是诺华的Cosentyx(secukinumab)和礼来的Taltz(ixekizumab)。
SHR-6390片
申报企业:恒瑞
SHR6390是江苏恒瑞医药股份有限公司研发的口服、高效、选择性的小分子CDK4/6抑制剂,属于化药1类新药。此前,SHR6390片联合氟维司群治疗HR阳性、HER2阴性的经内分泌治疗后疾病进展的局部晚期或晚期乳腺癌的多中心、随机、对照、双盲的III期临床研究达到方案预设的优效标准。研究结果表明,对于既往使用过内分泌治疗的HR阳性、HER2阴性晚期乳腺癌患者,接受SHR6390联合氟维司群对比安慰剂联合氟维司群,可显著延长患者的无进展生存期。近日, SHR6390片被国家药品监督管理局药品审评中心纳入拟突破性治疗品种公示名单,拟定适应症为SHR6390片联合氟维司群治疗经内分泌治疗后进展的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的复发或转移性乳腺癌。
泽布替尼胶囊
申报企业:百济神州
泽布替尼是布鲁顿氏酪氨酸激酶(BTK)选择性抑制剂。泽布替尼胶囊是我国自主研发并拥有自主知识产权的创新药。于2020年6月获批上市,用于治疗既往至少接受过一种治疗的成人套细胞淋巴瘤(MCL)患者和既往至少接受过一种治疗的成人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者,是首个国产BTK 抑制剂。此次公布的是治疗CD79B基因突变型复发或难治性弥漫大B细胞淋巴瘤的II期试验。
AK-112注射液
申报企业:康方生物
AK112是康方生物自主研发,全球行业内首个进入临床研究的PD-1/VEGF双特异性抗体。AK112是基于康方生物独特的TETRABODY技术设计,可阻断PD-1与PD-L1和PD-L2的结合,并同时阻断VEGF与VEGF受体的结合。PD-1抗体与VEGF阻断剂的联合疗法已在多种瘤种(如肾细胞癌、非小细胞肺癌和肝细胞癌)中显示出强大的疗效。鉴于VEGF和PD-1在肿瘤微环境中的共表达,与联合疗法相比,AK112作为单一药物同时阻断这两个靶点,可能会更有效地阻断这两个通路从而增强抗肿瘤活性。
HEC-53856胶囊
申报企业:东阳光药业
HEC53856胶囊是由广东东阳光药业有限公司研发的1 类新药,拟用于治疗慢性肾脏病相关的贫血,包括透析和非透析病人,为HIF-PH(低氧诱导因子脯氨酰羟化酶)抑制剂。HIF-PH(抑制剂能够在氧分压正常的情况下抑制 HIF-脯氨酰羟化酶,稳定 HIF-α,促内源性 EPO 生成及改善铁吸收利用,综合调控促进红细胞生成。






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论