
在创新药研发的漫长周期中,业界往往将目光聚焦于靶点机制、临床疗效或是资本运作。然而,在将潜在候选药物从先导化合物优化阶段推向临床开发的过程中,有一个极具破坏力却常被早期研发团队忽视的隐形变量——短期产品成本(CoG)。
短期成本主要指生产一批预期目标化合物所耗费的资源,涵盖原材料、单元操作及生产相关费用。在药物发现的极早期阶段,“唯快不破”确实是核心法则,时间周期重于一切。但是,若对产品成本缺乏前瞻性规划,这一因素将在临床前和临床开发阶段演变为巨大的财务黑洞,甚至直接干预商业化进程。
本文将聚焦于小分子新化学实体(NCE),深度拆解原料药(API)在早期研发阶段的成本控制逻辑。需要说明的是,本探讨不涉及仿制药、生物仿制药、疫苗及单克隆抗体等领域。理解并驾驭API成本,是我们打通从实验室到临床供应链生命线的关键。
一、演进逻辑:合成路线在不同研发阶段的终极使命
小分子NCE在早期上游开发阶段的损耗率远高于后期,因此,财务管理的明智之举应当是将其作为核心要素贯穿研究的始终。在生物制药的不同阶段,API合成路线承担着截然不同的历史使命。
- 药物发现阶段:核心诉求是“构效关系+速度”。化学家们需要快速制备出多样化的化合物以供筛选。
- 临床前研究阶段:此时的路线需要做到“与目的相适应”,满足初步的毒理和药效评估。
- 临床研究阶段:核心转向“供应研究需要”。此时需求量从毫克级跃升至更高量级,路线的稳定性成为焦点。
- 商业生产阶段:终极目标是“供应病人需要”并最大幅度地“减少产品成本”。
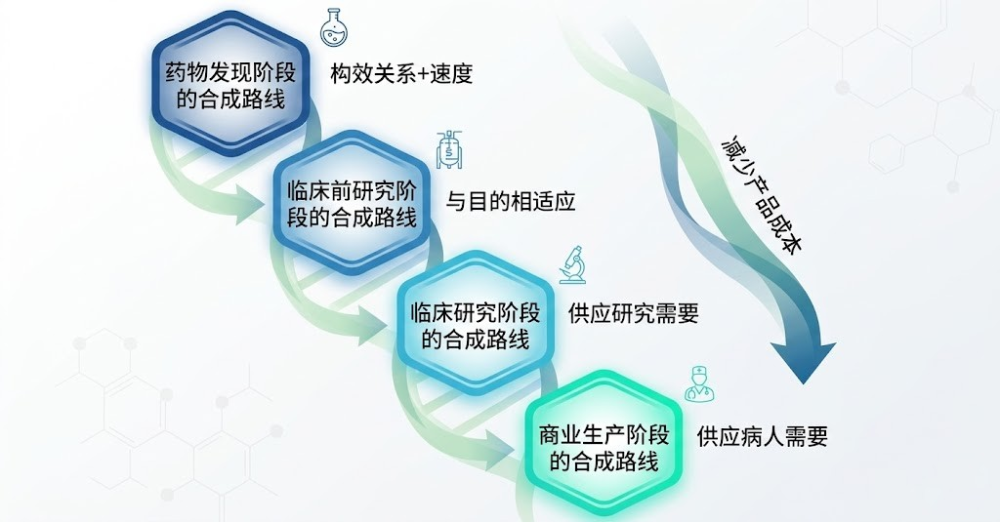
随着项目推进,决定候选药物能否进入下一个GO/NO GO决策节点的不仅是药效数据,还包括两个极具现实意义的供应链拷问:项目推进到底需要多少数量的API?现有合成路线的知识基础和信息储备是否足够支撑放大生产?
二、控本四重奏:路线转化与放大的核心策略
API的交付数量与生产成本存在直接的正相关。要实现研发资源的高效配置,必须在路线转化与放大过程中贯彻以下四大策略:
1. 精准聚焦:基于数据节点的API产能规划
最节省资源的投资策略,是仅生产满足当前GO/NO GO决策节点最低需求量的API。但这并非一成不变的铁律。为了保障后续研究的无缝衔接,有时需要提前生产备用API,或是基于积极的数据反馈进行“预先投资”生产第二批次。另一种折中方案是大量合成中间体,仅将部分转化为API,剩余的用于潜在的再补给或衍生物合成。这种策略在面临NO GO结局时,能有效止损。
2. 效率与收率的博弈:优化与直推的抉择
生产效率越低,成本自然越高。研发团队常常面临一个灵魂拷问:是直接使用现有路线进行放大,还是先停下来进行工艺优化?直接放大往往成本效益更高,但必须严格评估化学操作的不可重复性风险以及对环境、健康和安全(EHS)的基本要求。在定制(FFP)生产中,适度的研发投入以规避工艺安全隐患是必要的。此外,不要盲目追求理论上的高收率,而忽视了产量不达标带来的系统性风险。
3. 周期与资源的链式反应
产品成本的另一大驱动因素是时间周期、原材料获取难度以及人力资源投入。某些材料在实验室小试时唾手可得,一旦放大就可能面临价格暴涨或供应链断裂,进而无限期拉长生产周期。同时,减少生产步骤和人力干预能显著降低成本,反之,引入昂贵的替代试剂则会迅速推高账单。
4. 隐形成本的资本化:安全与合规的代价
为了推动化合物通过决策点而预先投入的研发成本,实际上与最终的生产成本深度绑定。例如,特殊资产采购、废弃物管理和监测测试等成本,都应当被计入总体核算中。但在达成集中生产指标前,不必过度追求路线的完美,单元操作优化、溶剂更换或结晶优化等工作可以根据项目进度灵活调整。
API可持续发展战略的组成部分和价值驱动因素
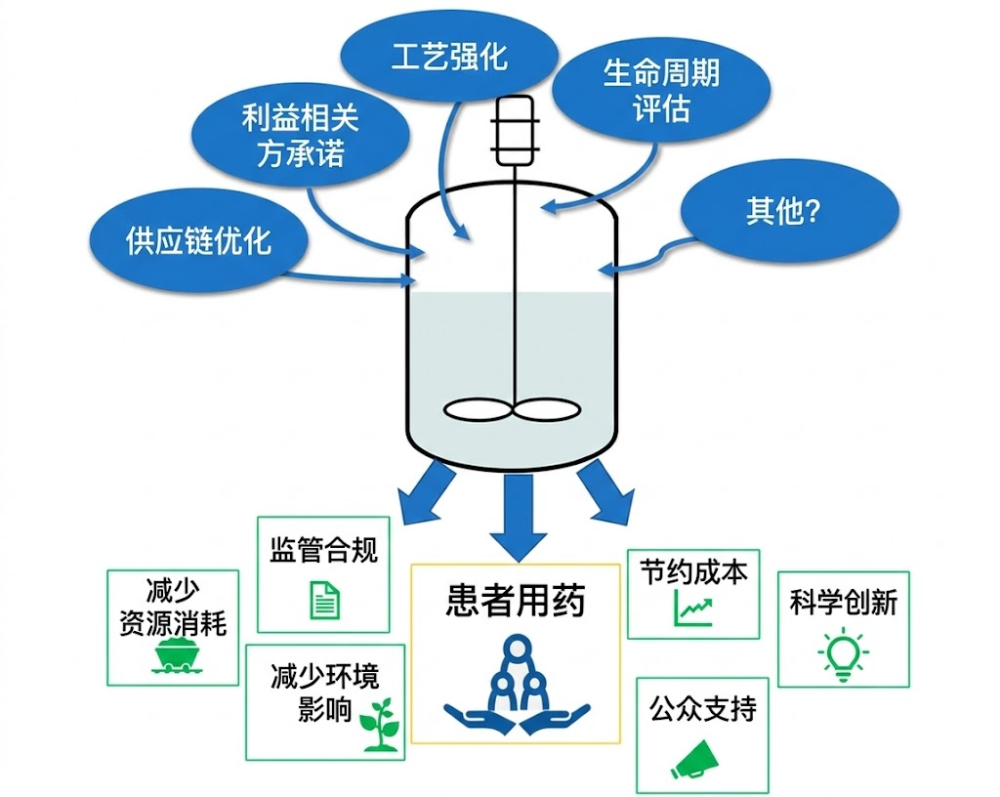
三、催化剂与原材料的陷阱:“完美”往往是放大的敌人
在将化合物推向临床供应链的过程中,起始原料和催化剂的选择堪称“生死劫” 。在发现阶段随处可得的起始原料,到了临床供应阶段可能面临严重的产能受限 。为了规避这种“无米下锅”的系统性风险,精算团队在早期即需引入动态的供应链监控机制。可以通过调用摩熵医药等行业数据库中关于关键中间体和起始物料的供应商产能分布、合规登记状态及历史价格波动趋势,能够在化学家着手优化前,提前剔除那些在工业化尺度上具有高供应链断裂风险的“完美路线”。如果化学家无法高效采购,就必须立刻投入额外研发成本自行合成,或是紧急开发备用路线。
催化剂的选择更是充满了反直觉的行业逻辑。一个简单的实验投入可能极大地改变产品成本,但“效率最高”的催化剂绝对不等于最佳选择。
- 理想与现实的落差:假设催化剂A能达到100%的收率和100%的选择性,它无疑是药物化学家的“梦中情剂”。但到了临床前及临床开发阶段,随着需求量激增,其高昂的价格和漫长的采购周期将直接扼杀项目的财务可行性。
- 务实的技术折中:相比之下,催化剂B虽然只能提供97%的收率和选择性,但如果它极易获取且成本低廉,它才是工艺放大的真正最优解。
- 极度追求性价比:如果一种催化剂(如催化剂C)价格极其低廉,且产生的杂质易于清除、不影响目标分子收率,那么即使其收率略有瑕疵,在工业化考量下也是完全可以接受的。
四、纯化技术的降维打击:SMB如何颠覆传统分离
随着工艺向后端延伸,工程师会不断重组药物发现阶段的合成步骤(例如采用汇聚合成代替线性合成),并积极引入新技术以突破纯化瓶颈。其中,模拟移动床(SMB)色谱法(又称多柱连续色谱法,MCC)展现出了极强的颠覆性。
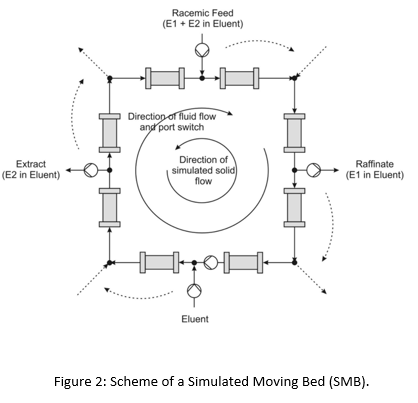
在处理难以通过结晶分离的手性化合物时,经典手性拆分往往伴随着巨大的损耗。如果在经典拆分中所需对映体的回收率仅有约45%(质量分数),通常会放弃从母液中回收残余产物。此时,SMB就成了一种极具成本效益的替代方案。
- 超高溶剂回收率:在大规模连续生产中,SMB可以回收超过99%的溶剂重复利用,几乎从根本上抹除了产品成本中的溶剂负担。
- 成本分摊与经济性:只要严格控制输入流质量,手性固定相可以被反复使用并按年摊销成本。在只存在一种杂质的理想情况下,SMB纯化手性异构体的成本甚至可以被压缩至极具竞争力的100~200美元/千克。
- 取代劳动密集型操作:相较于耗费大量劳动力和溶剂的制备柱色谱法,SMB展现出了显著的经济优势。它已成功应用于包括 依他普仑(escitalopram)和 舍曲林(sertraline)在内的多种API早期关键中间体的分离纯化。
在进行早期产品成本估算时,由于预测SMB的实际规模成本极其困难,将其成本粗略设定为每千克1000美元(约比常规分离高出5倍)是一个相对安全且合理的财务预估基准。此外,工艺路线中越早介入对映异构体的分离,其成本效益的杠杆作用就越明显。
五、建立动态成本核算模型:与时间周期的赛跑
无论选择内部生产还是外包(CDMO),对中间体或API进行初始的产品成本预测都是必修课。这并非一个静态的结果,而是一个涵盖工艺安全性分析、路线完善与修改的迭代项目。
在评估成本时,时间周期是一个无法避开的维度。我们可以构建一个“产品成本-时间周期”的象限模型来辅助决策:
- 象限C(低成本+短周期):这是所有研发团队梦寐以求的终极状态,能转化为按需研发的弹性供应链。
- 象限A(高成本+短周期)与象限D(低成本+长周期):这两类项目在早期研发中最为普遍。
- 现实困境(A类退化):许多项目最初看似路线简单,但面临试剂极其昂贵、供应量受限、地理运输壁垒或设施限制等负面因素。这会导致从启动生产到实际交付的时间被无限拉长,迫使项目从象限A跌落至不受欢迎的象限B(高成本+长周期),甚至面临项目被叫停的风险。
产品成本对时间周期的象限图
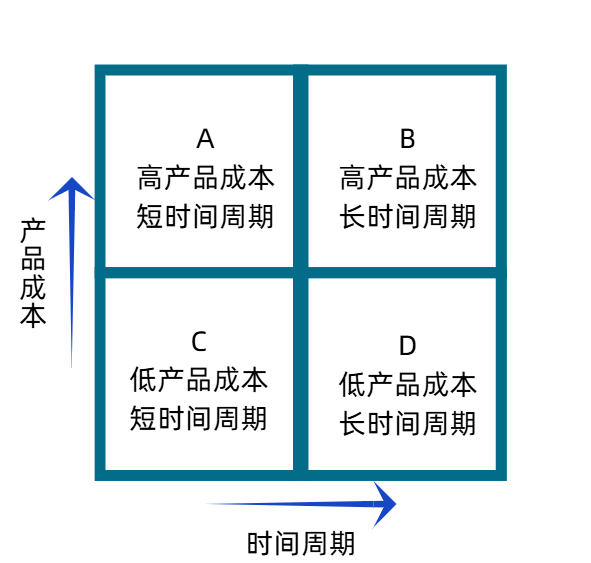
为了破解这一困局,电子表格成为了构建成本估算模型的利器。一个稳健的估算模型需要综合考量多维变量,如:
① 原料与收率:精确输入起始原料目录价格百分比、单步收率以及投入试剂的当量数量。
② 劳动力与规模经济:评估所需工时及人工费率。通常情况下,随着批量的增加,生产率上升,劳动力成本在总成本中的比重会被稀释,这就是规模经济的体现。
③ 时间系数放大的经验法则:在由实验室向大规模反应釜放大的过程中,处理时间并非线性增加。通常,每放大10倍的生产规模,所需处理时间约为原时间的2倍(即放大质量倍数的0.3次方)。
六、水面之下的冰山:附加成本与团队效能转移
除了硬核的试剂和设备成本,API开发中还潜伏着诸多容易被漏算的“柔性”与“合规”附加成本。
1. 分析验证与多晶型挑战
稳定的过程控制(IPC)和分析方法是可重复工艺的基石。如果在早期未能建立基于高效液相色谱(LCAP)或气相色谱(GCAP)的面积百分数分析标准,而是依赖液相色谱-质谱(LCMS)甚至薄层色谱(TLC)来补充数据,将会引发额外的财务负担。多晶型筛选和盐型筛选在极早期通常不计入成本,但如果针对的是吸入剂等对生物利用度和知识产权保护要求极高的项目,提前布局相关筛选将产生不可忽视的前期费用。
2. cGMP的合规溢价
在与CDMO合作时,现行药品生产质量管理规范(cGMP)环境下的操作会带来直接的附加费用。这里的核心博弈点在于监管性起始物料(RSM)的界定。
- 理论上,没有必要为RSM之前的中间体环节支付cGMP溢价。
- 但如果在研发后期监管机构对RSM的划定提出质疑,而前期步骤又是在非cGMP环境下进行的,整个临床研究数据的合规性将面临灾难性的风险。
- 因此,精算团队通常会选择在标定的RSM之前额外多安排一到两个步骤在cGMP条件下执行,以平衡合规风险与成本。
3. 从“药化”到“工艺化”的关键跳跃
随着NCE的推进,研发主导权必须从药物化学(MedChem)放大小组顺利交接到工艺化学放大小组。
- 药化团队优先追求的是速度。
- 工艺化团队则聚焦于工艺设计、安全性评估、采购经济性以及结晶纯化体系的建立。此外,如何根据现有反应釜的容量(例如100L级别的哈氏合金反应釜)进行容器适配以最大化提升经济效益,也是工艺团队的核心优势所在。
七、结语
将候选药物从早期发现推向临床的征途中,产品成本(CoG)绝对不是一个可以在后期再做清算的财务数字,而是一个高度动态、贯穿路线选择、操作评估和新兴技术应用全周期的战略工具。

明确核心假设,精准运用SMB等替代技术,建立严密的成本估算多维模型,并妥善管理向工艺化团队及CDMO的权责交接,是实现高成本效益新药研发的必由之路。只有真正掌握了早期API成本的底层逻辑,我们才能在这场极度烧钱的医药长跑中,为突破性疗法的最终突围备足“弹药”。
扩展阅读:
1. 新药开发提速!BMS经典战略解码FS-to-FIM加速逻辑
2. 深度解析原料药(API)的早期工艺开发:从“科学发现”到“临床验证”的破局之路
3. 新药研发全景图:从分子发现到临床确证,再到上市后监测的挑战
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论