肺癌作为全球发病率和死亡率均居首位的恶性肿瘤,其防控与治疗成为了医学界关注的焦点。非小细胞肺癌(NSCLC),作为肺癌的主要类型,其复杂的病理机制和多样的基因突变类型,给临床治疗带来了巨大挑战。随着现代生物技术和医学研究的不断深入,靶向治疗和免疫治疗等新型治疗手段的出现,为NSCLC患者带来了前所未有的治疗希望和生存机会。
本文基于摩熵咨询最新发布的《市场研究专题报告——非小细胞肺癌药物》部分精彩内容,旨在全面梳理非小细胞肺癌流行病学数据及其治疗领域的最新进展,探讨靶向治疗和免疫治疗如何重塑NSCLC围手术期治疗格局,同时还将对NSCLC市场趋势以及未来的治疗方向和药物研发热点进行前瞻性分析,以期为研究人员、临床医生及相关从业者提供有价值的参考信息。
一、非小细胞肺癌流行病学数据
1. 全球肺癌新增病例数和死亡数位列癌症榜首
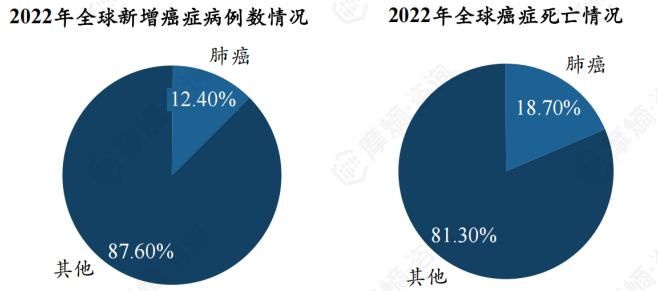
近年来,肺癌的高发病率和高死亡率造成全球负担。据数据显示,2022年全球新增癌症病例数达到2000万例,其中肺癌新增病例约为250万例,占比高达12.4%;男性肺癌患者占总新增癌病病例数的比例为15.3%,女性为9.4%。
同年,全球因癌症死亡病例共970万例,肺癌死亡病例数为180万例,占比达18.7%;其中,男性肺癌患者死亡数量占所有癌症死亡病例数的比例为22.7%,女性为13.6%。
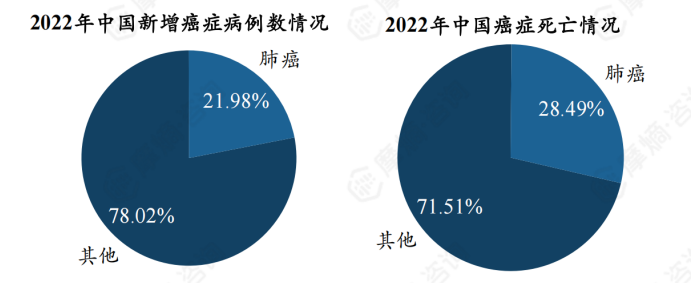
在中国,肺癌的流行形势同样严峻,是发病率最高和死亡率最高的癌症之一。2022年,中国癌症新发病例数为482.47万,其中肺癌新发病例达106.06万,发病率位居首位;同年癌症死亡总人数为257.42万,肺癌死亡人数高达73.33万,亦居首位。性别差异上,男性肺癌的发病率和死亡率均显著高于女性,分别为91.36/10万和71.55/10万,而女性则为58.18/10万和31.47/10万。
2. 中国肺癌以非小细胞肺癌为主,其EGFR突变占比超50%
肺癌主要分为非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)两大类,其中NSCLC占比高达90.34%,是肺癌的主要类型。NSCLC按病理分型可进一步细分为鳞癌(占比43.3%)、腺癌(占比45.31%)、腺鳞癌、大细胞癌等。
从基因分型来看,EGFR、KRAS和ALK是中国NSCLC患者中最常见的突变类型。2016年复旦大学附属肿瘤医院团队在《Oncotarget》上,发表了一项对1770例手术切除NSCLC样本(1305例为肺腺癌)的回顾性分析,显示中国EGFR、KRAS和ALK仍为NSCLC患者中最常见的三种突变,占比在整体人群中分别为50.3%、6.7%和4.3%。
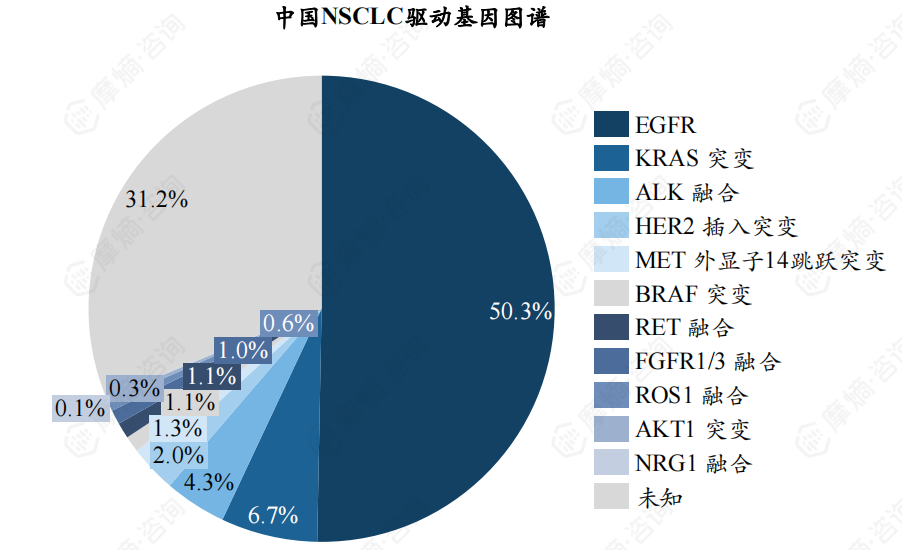
图片来源:摩熵咨询《2023年市场研究专题报告——非小细胞肺癌药物》
此外,中国NSCLC的核心驱动基因还包括HER2插入突变、MET外显子14跳跃突变、BRAF突变、RET融合、FGFR1/3融合、ROS1融合、AKT1突变、NRG1融合等。
3. 靶向治疗和免疫治疗正在重塑I-III期早期NSCLC围手术期治疗格局
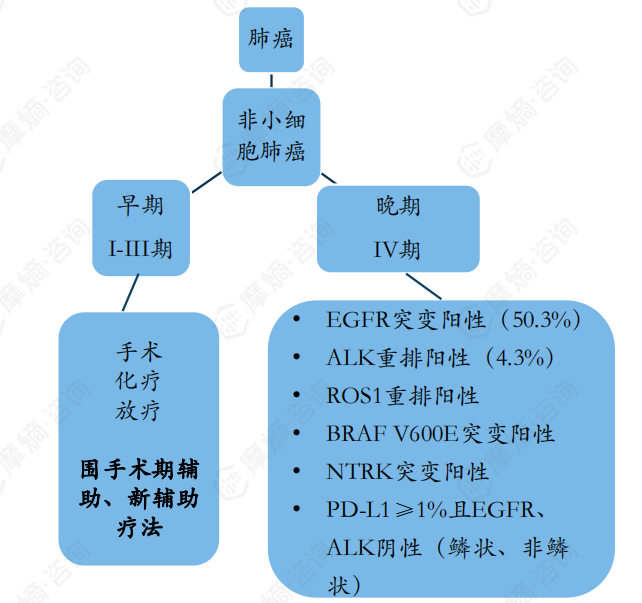
非小细胞肺癌按疾病进展情况可以分为I-IV期,I-III期为早期,一般治疗方式为手术+放化疗。随着靶向治疗和免疫治疗的兴起,正在改变和重塑NSCLC围手术期治疗格局。
新辅助化疗是指在实施局部治疗方法(如手术或放疗)前所做的全身化疗,缩瘤降期,降低手术难度,清除微残留或微转移病灶,减少复发风险,提高总生存。推荐联合纳武利尤单抗、帕博利珠单抗、替雷利珠单抗、度伐利尤单抗、特瑞普利单抗、卡瑞丽珠单抗等PD-(L)1新辅助治疗。
辅助治疗通常是手术后给予的治疗,以消灭体内任何仍然残余的癌细胞,以降低肿瘤复发或向其他部位播散的可能性。
按照治疗模式的不同,IV期NSCLC包括驱动基因阳性和阴性,其中驱动基因阳性包括EGFR突变、ALK融合阳性突变、其他驱动基因阳性突变,其中驱动基因阴性包括非鳞癌(腺癌为主)、鳞癌。
根治手术后,EGFR阳性患者推荐奥西替尼,埃克替尼辅助治疗、ALK融合患者推荐阿来替尼辅助治疗。基因驱动阴性患者,推荐阿替利珠单抗(PD-L1 TC≥1%)、特瑞普利单抗、帕博利珠单抗、替雷利珠单抗、卡瑞丽珠单抗、度伐利尤单抗、纳武利尤单抗。
二、非小细胞肺癌市场趋势分析
1. KRAS、 Her2插入突变等NSCLC仍有较大未满足的临床需求
尽管治疗进展显著,但KRAS突变和Her2插入突变等NSCLC亚型的临床需求仍未得到充分满足。KRAS突变在中国NSCLC患者中占比6.7%,Her2插入突变占比达2%,但目前国内市场尚无针对这些靶点的新药获批上市。
就KRAS突变的NSCLC药物研发情况来看,美国已有两款药物获批上市,分别是安进公司的AMG 510(Sotorasib),于2021年5月经FDA获批上市;Mirati Therapeutics/再鼎医药的MRTX849(Adagrasib),于2022年12月经FDA获批上市。两款药物均是针对KRAS G12C突变的小分子抑制剂,目前在国内处于III期临床阶段。
在国内,已有3款KRAS G12C抑制剂处于申请上市阶段,分别为信达生物/劲方医药的IBI-351、益方生物/正大天晴的D-1553、加科思的Glecirasib/JAB-21822。国内KRAS G12C抑制剂迎来研发热潮,竞争愈发激烈。“国内首款”的殊荣最终花落谁家,值得期待。

就治疗HER2插入突变的NSCLC药物研发情况来看,第一三共/阿斯利康的德曲妥珠单抗(T-DXd,Enhertu,DS-8201)已获得欧盟和FDA批准上市,并于2023年2月在我国获批上市,用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
德曲妥珠单抗是靶向HER2突变的ADC药物,也是非小细胞肺癌(NSCLC)治疗领域首个获批用于经治HER2突变晚期NSCLC患者的ADC药物。摩熵医药数据库显示,DS-8201已在全球不同地区获批用于乳腺癌、非小细胞肺癌、胃癌、胃食管交界处腺癌等多种癌症的治疗。
DS-8201全球适应症研发情况(部分)
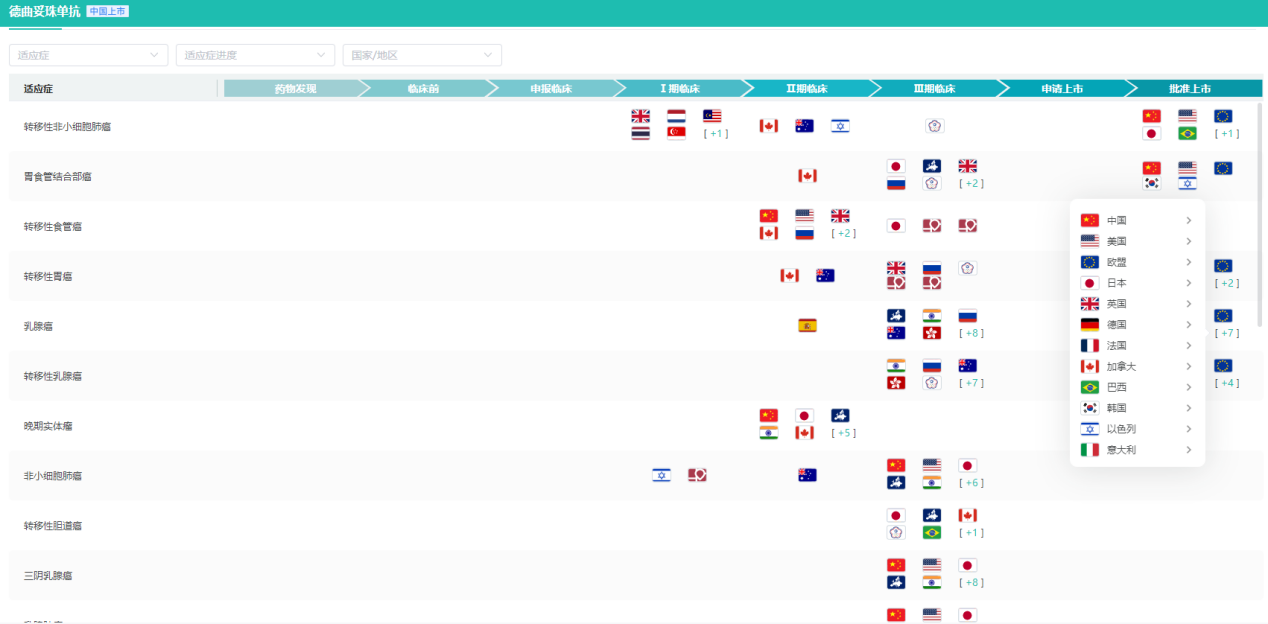
图片来源:摩熵医药数据库
恒瑞医药的吡咯替尼,已于2018年8月在国内获批上市,有真实世界回顾性研究表明吡咯替尼联合抗血管生成药物治疗HER2突变的晚期NSCLC有良好的疗效和耐受性。研究结果显示,中位无进展生存期(PFS)为7.13个月,客观缓解率(ORR)为19.6%,疾病控制率(DCR)为94.4%,中位总生存(OS)为19.50个月,接受阿帕替尼或安罗替尼/贝伐珠单抗治疗的患者的PFS无差异。
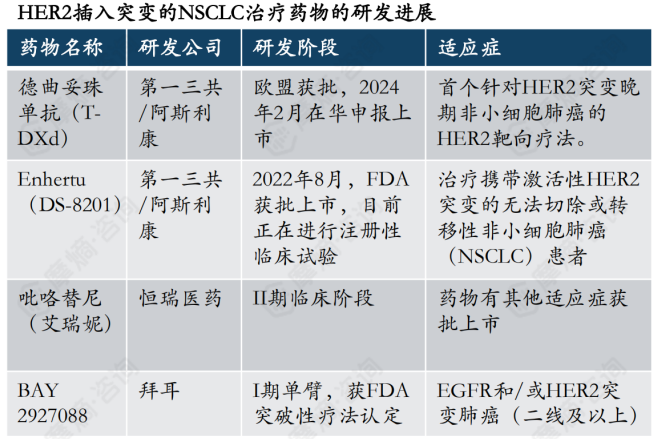
吡咯替尼(马来酸吡咯替尼片)是中国首个自主研发的抗HER1/HER2/HER4靶向药。作为一种小分子、不可逆、泛ErbB受体酪氨酸激酶抑制剂,吡咯替尼通过阻止肿瘤细胞内表皮生长因子(EGFR)和HER2的同质和异质二聚体形成,抑制其自身的磷酸化,阻断下游信号通路的激活,从而抑制肿瘤细胞生长。
吡咯替尼继2018年8月获得有条件批准上市后,于2020年7月获得国家药品监督管理局完全批准,2019年纳入国家医保目录,用于联合卡培他滨治疗HER2阳性、接受过曲妥珠单抗治疗的复发或转移性乳腺癌患者。2022年和2023年分别获批第二个适应症和第三个适应症,为乳腺癌患者提供治疗新选择。
摩熵医疗数据是基于多方来源脱敏后数据,涵盖多城市全科室已发生的标准数据产品,能够更深入地挖掘市场竞争情况及变化趋势,帮助客户评估治疗领域及产品市场潜力,赋能药品多个关键环节,从而发现更多机会。
摩熵医药药物流向数据,是与全国各省市多家药品流通配送商合作,脱敏合规统计的药物在全国的流向数据,落地到具体医院,可覆盖全国三级医院3000+,二级医院10000+,一级和未定级医院75000+。
2. 同癌异治、分期分层分级精准治疗已成为NSCLC诊疗的主流模式
同癌异治、分期分层分级精准治疗已成为NSCLC诊疗的主流模式。针对EGFR、ALK等相对成熟靶点,序贯靶向治疗已成为核心策略。
免疫联合治疗正逐步成为新常态。以PD-(L)1为代表的免疫疗法正逐步成为晚期NSCLC的基础疗法,特别是在围手术期辅助、新辅助疗法是个巨大的潜力市场。
未来,新一代免疫检查点抑制剂,如TIM-3抗体、TIGIT抗体、 LAG-3抗体、 PVTIG抗体、 ILDR2抗体、 CTLA-4抗体、甚至双靶点抗体有望带来更好的疗效。以及ADC等新型技术的涌现,将进一步丰富NSCLC的治疗手段,为患者带来更好的治疗选择和生存希望。
结语:
非小细胞肺癌的流行病学数据揭示了其严峻的防控形势,而治疗策略也正经历着从传统手术和放化疗向靶向治疗和免疫治疗的转变。随着治疗技术的不断进步和市场趋势的积极变化,未来的治疗将更加精准和个性化,以满足不同患者群体的需求。国内外的研究和药物开发正在加速,预示着未来治疗选择的多样化和优化,为患者点亮希望之光。
拓展阅读:
1. 2024年EGFR与ALK突变非小细胞肺癌(NSCLC):诊疗指南及市场竞争格局分析
2. 2024年非小细胞肺癌(NSCLC)罕见突变靶向治疗及市场竞争格局
3. 2024年NSCLC治疗前沿:PD-(L)1和VEGF抑制剂的市场表现与临床应用
以上内容均来自摩熵咨询{市场研究专题报告——非小细胞肺癌药物},如需查看或下载报告,可点击!
<END>
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论