
近日,近一年内被毙最多的产品乙酰半胱氨酸注射液迎来了首仿,这个自2024年以来被驳回企业最多的产品看见了曙光。
而被毙第二多的“氟比洛芬凝胶贴膏”前途却仍旧暗淡——氟比洛芬凝胶贴膏自2020年起共有21条申请上市的一致性评价受理号,其中13条已被驳回。
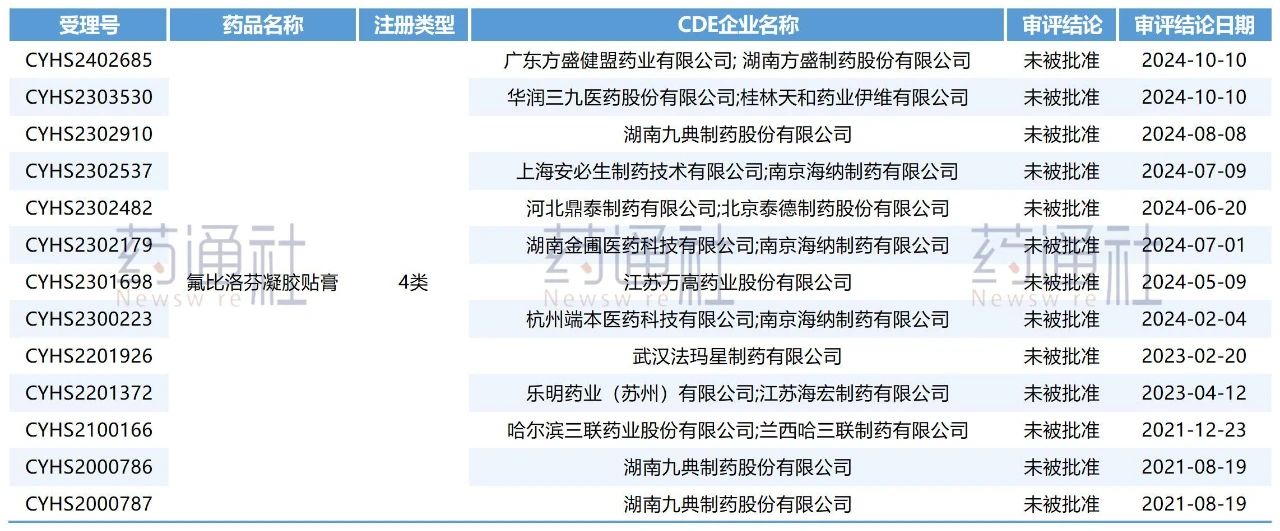
图 | 13条被驳回审评记录
数据源 | 摩熵医药(原药融云)数据库
提到国内贴膏剂,首先会想到中药贴膏。中药贴膏即传统贴膏,两只老虎(壮骨麝香止痛膏)就是最经典的中药贴膏之一,其他还有云南白药膏、麝香追风膏、镇痛贴膏等知名产品。据摩熵医药(原药融云)数据库,中药贴膏现行有效批文495个,品类繁多。
而与之相对,化药贴膏数量寥寥无几,仅29个批文,其中国产化药贴膏仅12个。
从销售数据来看,2023年医院全终端用于肌肉骨骼系统用贴膏销售额在132亿元,其中中药贴膏80亿元,占比60.6%;化药贴膏52亿元,占比不到40%。
而在这52亿化药贴膏市场之中,上述提到频繁被毙的氟比洛芬凝胶贴膏销售额就有28亿元,第二的是洛索洛芬钠凝胶贴膏,销售额13.4亿。
两大品种加起来占据全部化药贴膏的80%市场,这与百花齐放、势均力敌的中药贴膏市场格局截然不同。
目前氟比洛芬凝胶贴膏仅有2个批准字号(三笠制药株式会社、北京泰德制药股份有限公司),洛索洛芬钠凝胶贴膏仅1个现行有效的批准字号(湖南九典制药股份有限公司),凭着3个文号销售额就斩获近40亿的市场规模,市场不可小觑,因此很多仿制药企业觊觎这两个品种已久。
但仿制不容易,正如开头所说——氟比洛芬凝胶贴膏自21年起已经被毙了13条了。

氟比洛芬凝胶贴膏原研为日本三笠制药,2010年,泰德制药通过“原研产品直接进口、国内进行分包生产”方式,将40mg/贴的氟比洛芬凝胶贴膏引进中国市场,其商品名为“泽普思”。这是国内上市最早的化药凝胶贴膏剂产品。
2011年,泰德制药推出了自研的氟比洛芬凝胶贴膏仿制药,商品名为“得百安”,并迅速占领了超过80%的市场,成为了仿制取代原研的经典成功典例之一。但是自那以后,国内再无第二个氟比洛芬凝胶贴膏仿制药上市。
从2011年到现在仍无第二家仿制上市,连续13次失败,这真是传奇了,甚至就连泰德制药自己也被驳回。早期得百安上市时国家还未开展一致性评价,23年泰德重新进行一致性评价申报时,一样未被批准。
洛索洛芬钠凝胶贴膏原研厂家是日本LEADCHEMICALCO.,LTD.销售公司为第一三共株式会社,2014年进入我国,九典制药的洛索洛芬钠凝胶贴膏是在原研厂商LEAD的洛索洛芬钠贴剂基础上做了剂型改良,于2017年获国家药监局批准上市,原研批准字到期未续,洛索洛芬钠凝胶贴膏目前没有直接竞争对手。
洛索洛芬钠凝胶贴膏销售额不及氟比洛芬凝胶贴膏,经历也不及前者曲折,目前多家企业正在进行仿制申报,还也未有企业折戟沉沙,但这也是目前情况,后续审批情况不知。

图 | 洛索洛芬钠凝胶贴膏一致性评价申报情况
数据源 | 摩熵医药(原药融云)数据库
除这两大品种外,化药贴膏其余产品仿制情况也不太好,目前有仿制成功的产品仅九典制药的酮洛芬巴布膏,仿制上市申请被受理的品种也只有洛索洛芬钠贴剂和和吲哚美辛凝胶贴膏两种。
国内对化药贴膏新药研发进展也较为缓慢,仅一个按照化药2.2类申报的贴膏(长沙晶易医药的KEM2104凝胶贴膏已获得临床默示许可),根据晶易医药官网发布,KEM2102凝胶贴膏,是一种强效的解热镇痛消炎药,是治疗骨、关节和软组织风湿病等炎性病变所致疼痛。
获批难度在哪里?
凝胶贴膏剂的处方成分多,成型工艺复杂,技术壁垒高,尤其是对于药物进入皮肤组织的渗透速率控制难度大,药效差异大。
2022年05月30日CDE针对外用局部给药药物制定了《局部给药局部起效药物临床试验技术指导原则》写明:
申办方应基于药物特征,采取逐步递进的对比研究,依次开展药学、非临床和/或临床对比研究。申办方应基于药物制剂学特点、药学和非临床对比研究的结果,如因制剂学等原因,药学和非临床对比研究难以明确仿制药与参比制剂的一致性,申请人可在前期研究的基础上,考虑开展必要的临床对比研究,可包含以以药代动力学为终点的生物等效性研究(PK-BE)、以药效学为终点的生物等效性研究(PD-BE),以及以临床指标为终点的等效性研究。
还是以氟比洛芬凝胶贴膏为例,当前各申报企业的实践路径,大多数企业仍聚焦于PK-BE研究作为核心策略,但从被毙的企业来看,凝胶贴膏的获批似乎还需要做完整的临床试验。
比如,湖南九典制药已经连续三次对此品种发动攻坚,但仅做PK-BE的都被驳回了,早在2022年,九典就已经登记了III期临床试验,目标入组450人,第二次以仅完成PK-BE试验就申报大概是抱着赌一把的心思进行的,以失败告终,目前老老实实在进行大临床,九典是决心花大价钱也要拿下此品种了。
而洛索洛芬钠凝胶贴的申报,角质层胶带剥离法的皮肤药代动力学(DPK)已经被证实不被CDE接受,2021年武汉法玛星制药有限公司提交的BE实验结论不被批准。同样2022年3月南京海纳医药科技股份有限公司提交的DPK的BE实验也主动撤回。
洛索洛芬钠凝胶贴膏后续申报跟氟比洛芬凝胶贴膏一样走的是以PK-BE研究建立自研制剂和参比制剂的生物等效性,目前来看,新申报的BE实验均采用这种PK-BE的方式。
但氟比洛芬凝胶贴膏已证明仅进行PK-BE实验难以获批,洛索洛芬钠凝胶贴膏结果会如何不好说。
也有几家企业考虑到了仅PK-BE试验被毙的可能性,比如北京泰德制药,他家的洛索洛芬钠凝胶贴研发就采取了直接进行大临床的做法,2022年登记了III期临床试验,目标入组500例。
(OS:湖南九典和北京泰德这两家公司还挺有意思,互相布局对方的强势产品,一出手直接进行大临床,属实是针尖对麦芒了。)
分析这两大产品的仿制之路就会发现,先行者的经验格外重要。等这两个品种被攻破,届时化药贴膏是选择抢占中药贴膏市场还是同品类内卷降价进集采?就拭目以待了。
参考来源:邴药说
<END>
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!


















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论