
免疫检查点抑制剂ICIs改变了许多癌症的治疗方法,ICIs有效性预测的生物标志物中PD-L1应用相对更多。通常组织PD-L1蛋白表达主要通过免疫组化的方法来检测,量化指标为肿瘤细胞阳性比例分数(TPS)、综合阳性评分(CPS)和免疫细胞阳性比例分数(IPS)。但是,由于瘤内异质性,同一个肿瘤组织可能部分表达阳性、部分表达阴性,也可能会发生动态变化等因素,组织PD-L1表达量并不能完美预测免疫治疗的效果。
有学者就将目光投向了外泌体,外泌体表面是否携带PD-L1?是否具有功能?是否能够作为免疫治疗预测因子?
首先恩博一一举证回答上述问题,文末有外泌体PD-L1检测解决方案噢。
2018年,研究者发现外泌体表面携带PD-L1,且肿瘤外泌体PD-L1在免疫抑制中扮演重要角色;转移性黑素瘤患者中,循环外泌体PD-L1的水平与IFN-γ的水平呈正相关,在抗PD-1治疗过程中变化;在治疗的早期阶段,循环外泌体PD-L1的增加幅度可作为肿瘤细胞对T细胞更新的适应性反应的指标,从而区分临床应答者与非应答者,该研究发表在Nature杂志(Exosomal
PD-L1 contributes to immunosuppression and is associated with
anti-PD-1 response. Nature. 2018;560(7718):382-386. IF=50.5 1区)。
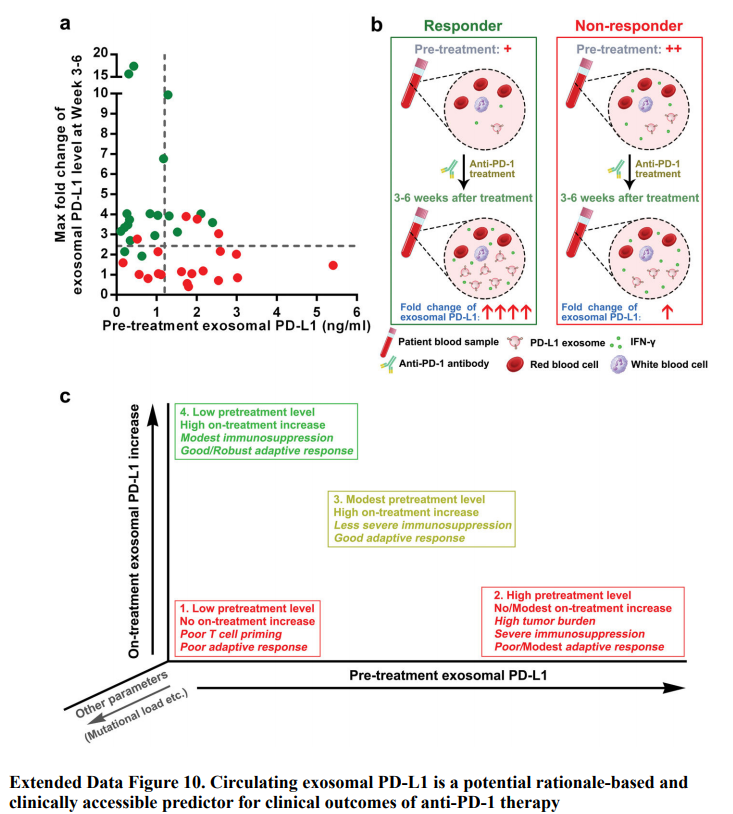
2020年,一项前瞻性的临床试验研究了黑色素瘤患者血浆外泌体PD-L1水平是否可用于预测患者对免疫治疗的反应。研究发现:PD-L1是由黑色素瘤细胞通过外泌体分泌的;携带PD-L1的外泌体具有免疫抑制特性;在黑色素瘤患者的血浆(N=30)中,外泌体中的PD-L1水平(中位数64.26
pg/mL)明显高于可溶性PD-L1。所有患者均检测到外泌体体PD-L1,只有67%的肿瘤活检组织PD-L1呈阳性。基线外泌体PD-L1水平与临床病理特征无关,但在治疗后相比于基线的变化(ΔExoPD-L1)与肿瘤对治疗的反应相关。ΔExoPD-L1的阈值大于100,对疾病进展的敏感性为83%,特异性为70%,阳性预测值为91%,阴性预测值为54%。ΔExoPD-L1可以对两组患者进行分层,这两组患者在总体生存率和无进展生存率方面存在统计学差异。循环外泌体中的PD-L1水平似乎是比肿瘤活检中PD-L1表达更可靠的标志物。监测循环外泌体PD-L1可能有助于预测肿瘤对治疗的反应和临床结果。(Tracking
the evolution of circulating exosomal-PD-L1 to monitor melanoma
patients. J Extracell Vesicles. 2020;9(1):1710899. IF=15.5 1区)
de
Miguel-Perez
D等在22年评估了细胞外囊泡PD-L1的表达是否可以用作预测接受ICIs治疗的非小细胞肺癌患者的持久治疗反应和存活率的生物标志物。分别在33名和39名患者的回顾性和前瞻性独立队列中,分析治疗前和治疗期间9±1周收集的血浆样本中EV
PD-L1的动态变化。与有应答者相比,无应答者的EV
PD-L1治疗后增加,是更短的无进展生存期和总生存期的独立生物标志物。相反,常用的生物标志物组织PD-L1表达既不能预测持久反应,也不能预测生存。EV
PD-L1动力学可用于对将从ICIs中获得持久益处的晚期NSCLC患者进行分层。(Extracellular
vesicle PD-L1 dynamics predict durable response to immune-checkpoint
inhibitors and survival in patients with non-small cell lung cancer.
J Exp Clin Cancer Res. 2022;41(1):186. IF=11.4 1区 )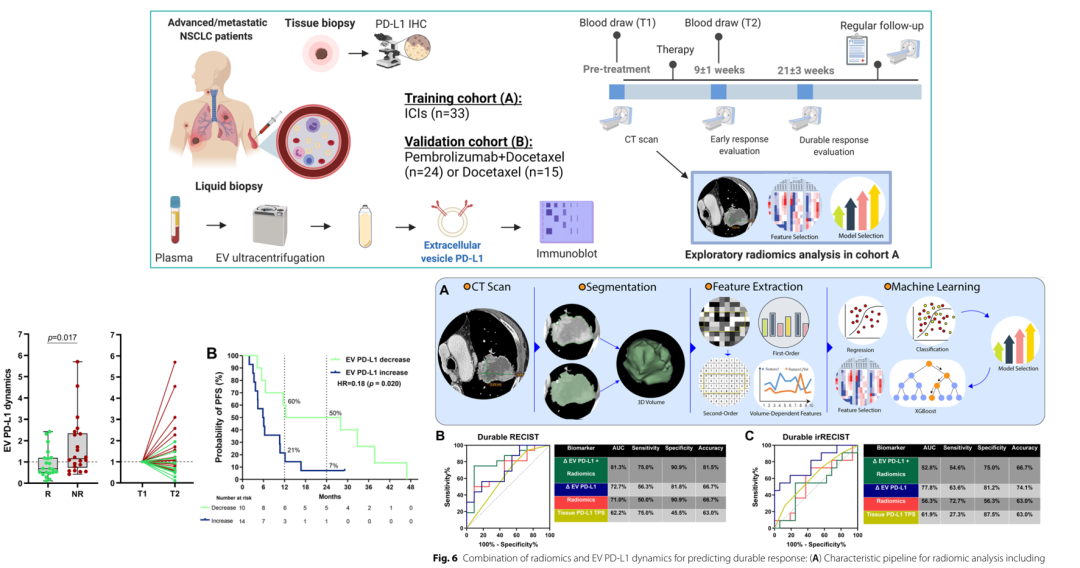
24年de
Miguel-Perez
D等,在接受ICIs加化疗的肺癌患者前瞻性队列中验证了上述模型,(17例接受Pembrolizumab+Docetaxel联合治疗,13例接受Docetaxel治疗,27例接受ICIs治疗),并将其与单独接受化疗的患者进行了比较。该多参数模型在识别ICIs治疗无应答者方面表现出高度的敏感性和特异性,其表现优于组织PD-L1,与肿瘤变化直接相关。放射组学和EV
PD-L1动力学的结合是一种微创且有前景的生物标志物,可用于对接受ICIs的患者进行分层。(Validation
of a multiomic model of plasma extracellular vesicle PD-L1 and
radiomics for prediction of response to immunotherapy in NSCLC. J Exp
Clin Cancer Res. 2024;43(1):81. IF=11.4 1区)
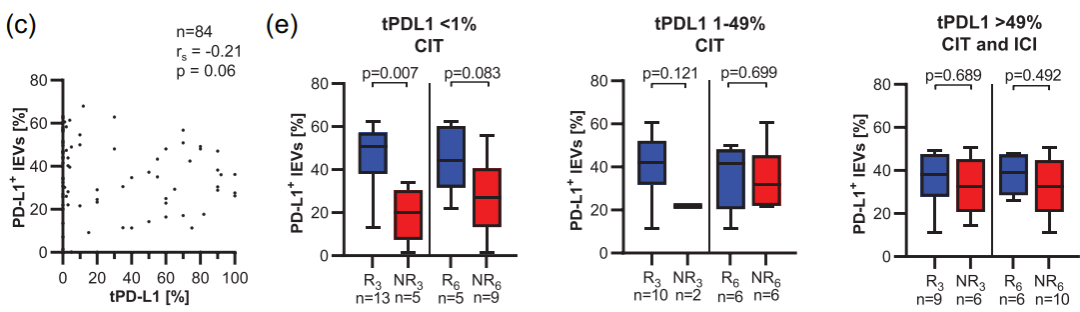
组织PD-L1(tPD-L1)的高表达是目前唯一被批准用于预测治疗反应的生物标志物。然而,即使tPD-L1低(1-49%)和缺失(<1%)的患者也可能从免疫疗法中受益,但迄今为止,还没有可靠的生物标志物可以预测这一特定患者亚组的反应。Schöne
N等24年3月发表在JEV中这项研究,旨在测试肿瘤相关的细胞外囊泡(EV)是否可以填补这一空白。通过对非小细胞肺癌细胞系研究发现,与较小的EV相比肿瘤相关抗原在较大的EV(lEV)上富集。携带这些抗原的lEV在NSCLC患者(n=108)血浆中的水平显著升高,并将其与对照组(n=77)区分开来。血液中PD-L1+
lEV基线水平较高的患者对免疫治疗的反应明显更好,生存期也更长。在tPD-L1表达低或缺失的NSCLC患者亚组中尤其如此,因此将血浆中PD-L1阳性的lEV鉴定为免疫治疗新的疗效预测和预后标志物。(PD-L1
on large extracellular vesicles is a predictive biomarker for therapy
response in tissue PD-L1-low and -negative patients with non-small
cell lung cancer. J Extracell Vesicles. 2024 May;13(5):e12443.
IF=15.5 1区)

前面所述的研究,在非小细胞肺癌和转移性黑色素瘤中,证实了胞外囊泡EV
PD-L1相比于肿瘤组织PD-L1表达,更有效预测免疫治疗疗效以及预后,尤其是组织PD-L1低表达或缺失的患者中。当然有些研究中是免疫治疗或免疫治疗联合化疗治疗前,即基线EV
PD-L1水平,有些是治疗后相比于治疗前的EV
PD-L1变化水平即ΔEV
PD-L1。
也有研究发现:初诊时循环外泌体的高PD-L1含量与骨肉瘤患者肺转移、多发转移和死亡等临床病理疾病标志物之间存在显著的正相关,初诊循环外泌体PD-L1可预测骨肉瘤患者的预后和生存率。(Circulating
Exosomal PD-L1 at Initial Diagnosis Predicts Outcome and Survival of
Patients with Osteosarcoma. Clin Cancer Res. 2023;29(3):659-666.
IF=10.0 1区)也就是说EV
PD-L1水平不只能预测免疫治疗疗效及相关预后,也可能可以提示强免疫抑制,促进转移、死亡等。

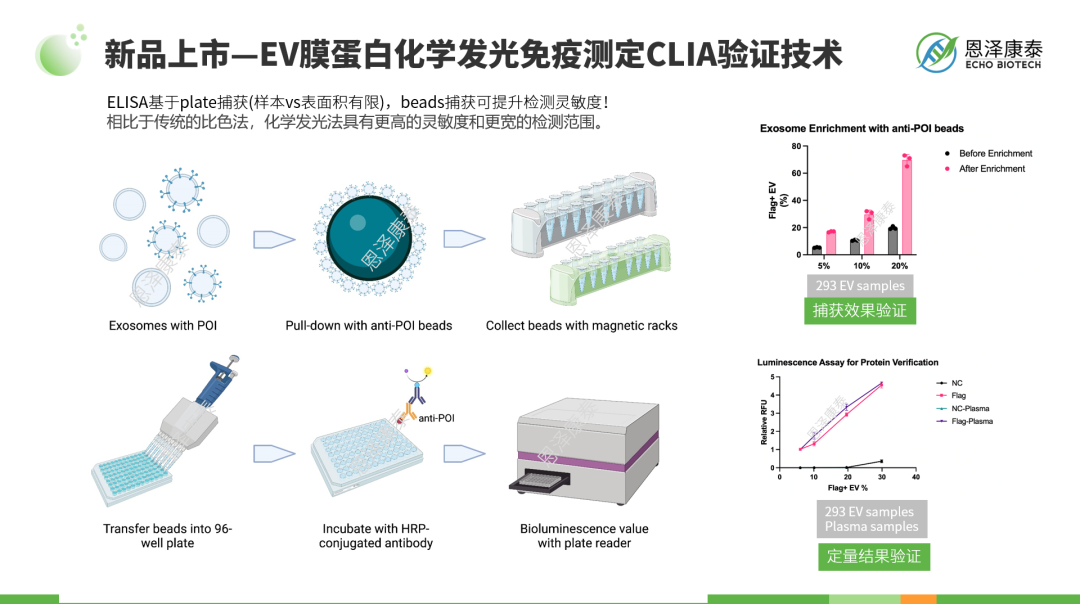
您可能又有一个问题,说的这么好,怎么检测外泌体PD-L1呢?恩泽康泰即将上新EV膜蛋白化学发光免疫测定CLIA验证技术,鉴于上述外泌体PD-L1的研究价值,现基于该技术推出EV
PD-L1助力肿瘤免疫治疗疗效和预后预测标志物研究计划(简称EVP-IB计划)。
1.以肿瘤免疫治疗(及联合治疗)疗效和预后预测为研究目的;
2.目前已知疗效(应答、不应答)和PFS/OS等信息,具备组织PD-L1检测数据;
3.具备初诊和治疗后疗效评估至少1个时间点的血浆样本;
4.应答和不应答各入组≥25例/组患者,以及治疗前后2个时间点样本;
5.愿意提供应答和不应答至少3例样本供恩泽康泰测试产品性能,且数据可用于产品宣传的客户。
1.优惠项目名额:3个;
2.享受恩泽康泰资助补贴,最高补贴35%;
3.协助进行方案设计;
4.享有机器学习构建疗效/预后预测模型生信分析服务。
注:
1.科学研究为探索性研究,虽然上述研究都证实有效,但也有可能实际检测结果与预期不符。恩泽康泰保证实验严谨性,实验过程会添加阳参确保实验可靠性,并交付真实结果。如介意者勿参与本计划。
2.EVP-IB计划有效期:即日起-2024年8月31日

扫码立即报名

北京恩泽康泰生物科技有限公司成立于 2017 年,坐落于被誉为“中国药谷”的北京大兴生物医药产业基地,是致力于外泌体技术开发与临床转化的创新型高科技公司。恩泽康泰将十余年的外泌体基础研究与分子生物学、细胞生物学及生物信息学相结合,建立了具有自主知识产权的三大外泌体研究与应用平台:外泌体组学平台 Exoomics®—面对研究型医院及科研机构提供外泌体产品 / 试剂盒及外泌体科学研究整体解决方案;工程化外泌体平台 Echosome®—面对生物医药企业提供工程化外泌体载体设计开发、药物装载、靶向改造等 CRO服务;外泌体 CMC 平台 EchoPharm®—面对生物医药企业提供工程化外泌体的CDMO服务及原料生产。
公司成立以来累计获得多轮数亿元融资,现已建成超 3000 平米的外泌体 GMP 生产车间,并与国内外上千家医院、科研院校及生物企业建立合作,合作发表论文200+篇,处理不同类型的样本4万+例,申报国内外发明专利30+件,获有“国家级专精特新小巨人企业”、“博士后科研工作站”、“国家高新技术企业”、“中关村金种子企业”、北京市知识产权试点单位”等荣誉。
公司致力于通过提供系统的外泌体研究与应用解决方案,赋能临床科研,加速产业转化,并通过持续的创新和严格的质量要求,让外泌体科技推动医学发展,造福美好生活!





















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论