
免疫疗法通过激活人体免疫系统杀伤肿瘤,为彻底治愈癌症带来曙光。当前获批的大部分免疫疗法在血液瘤中效果显著,然而在实体瘤中响应率低、治疗效果差。其主要原因在于实体瘤存在复杂且高度异质的肿瘤免疫微环境,多种类型免疫细胞协同影响免疫治疗效果。理想条件下,开发出能同时调动多种免疫细胞的治疗策略,将最大程度激活免疫,提高实体瘤治疗效果。
传统免疫疗法如免疫检查点抑制剂、过继性细胞疗法等,大多只针对单一类型的免疫细胞发挥作用。双/多特异性抗体能同时结合多个靶标,因此为同时靶向不同种类免疫细胞提供了可能。
但迄今为止,大部分双/多特异性抗体实际上只能招募一种免疫细胞(如T或NK细胞)。因此,开发一种能够同时招募多种免疫细胞对抗肿瘤的方法仍然未被满足,而这对于推动免疫治疗的发展尤为关键。
2024年11月5日,北京大学陈鹏教授团队与国内多位交叉学科合作者(北京大学席建忠教授,中国医学科学院肿瘤医院康晓征教授,南京大学李颜教授,北京大学第三医院林坚研究员)在Cell杂志在线发表了题为Multimodal targeting chimeras enable integrated immunotherapy leveraging tumor-immune microenvironment的研究论文。
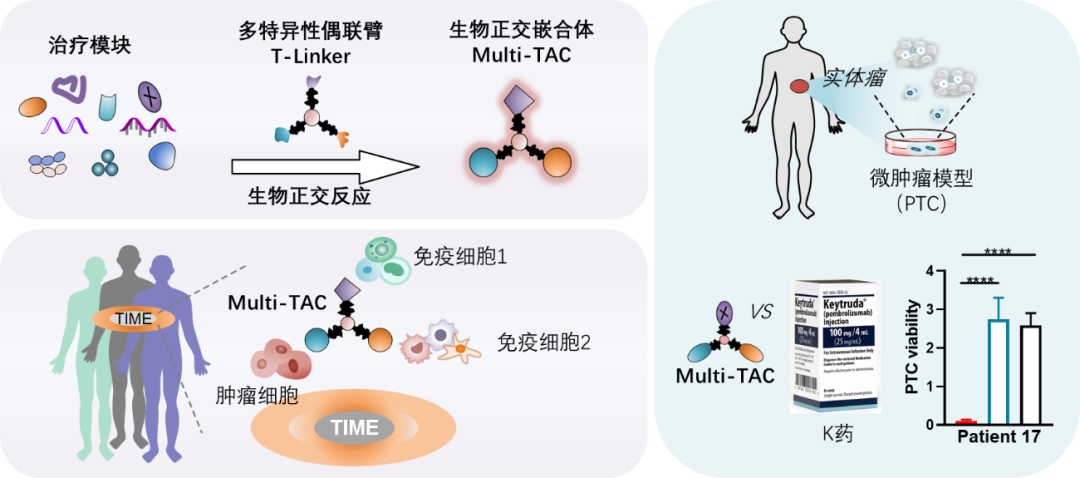
该论文系统发展了一种生物正交嵌合体平台,利用其构建的多特异性生物正交偶联臂(T-Linker),完成三种不同药物模块的特异-高效整合,形成生物正交嵌合体(Multi-TAC),实现实体瘤微环境中多种免疫细胞的同时招募,显著促进了免疫治疗效果。

首先,作者通过筛选生物正交反应,获得了三种相互正交的高效偶联反应。基于这些反应,他们合成了一种多特异性生物正交偶联臂(T-Linker)。
这一偶联臂T-Linker含有上述反应中的三种不同活性官能团,因此能同时偶联三种带有对应反应官能团的模块。
为了展示该平台的通用性,他们利用T-Linker完成了两种纳米抗体和小分子化合物、核酸、多肽、蛋白等不同模块的偶联。此外,通过进一步整合树枝状连接子和可切割型连接子,他们还展示了T-Linker用于偶联不同比例的模块分子,以及原位释放模块分子的能力。
该偶联平台具有模块化、位点特异、高效等特点,可以精准整合包括抗体在内的任意三种模块分子,以产生不同类型和用途的生物正交嵌合体Multi-TACs。
随后,作者尝试探究其构建的Multi-TAC分子能否用于招募多种免疫细胞,提高免疫治疗效果。
肿瘤中T细胞和树突状细胞(DC)已被证明能协同促进抗肿瘤免疫,因此他们开发了EGFR-CD3-PDL1 Multi-TAC用于同时招募T细胞和DC靶向肿瘤。
在体外研究中,他们证实EGFR-CD3-PDL1 Multi-TAC通过结合肿瘤细胞EGFR、T细胞CD3和DC细胞PDL1受体分子,实现T细胞-DC细胞的同时招募与肿瘤靶向。在多细胞培养体系,他们发现EGFR-CD3-PDL1 Multi-TAC通过促进“肿瘤细胞-T细胞-DC细胞”三者的物理相互作用,同时激活T细胞-DC细胞抗肿瘤免疫。
具体地,他们发现EGFR-CD3-PDL1 Multi-TAC介导的肿瘤-T以及T -DC相互作用,能瞬时激活T细胞,释放穿孔素和颗粒酶,从而直接裂解肿瘤。而EGFR-CD3-PDL1 Multi-TAC介导的T-DC相互作用,能诱导DC成熟和活化,增加肿瘤抗原的提呈、激活抗原特异性T细胞并最终完成肿瘤特异性杀伤。
进一步,作者在三种不同人源化小鼠模型中测试了EGFR-CD3-PDL1 Multi-TAC的活体治疗效果。
在人外周血单个核细胞(PBMC)重构的人源化小鼠模型中,EGFR-CD3-PDL1 Multi-TAC能明显抑制肿瘤生长,激活肿瘤组织内T细胞。在人CD34+造血干细胞(HSC)重构的人源化小鼠中,他们发现EGFR-CD3-PDL1 Multi-TAC能完全控制肿瘤生长,在激活肿瘤T细胞和DC的同时也重塑了肿瘤免疫微环境,提高了其他效应细胞如NK、NKT细胞的激活,降低了免疫抑制型Treg细胞的比例。
在转基因人源化小鼠模型中,EGFR-CD3-PDL1 Multi-TAC几乎彻底消灭肿瘤,其不但激活了肿瘤内T细胞和DC,还最终诱导了小鼠体内肿瘤特异性免疫反应,这也显示出EGFR-CD3-PDL1 Multi-TAC的治疗能够引发抗肿瘤免疫记忆。
更进一步,作者在临床肿瘤病人组织来源的微肿瘤(PTC)类器官模型中评估了EGFR-CD3-PDL1 Multi-TAC的治疗效果。
PTC是一种原代肿瘤模型,能在体外保持病人肿瘤组织的原始特征包括其免疫微环境,因此非常适合临床个性化药物的筛选。
作者通过免疫荧光、流式细胞分析和ELISA等多种手段验证了EGFR-CD3-PDL1 Multi-TAC能激活肿瘤病人组织中的T细胞和DC细胞抑制PTC的生长。
作者还将EGFR-CD3-PDL1 Multi-TAC与临床上广泛使用的PD1/PDL1免疫检查点抑制剂“K药”(帕博利珠单抗)进行了“头对头”的比较,结果发现在7例测试的肿瘤病人组织中有6例EGFR-CD3-PDL1效果明显优于“K药”。
最终,作者总共测试了6种不同癌症类型,44例肿瘤病人样本。EGFR-CD3-PDL1 Multi-TAC的整体有效率为75%,而在大部分测试的非小细胞肺癌(NSCLC)样本中,EGFR-CD3-PDL1 Multi-TAC有效率高达86%,说明EGFR-CD3-PDL1 Multi-TAC具有临床治疗潜力。
除了上述EGFR-CD3-PDL1 Multi-TAC嵌合体,作者还构建了其他Multi-TAC分子用于同时招募更多类型的免疫细胞。
作为具体展示例,他们构建和验证了EGFR-CD3-CD16 Multi-TAC,通过同时结合肿瘤EGFR、T细胞CD3和NK细胞CD16受体,实现了肿瘤靶向的T-NK细胞同时招募。
他们还构建和研究了HER2-CD3-(IMDQ)6 Multi-TAC,通过结合肿瘤HER2和T细胞CD3受体,在招募T细胞的同时,能够响应肿瘤还原性微环境,释放6分子TLR激动剂IMDQ,进而激活癌细胞周围的髓系免疫细胞。
综上,此项研究开发了一种高度模块化的生物正交嵌合体平台,该平台可精准整合多种药物模块,从而构建各种类型的多特异性生物正交嵌合体,用于同时招募T、DC、NK以及髓系免疫细胞等,靶向实体瘤免疫微环境。
作为代表,EGFR-CD3-PDL1 Multi-TAC通过介导“肿瘤细胞-T细胞-DC细胞”三者的直接相互作用,同时激活了肿瘤组织中T细胞和DC,逆转肿瘤免疫微环境,最终诱导肿瘤特异性免疫响应。
这项工作为肿瘤免疫治疗提供了一种全新的思路,同时为多细胞视角下复杂生命体系的机制研究和靶点验证提供了强大的技术工具。
原文链接:https://doi.org/10.1016/j.cell.2024.10.016
免责声明
1.Nature | 最新头条!用培养的病毒,治好自己的癌症,却陷入“伦理”风波!
2.控糖竟要从未出生开始?婴幼儿吃甜(包括在妈妈肚子里),增加成年后糖尿病和高血压风险
3.Nature子刊 | 大刊“催婚”,别具一格!单身抑郁风险增加,而婚姻是抗抑郁良药
5.别迷信“站立式”办公,跟久坐一样伤身!多站立会带来其他健康风险




































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论