 关注小药说药,一起成长!
关注小药说药,一起成长!呼吸道合胞病毒(RSV)是全球急性下呼吸道感染(LRTI)的主要原因。免疫功能低下的成年人和老年人容易受到严重感染,死亡率很高。在儿童中,呼吸道合胞病毒是LRTI最常见的原因,它是婴儿住院的主要原因之一,特别是在2岁以下的婴幼儿中,在这个年龄段,这一群体中有一半人会感染两次。RSV感染通常发生在秋季和冬季,高峰期持续3至5个月,全球每年约有6400万儿童感染RSV,每年有 336,000 名老年人因 RSV 住院。
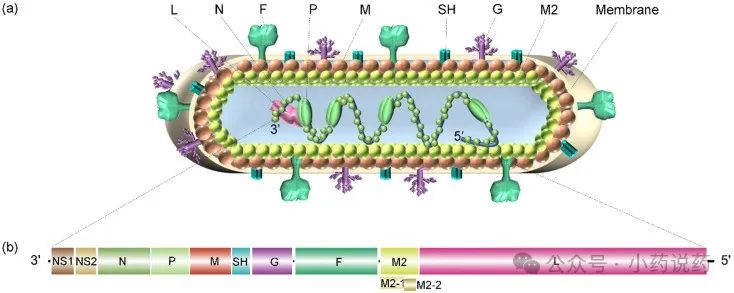
RSV是一种包膜球形RNA病毒,属于肺炎科正肺病毒属;当感染发展时,RSV会使细胞融合形成大细胞,称为合胞体。病毒的结构主要由三种膜蛋白组成:一种小疏水蛋白(SH)、一种附着糖蛋白(G)和一种融合蛋白(F),其中G蛋白与F蛋白在细胞融合中起着重要作用,同时也是刺激机体产生保护性抗体的蛋白。根据G蛋白序列,可以分为亚型A和B。这两种亚型在流行季节同时传播,但通常每年都有其中一种占主导地位。这种病毒的复制周期容易出错,允许快速产生突变,从而导致RSV毒力的变化以及制备抗病毒药物或疫苗的困难。
尽管许多单克隆抗体(mAb)对RSV A和RSV B都有交叉反应,但一些针对RSV A位点Ø的mAb对RSV B没有中和活性或中和活性较低,这表明存在“亚群特异性免疫”。这些差异对RSV预防措施(单克隆抗体和疫苗)具有潜在影响,这可能解释感染后免疫反应和临床严重程度的差异。
RSV膜蛋白结构的差异
RSV分为两个主要亚群,RSV A和RSV B,RSV A和RSV B亚群主要基于RSV G抗原和序列变异,RSV G是变异最大的RSV基因序列。这两个亚群中的可以进一步区分和鉴定几种基因型。尽管没有达成共识的基因型定义标准,但已描述了15种不同的RSV B基因型和9种不同的RSV A基因型。

呼吸道合胞病毒在全球范围内不断进化,多年来出现了新的基因型。RSV B的基因型多样性大于RSV A,RSV A毒株可以分为9种不同的基因型,但至少有37种RSV B基因型被报道。这很可能是由于RSV B的全基因组进化率高于RSV a。然而,值得注意的是,最近对全球数据库的分析表明,RSV A中G蛋白的核苷酸多样性是RSV B的三倍。
RSV F蛋白在RSV A和RSV B中比RSV G蛋白更保守,是疫苗和单克隆抗体开发的主要靶点。RSV F蛋白在RSV A和B之间仅相差25个氨基酸。F蛋白含有融合前和融合后构象共享的抗原位点,以及每种构象独有的位点。RSV F蛋白上定义了六个主要的抗原位点(Ø,I,II,III,IV,V)。一些抗原位点在Pre-F和Post-F上都有表达,而其他位点仅在一种构象上存在。抗原位点I、II、III和IV存在于Pre-F和Post-F构象中,并呈现不同的亲和力;抗原位点Ø和V仅存在在Pre-F构象中,对中和抗体具有最高的亲和力。

尽管RSV F相对保守,但它仍在不断进化。随着时间的推移,已经观察到氨基酸序列的变化。在中国的一项研究中,发现RSV F存在多种氨基酸差异,位于多个抗原位点,在RSV A和RSV B之间有所不同。在美国的一项研究中,RSV B的F抗原位点的变化比RSV A更频繁,主要发生在RSV-B F的抗原位点V(99.6%)、Ø(18.6%)和IV(7%)。在中国的另一项研究中,RSV A和RSV B之间的RSV F氨基酸序列同源性为89-90.6%,在单克隆抗体的靶位点II发现了更多的突变。
RSV A和RSV B的全球分布
这两种毒株通常在一个季节内共同传播,其优势因季节和国家而异。在1990年至2021年期间,在29个国家分析的138个RSV流行季节中,RSV A在76个季节中占主导地位(55.1%),RSV B在54个季节中占据主导地位(39.1%),8个季节(5.8%)没有明显优势。
在分析的104个季节中,有关于特定季节亚组优势的数据。RSV A的优势百分比从2014年之前的76%(37/49)下降到2014年之后的40%(22/55)。RSV B亚群的优势从24%(12/49)增加到53%(29/55)。这两个分组每年都在继续变化,其主导地位因国家而异。最常见的RSV A基因型是NA1(76.30%),最常见的RSV B基因型是BA(70.65%)。
中和抗体的差异
人血清中的RSV中和活性主要来源于靶向融合前构象的F蛋白的抗体,更具体地说是抗原位点Ø和V。免疫学分析表明,超过85%的高效抗体对Pre-F特异性。此外,Pre-F特异地抗体比Pre-F和Post-F交叉反应抗体更有效,也比Post-F特异性抗体更有效。相比之下,G蛋白特异性血清没有观察到病毒中和活性。因此,目前大多数单克隆抗体和疫苗设计工作都集中在RSV F蛋白上。
成年人自然感染诱导的大多数中和抗体对A和B亚群都有活性。它们能够中和多种临床分离株,并显示出体内保护作用。这些研究证实,Pre-F具有高度保守的表位,因此是RSV疫苗和mAbs的理想靶标。然而,一些研究也表明,许多靶向位点Ø的抗体对RSV A的中和效力高于对RSV B的中和效力。
靶向位点Ø的单克隆抗体在两个不同的RSV亚群之间的中和效力差异最大。一些针对RSV A位点Ø的单克隆抗体对RSV B没有或几乎没有中和活性。事实上,两种位点特异性单克隆抗体已经得到了很好的表征:5C4和D25。它们识别抗原位点Ø,但角度不同。5C4能有效中和一组RSV A亚群毒株,但对RSV B亚群毒株的中和活性有限。相比之下,D25能有效中和两个RSV亚群的毒株。这些结果表明,中和抗体与关键的RSV表位(如抗原位点Ø)的结合存在差异。
虽然诱导强效中和抗体是大多数疫苗开发计划的主要目标,但CD4和CD8 T细胞在清除感染细胞方面起着关键作用,因此对RSV感染具有保护作用。
使用计算方法,预测RSV表面蛋白具有很强的引发T细胞免疫的潜力,其中F蛋白可能具有较高的T细胞表位密度。计算结果表明,RSV表面蛋白可能刺激对保护性免疫至关重要的T细胞。多功能性是指T细胞执行一系列功能的能力,包括在单细胞水平上同时分泌细胞因子、趋化因子或细胞毒性颗粒。多功能T细胞的存在可能是免疫性疾病控制的标志,它们在RSV保护性免疫中的作用尚不清楚。研究发现,在65岁以下的健康成年人中,急性和最近感染RSV的患者在入组时的CD4+和CD8+记忆T细胞的T细胞多功能性均低于未感染组。这表明,多功能RSV特异性记忆T细胞的存在可能有助于防止再次感染。
更重要的是,虽然在研究期间,RSV B是主要的循环亚群,并且观察到针对RSV B的中和抗体反应比针对RSV A更强。但在暴露于RSV-A F蛋白肽库后,所有T细胞亚群的多功能性都高于暴露于RSV-B F蛋白肽库。目前尚不清楚这种反应的差异是否反映了这些成年人在之前的呼吸季节中受到的影响。
呼吸道合胞病毒可引起从轻度感冒到严重呼吸道疾病的一系列症状。并发症与流感和其他呼吸道病毒引起的并发症相似,可能包括肺炎、心肺并发症并可能导致死亡。在美国进行的两项研究表明,与RSV A和RSV B毒株相关的疾病临床分类在两个亚组之间似乎有所不同。RSV B型儿童毛细支气管炎的发生率较低(p=0.025),而哮吼发作率较高(p值未报告)。在芬兰的一项研究中也得到了类似的结果,其中71%的RSV A感染儿童和59%的RSV B感染儿童患有毛细支气管炎(p=0.02)。然而,使用之前描述的诊断标准,这些发现无法在日本研究人群中得到验证。
在46项报告RSV亚组对临床严重程度影响的研究中,29项研究报告亚组A和B之间的严重程度没有显著差异,14项研究报告称RSV A感染导致更严重的结果,而两项研究报告称RSV B感染导致更为严重的结果。目前,尚未就这一问题达成共识。一些研究特征可能会阻碍对RSV A和RSV B之间临床严重程度差异的确切结论。
RSV A和RSV B亚群都会导致儿童和成人下呼吸道感染住院或死亡。每年,循环亚群的主导地位各不相同,但通常两个亚群在特定季节共同循环。大多数预防措施针对的是亚群之间高度保守的Pre-F蛋白。大多数预防策略针对RSV F的融合前构象,主要是在抗原位点Ø上,该位点也显示出最高的中和效力。中和抗体对RSV A和B都表现出一定程度的交叉活性,靶向位点Ø的抗体对RSV A的中和效力可能比对RSV B的中和效力更大。较高的中和滴度与降低RSV疾病风险有明显的关系。
最近两种稳定的基于Pre-F蛋白的疫苗Arexvy和Abrysvo已在美国和欧洲获得授权,可保护老年人免受RSV相关的下呼吸道疾病。Abrysvo还表明可以通过母体疫苗接种保护婴儿免受RSV的侵害。单价疫苗Arexvy基于源自RSV A2毒株F蛋白的RSV PreF3抗原,而二价RSV疫苗Abrysvo基于来自RSV A基因型Ontario(on)和RSV B基因基因型Buenos Aires(BA)的Pre-F蛋白。基于这两个亚群抗原的疫苗和免疫产品可能具有各种优势,例如限制免疫逃逸的风险,并可能限制对F表位的选择压力。随着中和抗体随时间的推移而减弱,并且亚群优势随季节自然变化,针对RSV A和B亚群的特异性保护性免疫的不同持久性可能会变得更加明显。
参考文献:
1.Differences Between RSVA and RSV B Subgroups and Implications for Pharmaceutical Preventive Measures. Infect Dis Ther. 2024 Aug; 13(8): 1725–1742.
公众号内回复“肿瘤免疫”或扫描下方图片中的二维码免费下载《小药说药肿瘤免疫全集》的PDF格式电子书!

公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。





































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论