据药融云药品审评数据库统计,2022年1月,共有5款1类新药报产。含3款生物制品、1款化药和1款中药。分别是上海盛迪医药的阿得贝利单抗注射液、贝达药业的伏罗尼布片、我武生物的葎草花粉点刺液、博锐生物制药的泽贝妥单抗注射液以及华春生物的太子神悦胶囊。而在2021年1月,国内报产的1类新药仅2款。
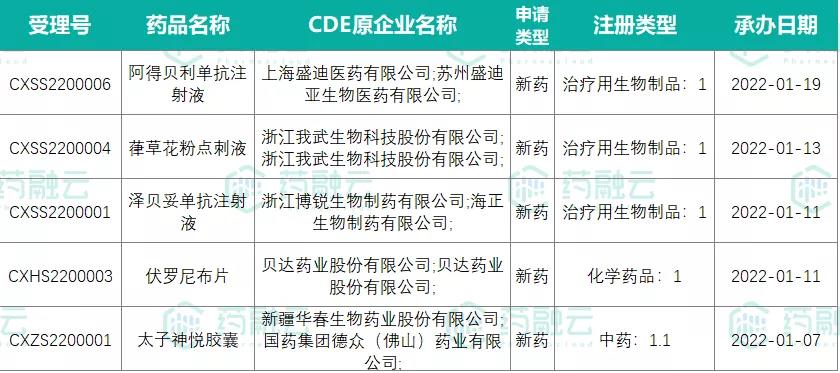
数据来源:药融云药品审评数据库
阿得贝利单抗注射液:国产第5家报产的PD-L1单抗
阿得贝利单抗是由恒瑞医药自主研发的人源化抗PD-L1单克隆抗体,是我国申报上市的第5款PD-L1单抗,之前还有思路康瑞的恩沃利单抗、基石药业的舒格利单抗获批,分别为国产PD-L1单抗的第一和第二。兆科药业的首克注利单抗和科伦药业的泰特利单抗也已提交了NDA。
据了解,阿得贝利单抗能通过特异性结合PD-L1分子从而阻断导致肿瘤免疫耐受的PD-1/PD-L1通路,重新激活免疫系统的抗肿瘤活性,从而达到治疗肿瘤的目的。据悉,阿得贝利单抗注射液相关项目累计已投入研发费用约2.74亿元。
伏罗尼布片:用于二线晚期肾癌
伏罗尼布片(CM082片,简称“伏罗尼布”)是具有全新化学结构的新一代多靶点激酶抑制剂,可抑制肿瘤血管生成及生长,用于多种癌症的治疗。此次报产,适应症为与依维莫司联合拟用于治疗既往接受过抗血管酪氨酸激酶抑制剂治疗失败的晚期肾细胞癌(RCC)患者,该上市许可申请已获得NMPA受理。
这是贝达药业第4款报产的1类新药。据新闻稿,目前尚无治疗肾癌的国产创新药物上市,伏罗尼布或将成为中国第一个用于治疗晚期肾癌的国产1类新药,填补国内空白。
贝达药业在2021ASCO年会上公布了伏罗尼布联合依维莫司治疗肾癌患者的II/III期临床(CONCEPT研究)结果。结果显示,与依维莫司单药相比,伏罗尼布联合依维莫司对转移性RCC患者有PFS获益,且具有安全耐受性。
此前,贝达药业通过控股子公司Equinox拥有伏罗尼布眼科适应症的海外权益,通过控股子公司Xcovery Holdings拥有伏罗尼布肿瘤适应症的海外权益,通过全资子公司卡南吉拥有伏罗尼布全部适应症的中国权益。
葎草花粉点刺液
葎草花粉点刺液用于点刺试验,辅助诊断因葎草花粉致敏引起的I型变态反应性疾病。经查询,截至1月13日,获得国家药品监督管理局批准上市的变应原点刺产品均为尘螨类,分别为公司的“粉尘螨皮肤点刺诊断试剂盒”(国药准字S20080010)、“屋尘螨皮肤点刺诊断试剂盒”(国药准字S20190022),以及ALK-Abello的“螨变应原皮肤点刺试剂盒”(国药准字SJ20150031)。
泽贝妥单抗注射液:首个国产CD20新药
泽贝妥单抗注射液(研发代号:HS006,商品名:安瑞昔)是博锐生物/海正生物自主研发的1类创新型CD20单抗,用于初治CD20阳性弥漫大B细胞性淋巴瘤(DLBCL)。这是博锐生物获得NMPA受理的第一个1类创新型生物药上市申请,也是博锐生物继英夫利西单抗 、阿达木单抗 、注射用重组人II型肿瘤坏死因子受体-抗体融合蛋白 、托法替布获批上市后,第5个申请上市的产品。
泽贝妥单抗(HS006)是一种人-鼠嵌合型单克隆抗体,能特异性地与B细胞表面CD20抗原结合,并通过抗体依赖的细胞介导的细胞毒作用(ADCC)和补体依赖的细胞毒作用(CDC)等清除B细胞。
目前国内上市的CD20单抗创新药包括罗氏的利妥昔单抗(已有信达生物、复宏汉霖有生物类似药在国内获批上市)和奥妥珠单抗(独家产品)以及诺华的奥法妥木单抗(独家产品)。
太子神悦胶囊
太子神悦胶囊由华春生物和国药德众联合申报。据新闻稿,该药是目前治疗轻、中度抑郁症的纯中药新药,是中国第一个原创性抗抑郁中药,与经典化学药氟西汀相比,太子神悦胶囊有效性与其相当,其安全性有一定优势。经查询,国内首款获批的抗抑郁中药1类新药为以岭药业的苏夏解郁除烦胶囊,于2021年12月获批上市。
药融云数据库 https://www.pharnexcloud.com/

想要了解更多数据内容吗?欢迎注册药融云数据库!注册立享15天免费使用和虎年首份医药数据大礼包!
—END—





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论