

18983288589(微信同号)

18983288589(微信同号)

18908392210(微信同号)

18980413049


2022-11-07
国卫办医函〔2022〕370号
其他
中国
现行有效
2022-11-07
国家卫生健康委办公厅
国家检验医学中心设置标准
一、基本要求
国家检验医学中心应依托检验学科特色突出的三级甲等综合医院,在全国检验医学领域处于引领地位,并具有较好的国际影响力。临床检验项目齐全,检验配套设施设备完善,人才梯队结构合理,有相对成熟合理的检验医学组织管理运行机制。 始终坚持公益性,认真贯彻落实国家相关卫生健康政策,积极承担医学教育人才培养工作,组织全国检验医学协同网络开展 相关临床、教学、科研、公共卫生服务等创新工作和技术指导,组织协调检验医学的国内外学术交流与合作,引领国家检验医学发展,推动检验医学走向国际,为临床疾病预防、诊断、治疗和学科发展提供坚实的检验医学支撑。
国家检验医学中心应当满足以下基本条件:
(一)检验医学科通过 ISO 15189 医学实验室认可。
(二)检验医学科获得国家临床重点专科建设项目。
(三)检验医学科为博士学位授权点。
(四)以下与检验医学密切相关的临床科室中获得国家临床重点专科建设项目科室≥10 个,包括内分泌科、心血管内科、重症医学科、血液病科、急诊科、肾脏病科、风湿免疫科、呼 吸内科、神经内科、消化内科、感染科、妇科、产科、儿科、肿瘤科、普通外科、器官移植科、皮肤科。
(五)临床常规开展检验项目数≥800 项,年总检测工作量≥2500 万项次。
(六)病原微生物实验室依法取得所开展病原微生物实验活动的相应资质。
二、医疗服务能力
国家检验医学中心应当具备重大疾病以及疑难病与危重症和突发传染病诊疗相关检验能力,具备辐射和指导基层检验服务能力和水平提高的能力。
(一)科室及平台设置。
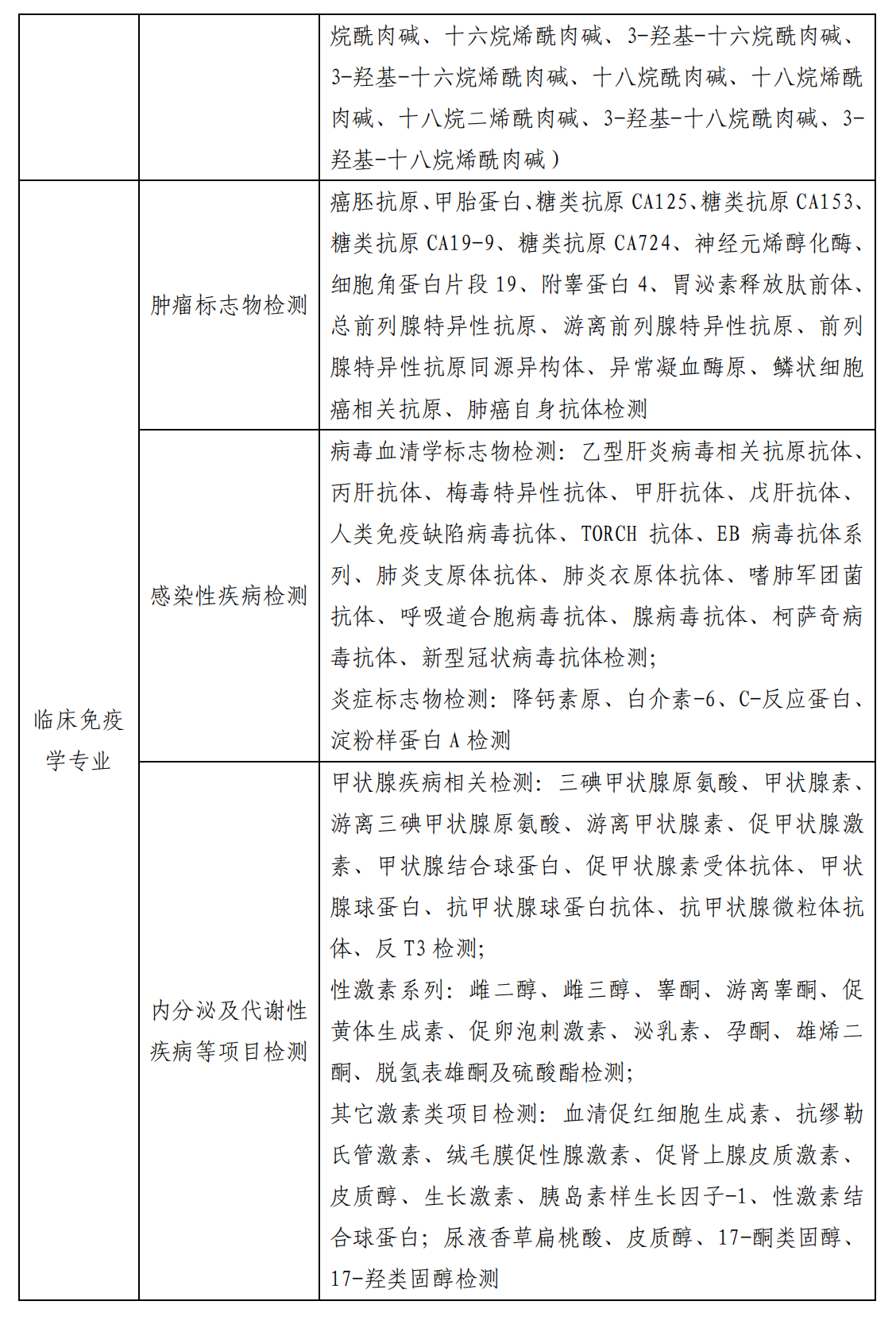
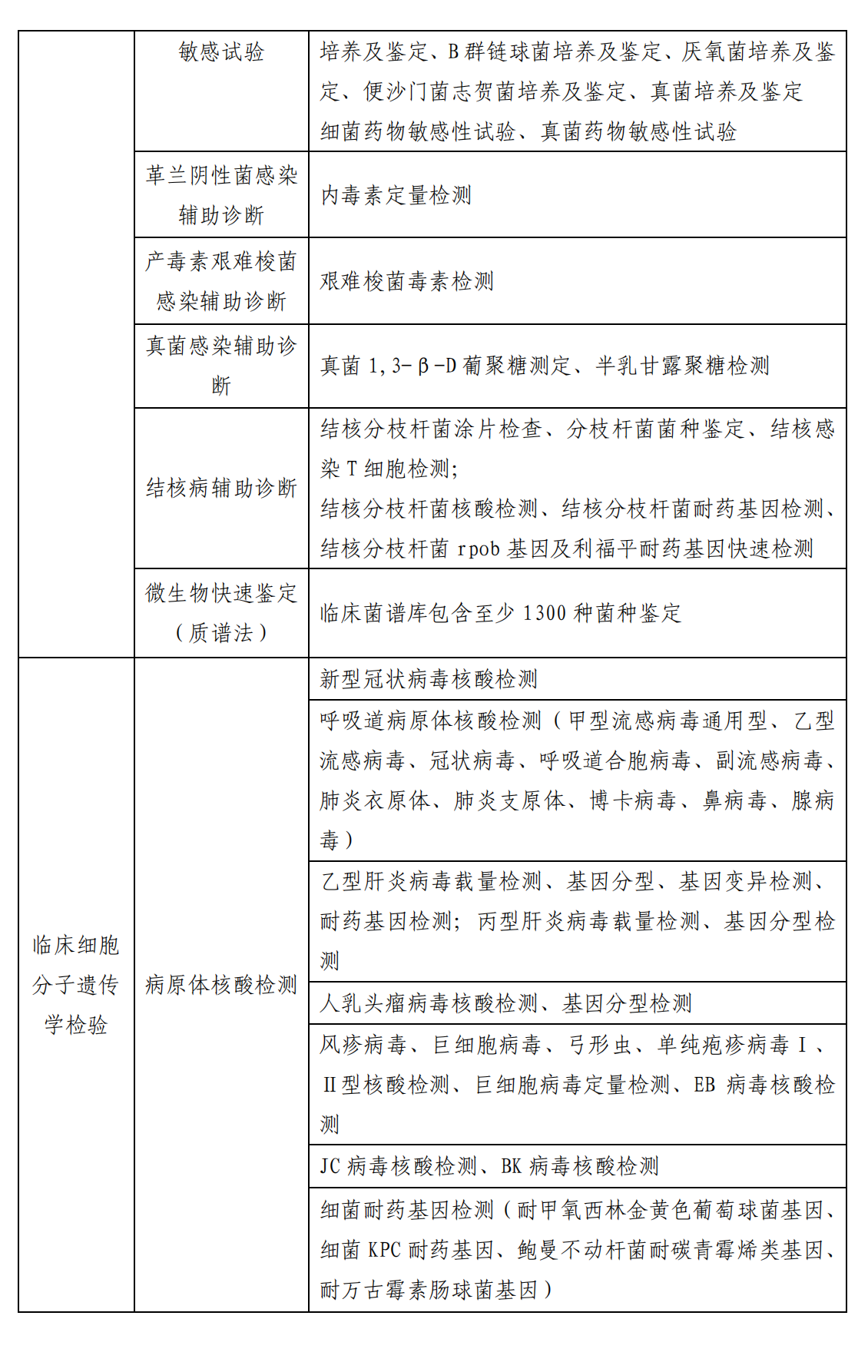
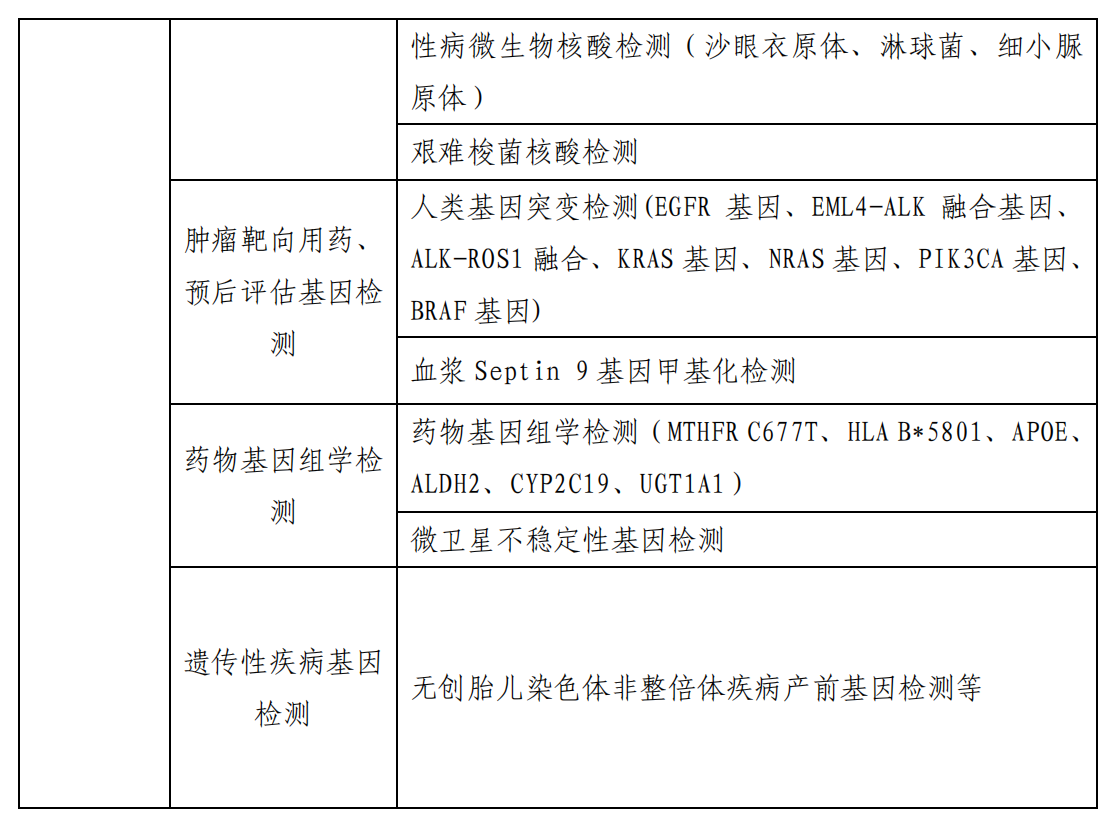
1.具有包括临床体液、血液检验;临床微生物学检验;临床化学检验;临床免疫、血清学检验;临床细胞分子遗传学检验在内的专业划分,配套设施、设备完善。近 3 年,开展检验项目覆盖必备检验项目清单(见附表)。
2.依托医院具备或有可共享的生物安全三级实验室,有重大及突发传染病鉴定、检测能力者优先考虑;遵守病原微生物实验室生物安全相关法律法规,符合 GB 19489 要求,通过生物安全认可者优先考虑。
3.具备先进的检测技术平台以及规范的实验室自建项目管理体系和能力,具有新发突发传染病病原体鉴定与检测能力。检测技术平台包括:流式平台,并开展检测项目≥50 项;质谱平台,并开展临床检测项目≥50 项;高通量基因测序平台,具备高通量基因测序的能力并已开展临床检验项目。
4.具有稳定的检验医师队伍,总人数应≥5 人。
(二)牵头制定本领域标准或技术指南。曾牵头制定国家标准或卫生行业标准≥5 项,牵头制定行业技术指南≥1 项,并在全国推广应用。
三、教学能力
高度重视医学教育和人才培养工作,具有完整的临床医学人才培养体系,能够承担院校医学教育、毕业后医学教育和继续医学教育,教学能力与硬件设施能满足教学需求,引领我国检验医学学科人才培养高质量发展。
(一)教学条件。符合院校教育和国家住院医师规范化培训有关要求。具有检验医学本科、硕士、博士研究生学位授权点和博士后流动站,并具备相应完整的教学体系。
(二)组织管理。建立完备的组织管理体系,具有完善的毕业后医学教育管理制度和继续医学教育管理制度。设有教学相关委员会,明确承担教学职能的部门,人员能够满足教学需 求,各项教学工作负责人职责清晰。建立健全教学质量保证机制、教学结果评价与反馈体系,贯彻教学质量持续改进机制。
(三)师资条件。检验医学专业带教师资数与住院医师规范化培训对象的数量比例符合国家要求。建立师资遴选、培训、考核、激励与约束机制,医院和科室均建立有效的教学激励机制。具备承办全国医学教育师资培训的条件。
(四)教学培训。为国家住院医师规范化培训基地检验医学专业基地,积极承担国家检验医学专业住院医师规范化培训和省级以上考核任务。近 3 年,累计检验医学专业住院医师规范化培训人数≥10 人(含临床医学硕士专业学位研究生),结业考核通过率≥95%。具备承担检验医学专业领域国家级继续教育项目的能力。
(五)研究生培养。检验专业领域研究生导师≥15 人(其中博导≥5 人)。有教育部高等学校医学技术类教学指导委员会委员≥1 人。近 3 年,平均每年培养检验医学专业博士、硕士研 究生毕业≥15 人。加强教学工作高质量发展,建有不断完善的高质量人才培养机制,近 3 年,累计培养省级及以上优秀毕业生≥3 人或优秀研究生论文≥3 篇。培养熟练掌握现代检验技术技能和检验医学研究的高水平人才。
(六)教学成果。在检验领域,获国家级教学团队或国家精品课程或国家级精品资源共享课程;近 3 年,主编国家级规划教材≥1 部,获评国家一流本科专业、国家一流本科课程。
四、科研能力
(一)平台建设与科研人才队伍。
1.所在单位已依法进行药物临床试验机构备案。若为本专业国家医学检验临床医学研究中心依托单位或国家重点实验室或国家工程研究中心者优先考虑。
2.学科带头人具备以下条件者优先:中国科学院或中国工程院院士(检验医学专业);曾任、现任或候任中华医学会检验医学分会主委或中国医师协会检验医师分会会长;教育部长江学者特聘教授;国家自然科学基金杰出青年。具有较强的国际影响力。
3.科室核心人才队伍具备以下条件者优先:现任中华医学会检验医学分会常委、中国医师协会检验医师分会常委;近 3 年,主持国家级重大、重点科研项目(国家科技重大专项、国家重点研发计划、国家科技支撑计划项目及课题,国家自然科学基金重大或重点项目)≥3 人;主持国家自然科学基金≥10 人。
(二)科研项目。近 3 年,主持国家级重大、重点科研项目(国家科技重大专项、国家重点研发计划、国家科技支撑计划项目及课题,国家自然科学基金重大或重点项目、国家杰出青年科学基金项目)≥3 项;主持国家自然科学基金项目数量≥ 10 项。
(三)科研成果。
1.以第一完成单位曾获得国家级科技成果奖励≥1 项。
2.获得授权国家、国际发明专利累计≥5 项。
3.近 3 年,作为第一作者或通讯作者单位发表高水平文章,其中年均发表中科院二区及以上论文≥10 篇。
(四)研究资源。
1.已建立健康人群标本及信息库,生物样本数量≥5 万份。
2.已建立重大慢性病及重大传染病队列、标本库及信息库,生物样本总数量≥100 万份,具有完善的管理系统。
(五)专业化科研支持和转化研究平台。
1.具备完善的医学检验研究支撑平台,配备代谢组学、蛋白组学、基因组学、宏基因组学、病毒学、免疫学等基础与转化研究平台。
2.应当具备高新检验技术和新生物标志物研发、转化应用及示范推广的能力。
3.近 3 年,牵头开展临床检验相关全国多中心临床试验。
(六)协同研究网络。具备建立覆盖全国 31 个省、自治区和直辖市的检验协同研究网络的能力,建立临床、基础和相关企业的多学科多渠道的协同攻关机制。
五、承担公益性任务及应对重大公共卫生事件的能力
(一)参与国家卫生政策的制定。参与检验医学相关的国家卫生政策制定以及国家重大、突发公共卫生事件应对策略的制定。
(二)具备新发突发传染病应对能力。具备新发突发传染病核酸大规模检测能力,配置核酸检测平台≥5 套;检验人员中熟练掌握 PCR 检测技术人数≥50 人;具备病毒核酸检测能力≥ 10000 人份/日,并能够短期内进一步拓展。建有检验技术专家团队和医疗队,并具有开展检验相关科技攻关的研究平台和专业人员。
(三)具备重大传染病病原体监测能力。是国际或国家级重大传染病病原体监测网络成员单位,具备监测病原体流行及耐药的技术能力。
(四)开展检验医学科普和宣教工作。通过线下、线上多种途径开展面向患者及公众的检验科普宣传,提升公众对检验医学知识的认识和理解,服务于大众健康。
六、落实医改相关任务及医院管理情况
(一)推进建设覆盖全国的检验医学协作网络。具备建立覆盖全国 31 省、自治区和直辖市各级医疗机构协作网络的能力,开展检验技术和质量管理培训,加速卫生行业标准的推广应用,推进先进检验技术的普及,加强对基层检验机构的技术帮扶。
(二)推进检验结果互认共享。牵头全国多中心临床研究,加快建立参考区间国人标准,并在全国各级医院推广使用;统一临床检验标准,推动检验结果互认共享。
(三)信息化建设。基于医院信息平台强化检验信息化标准化建设,系统功能覆盖样本接收、检验进程跟踪、检验质量控制、报告自动审核的检验全过程,扩大自动审核的覆盖项目 及自动审核通过率,提高检测能力,并促进检验标准化及同质化建设。利用信息化管理实现检验医学科人、财、物优化配置,提高管理水平。
(四)检验大数据开发。深度挖掘检验大数据,探索在构建检验项目参考区间、疾病早期诊断和风险预测模型、检验图像智慧识别等方面的运用,提高检验指标的诊断效能,做好检验数据和个人信息安全保护工作。
(五)医院管理。建立健全现代医院管理制度,以章程为统领规范医院内部管理。公立医院应当落实“两个允许”,人员支出占医院业务支出的比重逐年提升。
附表:必备检验项目清单




Pharma CMC2024-10-15

摩熵医药(原药融云)2024-08-21
数屿医械2024-06-24
数屿医械2024-06-13
数屿医械2024-05-30
摩熵医药(原药融云)2024-05-27
药事纵横2024-02-28
药通社2023-12-26
摩熵医药(原药融云)2023-12-13
药通社2023-06-25
2024-11-20
2024-11-19
2024-11-19
2024-11-19
2024-11-19
2024-11-19
2024-11-18
2024-11-18
2024-11-18
2024-11-11
2024-11-11
2024-11-05
2024-11-04
2024-11-04
2024-10-30
2024-10-22
2024-09-23
2024-09-11
2024-09-09
2024-09-09
2024-08-13
2024-07-31
2024-07-30
2024-07-29
2024-07-29
2024-07-29
2024-06-25
2024-06-06
2024-05-31
2024-05-28
2024-11-19
2024-11-19
2024-11-11
2024-10-30
2024-10-29
2024-10-28
2024-10-24
2024-10-24
2024-10-22
2024-10-22
2024-10-22
2024-10-22
2024-10-21
2024-10-21
2024-10-17